Clear Sky Science · ru
Механистические данные о структуре и функции С‑концевого хвоста RecA
Как бактерии справляются со стрессом ДНК
Бактерии постоянно подвергаются воздействиям, повреждающим их ДНК — от антибиотиков до излучения. Тем не менее они часто выживают и даже становятся труднее убиваемыми. В этом исследовании подробно изучается ключевой бактериальный белок RecA, который помогает восстанавливать разрывы ДНК и запускать аварийную программу, известную как SOS‑ответ. Авторы сосредоточились на небольшом гибком хвосте на одном конце RecA, который долгое время ускользал от структурных исследований, и показали, как этот крошечный фрагмент действует как встроенный тормоз и переключатель для репарации ДНК и выживания при воздействии антибиотиков.
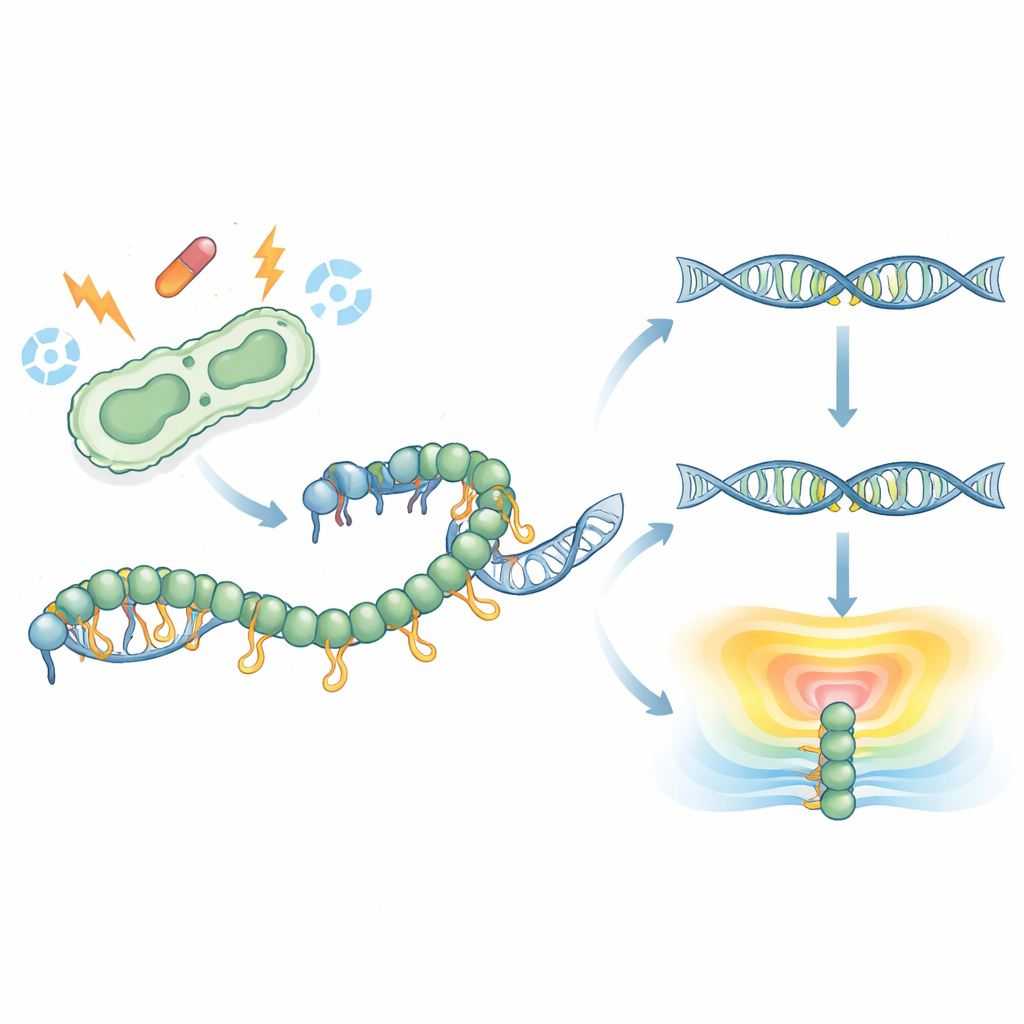
Молекулярный первый взгляд на скрытый хвост
RecA обвивает одиночные цепи ДНК, формируя филамент, который обеспечивает репарацию ДНК и активирует SOS‑ответ. Предыдущие структуры никогда не захватывали подвижный С‑концевой хвост RecA, поэтому его роль оставалась загадкой. Здесь исследователи решили структуру полного RecA от патогена Klebsiella pneumoniae в высоком разрешении, связанную с молекулой, подобной ATP. К их удивлению, часть хвоста свернулась в короткую упорядоченную полосу и протянулась, чтобы контактировать с центральной моторной областью молекулы RecA в соседнем филаменте. Это взаимодействие объединяет отрицательно заряженные участки хвоста с положительными зарядами в ядре, раскрывая ранее не виданный способ, которым молекулы RecA могут соприкасаться друг с другом и собираться в высшие структуры.
Встроенный тормоз для связывания с ДНК и репарации
Поскольку хвост располагается близко к областям связывания ДНК у RecA, команда проверила, как он влияет на контакт с ДНК. С помощью гель‑сдвиговых анализов они показали, что варианты RecA без хвоста или с изменениями зарядов в хвосте захватывали как одноцепочечную, так и двухцепочечную ДНК более прочно, чем нормальный белок. Электронная микроскопия подтвердила, что эти изменённые белки формировали более длинные филаменты RecA на коротких фрагментах ДНК, чем белок в полном виде. В прямых экспериментах по обмену цепей, имитирующих суть гомологичной рекомбинации, RecA без хвоста или с мутациями в хвосте выполнял обмен ДНК более эффективно. В совокупности эти результаты показывают, что хвост обычно действует как автоингибирующий элемент: он затрудняет связывание RecA с ДНК, его наращивание вдоль молекулы и проведение обмена цепей, что помогает предотвращать неконтролируемую рекомбинацию на интактных хромосомах.
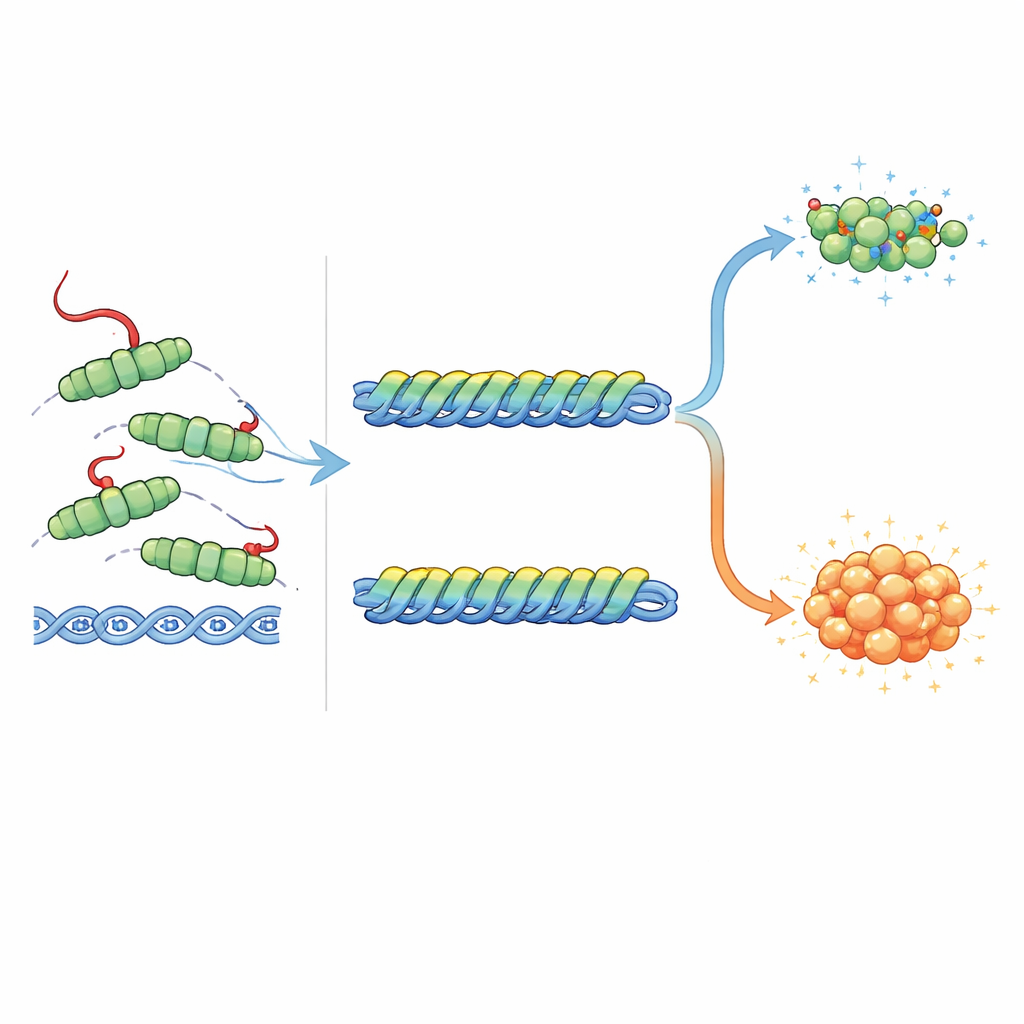
Тонкая настройка бактериального SOS‑тревожного сигнала
Функция RecA — не только ремонт ДНК, но и запуск SOS‑ответа путём содействия саморазрезанию двух других белков, LexA и UmuD. LexA обычно удерживает гены SOS в неактивном состоянии; при его расщеплении эти гены включаются. Расщепление UmuD даёт партнёра для специальной ошибкоёмкой ДНК‑полимеразы, которая может обходить повреждения, но при этом вносит мутации. Авторы обнаружили, что хвост RecA оказывает противоположные эффекты на эти два саморазрезания. Полноразмерный RecA с интактным хвостом наиболее эффективно стимулировал расщепление LexA, тогда как версии без хвоста или сильно изменённые были менее эффективны. Наоборот, те же варианты без хвоста и мутации лучше стимулировали расщепление UmuD по сравнению с обычным белком. Сопоставление структур даёт объяснение: хвост может удобно располагаться рядом с связанной LexA и даже формировать благоприятные зарядовые взаимодействия, тогда как он физически и электроstatически конфликтовал бы с связанной UmuD′. Иными словами, хвост помогает включать SOS‑сигнал, одновременно сдерживая наиболее мутагенную ветвь ответа.
Влияние на ответ на антибиотики в живых клетках
Чтобы проверить, как это проявляется в бактериях, исследователи сконструировали штаммы Escherichia coli, в которых флуоресцентный репортер светится при активации раннего гена SOS, называемого recN. Затем они обработали эти штаммы двумя повреждающими ДНК препаратами: митомицином C и широко используемым антибиотиком ципрофлоксацином. Клетки с нормальным RecA демонстрировали сильную активацию SOS. Клетки без хвоста однако давали значительно более слабые флуоресцентные сигналы, что согласуется с уменьшенным расщеплением LexA и приглушённым SOS‑ответом. Мутантные хвосты, которые усиливали связывание с ДНК и образование филаментов, напротив, часто вызывали ещё более сильный SOS‑ответ. Результаты в клетках соответствуют биохимическим данным и подчёркивают роль хвоста в балансировании репарации, выживания и мутаций при антибиотическом стрессе.
Почему этот небольшой хвост важен
Эта работа выявляет С‑концевой хвост RecA как тонкий, но мощный регулятор поддержания бактериального генома. Контактируя с ядром белка и смещая ДНК и партнёрские белки ближе или дальше, хвост замедляет рост филаментов и обмен цепей ДНК, помогает обеспечить адекватное включение SOS через LexA и ослабляет чрезмерно мутагенную репарацию через UmuD. Для широкой публики это важно потому, что RecA и система SOS влияют на то, как быстро бактерии развивают устойчивость к антибиотикам. Понимание структурных и функциональных приёмов этого крошечного хвоста в будущем может направить разработку препаратов, которые смещают баланс в сторону репарации без неконтролируемых мутаций, делая существующие антибиотики более эффективными дольше.
Цитирование: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Ключевые слова: белок RecA, SOS‑ответ, репарация ДНК, устойчивость к антибиотикам, стабильность бактериального генома