Clear Sky Science · sv
Det intrinsiskt oordnade proteinet SPE-56 krävs för acrosomliknande exocytos och fertilitet hos Caenorhabditis elegans
Varför små maskar kan lära oss om fertilitet
Fertilitet hänger på ett dramatiskt ögonblick när en spermie övergår från en tyst, vilande form till en aktiv, äggfusande maskin. Denna studie använder den mikroskopiska rundmasken Caenorhabditis elegans för att avslöja hur ett lite känt spermieprotein, SPE-56, bidrar till att driva den övergången. Eftersom många av de grundläggande stegen i spermieaktivering och membranfusion är gemensamma för djur, kan förståelsen av detta protein i maskar kasta ljus över varför spermier misslyckas i andra arter, inklusive människor.
Från tyst vilocell till aktiv simmare
Både hos hon- och hanmaskar börjar spermier som enkla runda celler kallade spermatider. För att bli kapabla att befrukta måste dessa genomgå en förvandling känd som spermiogenes. Två förändringar är avgörande: interna blåsor kallade membranösa organeller smälter samman med spermions yta, och en flexibel ”fot” kallad pseudopod växer ut så att cellen kan krypa mot ägget. Dessa steg liknar acrosomreaktionen hos mänskliga och andra däggdjurs spermier, där ett specialiserat rum tömmer sitt innehåll och spermieytan omformas strax före befruktningen.
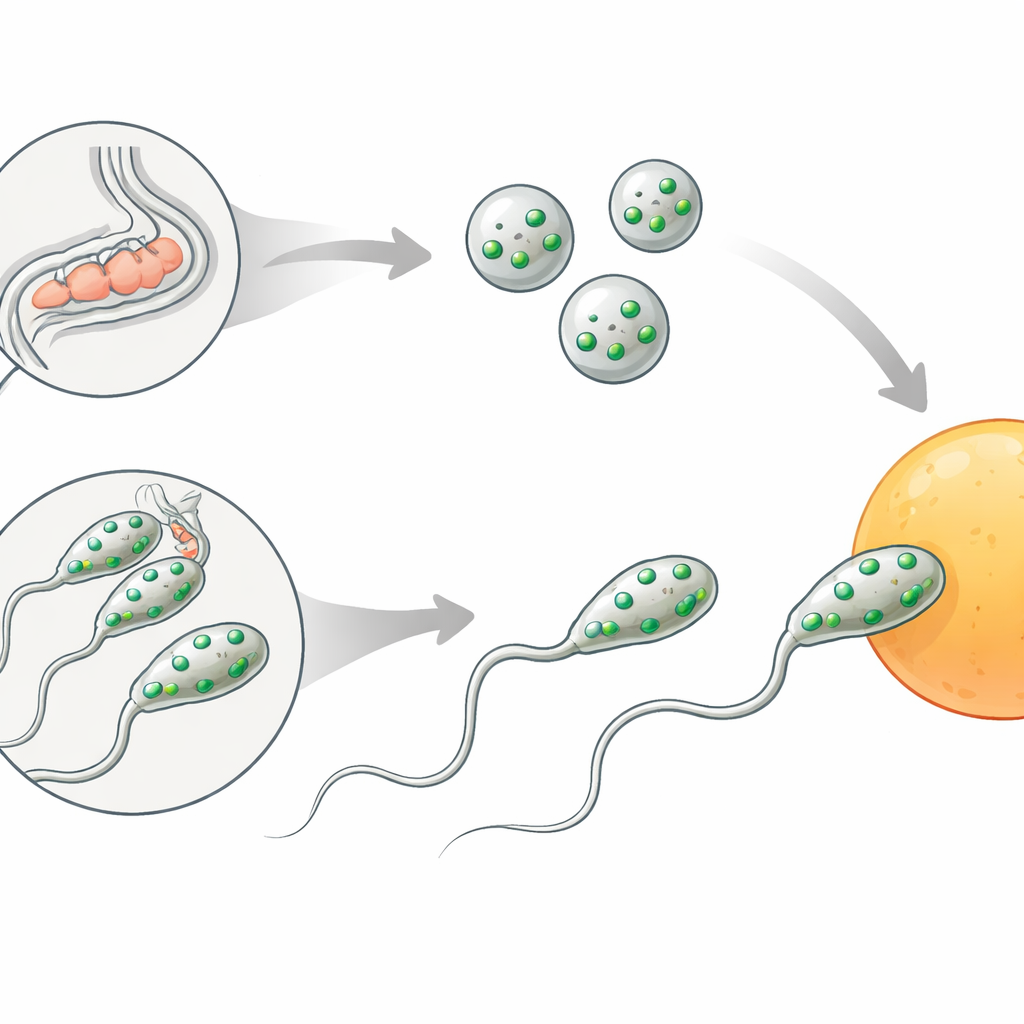
En fertilitetsbrytare gömd i spermier
Författarna fokuserade på en tidigare okarakteriserad gen, nu kallad spe-56. Maskar som saknar spe-56 producerar normala mängder spermier och uppvisar inga uppenbara defekter i kroppsform, rörelse eller äggproduktion. Ändå är dessa djur nästan helt sterila när de förlitar sig på sina egna spermier: de lägger obefruktade oocyter som degenererar i livmodern. När mutanta hermafroditer parar sig med normala hannar återställs fertiliteten, vilket visar att deras ägg och reproduktionskanal fungerar och att problemet ligger i deras egna spermier. På samma sätt kan spe-56-mutanthanar para sig och överföra spermier normalt, men deras spermier förmår inte ge avkomma, vilket åter pekar på ett spermie-intrinsikt fel.
När fusionssteget misslyckas
Närmare granskning visade att spe-56-mutant spermier fastnar under aktiveringen. Under mikroskopet ser deras runda utgångsform normal ut, men efter aktivering växer de bara korta, trubbiga pseudopoder och rör sig dåligt. Med en fluorescerande färg som framhäver membranfusionsplatser observerade forskarna ljusa punkter längs ytan på normala spermier, som markerade där interna organeller hade smält samman med yttre membranet. I kontrast visade spe-56-mutantens spermier en jämn, enhetlig signal utan fusionspunkter, vilket avslöjade att det avgörande fusionssteget hade misslyckats. Genetiska tester placerade spe-56 nedströms kända regulatorer av spermieaktivering, vilket betyder att aktiveringssignalen fortfarande anländer men inte kan omvandlas till fullständig strukturell förändring utan SPE-56.
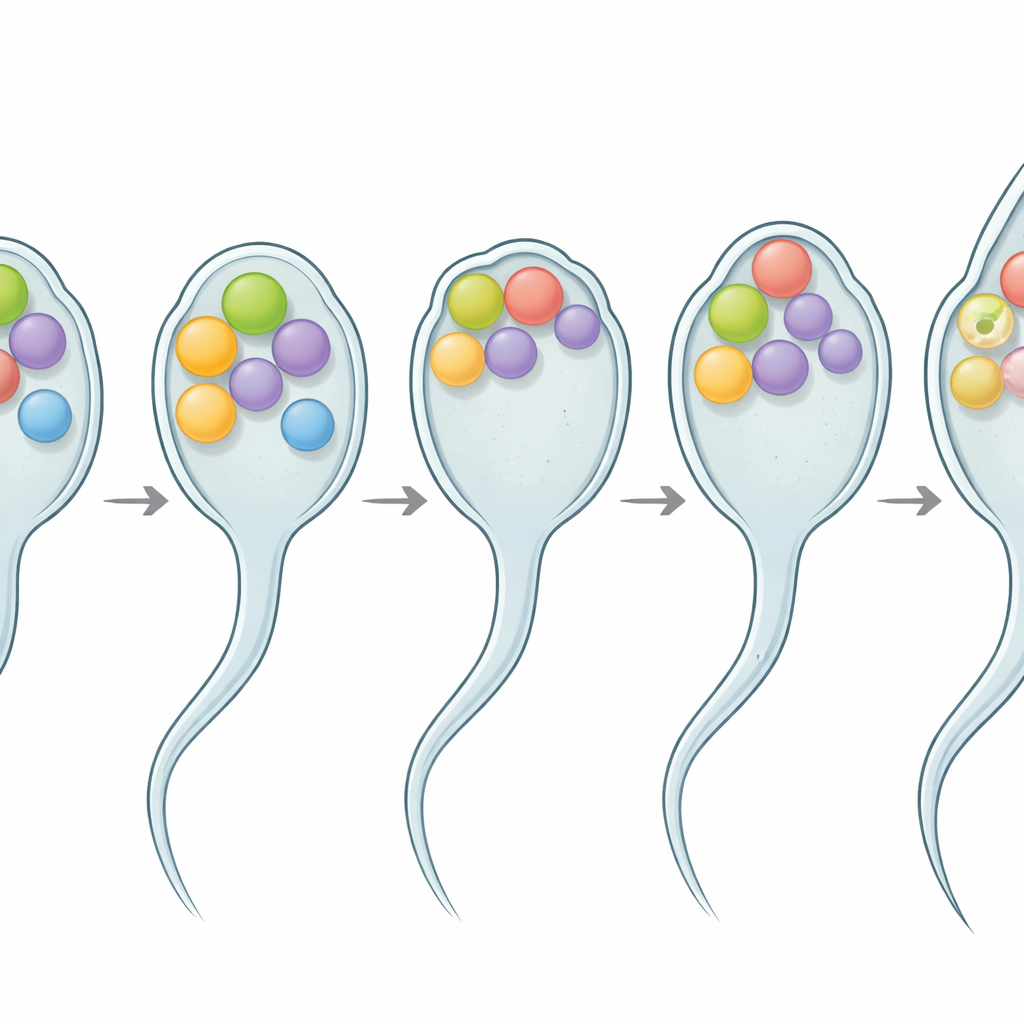
Ett flexibelt protein vid fusionsgränssnittet
Biokemiskt och bildmässigt arbete visade att SPE-56 är ett enpassagemembranprotein som sitter främst på membranen hos de interna organellerna i spermierna. Dess svansregion, som sträcker sig in i cellens inre, saknar en styv form och beter sig istället som ett ”intrinsiskt oordnat” segment — en sladdrig, flexibel kedja snarare än ett fast ställverk. Sådana oordnade regioner erkänns i ökande grad som kraftfulla verktyg celler använder för att böja, omforma och smälta samman membran. Här underminerade borttagning av delar av denna flexibla svans gradvis fertiliteten, särskilt vid högre temperaturer, utan att förändra hur många spermier som producerades. Ju mer av svansen som togs bort, desto allvarligare blev fertilitetsförlusten, vilket tyder på att dess längd och flexibilitet hjälper spermierna att förbli funktionella vid temperaturförändringar.
Hur strukturell löshet kan stödja liv
Sammantaget avslöjar studien SPE-56 som en nyckelaktör i det sista skedet av spermieaktivering hos C. elegans. Utan det fullföljer spermier sällan membranfusionssteget eller bildar en ordentlig krypande pseudopod, och befruktning sker nästan aldrig. Resultaten stödjer en bredare idé: flexibla, oordnade proteinregioner kan fungera som anpassningsbara ”molekylära stötdämpare” som hjälper membraner att komma samman, destabiliseras så pass att de kan fusera och ändå behålla integriteten. Genom att visa hur ett sådant protein bevarar spermiefunktionen över olika temperaturer i en enkel mask pekar detta arbete på en potentiellt bevarad, evolutionärt gammal strategi som kan hjälpa spermier — och andra celltyper — att förbli pålitliga i en föränderlig värld.
Citering: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Nyckelord: spermaktivering, membranfusion, intrinsiskt oordnade proteiner, Caenorhabditis elegans, fertilitet