Clear Sky Science · nl
Het intrinsiek gedesorganiseerde eiwit SPE-56 is vereist voor acrosoomachtige exocytose en vruchtbaarheid in Caenorhabditis elegans
Waarom piepkleine wormen ons iets kunnen leren over vruchtbaarheid
Vruchtbaarheid draait om een dramatisch moment wanneer een zaadcel verandert van een stille, opgeslagen vorm in een actieve, met eieren versmeltende machine. Deze studie gebruikt de microscopische rondworm Caenorhabditis elegans om te onthullen hoe een weinig bekend sperma-eiwit, SPE-56, die overgang helpt aandrijven. Omdat veel van de basale stappen van sperma-activatie en membraanfusie bij dieren gedeeld zijn, kan begrip van dit eiwit in wormen inzicht geven in waarom sperma bij andere soorten, waaronder de mens, faalt.
Van stille zaadcel naar actieve zwemmer
Bij beide wormseksen beginnen spermacellen als eenvoudige ronde cellen die spermatiden worden genoemd. Om bevruchtingsbekwaam te raken, moeten deze een transformatie ondergaan die spermiogenese heet. Twee veranderingen zijn cruciaal: interne blaasjes, membranous organelles genoemd, fuseren met het buitenoppervlak van het sperma, en een flexibel “voetje” genaamd pseudopod groeit uit, waardoor de cel naar het ei kan kruipen. Deze stappen lijken op de acrosomereactie bij menselijke en andere zoogdiersperma, waarbij een speciale compartiment zijn inhoud vrijgeeft en het oppervlak van het sperma kort voor de bevruchting wordt hervormd.
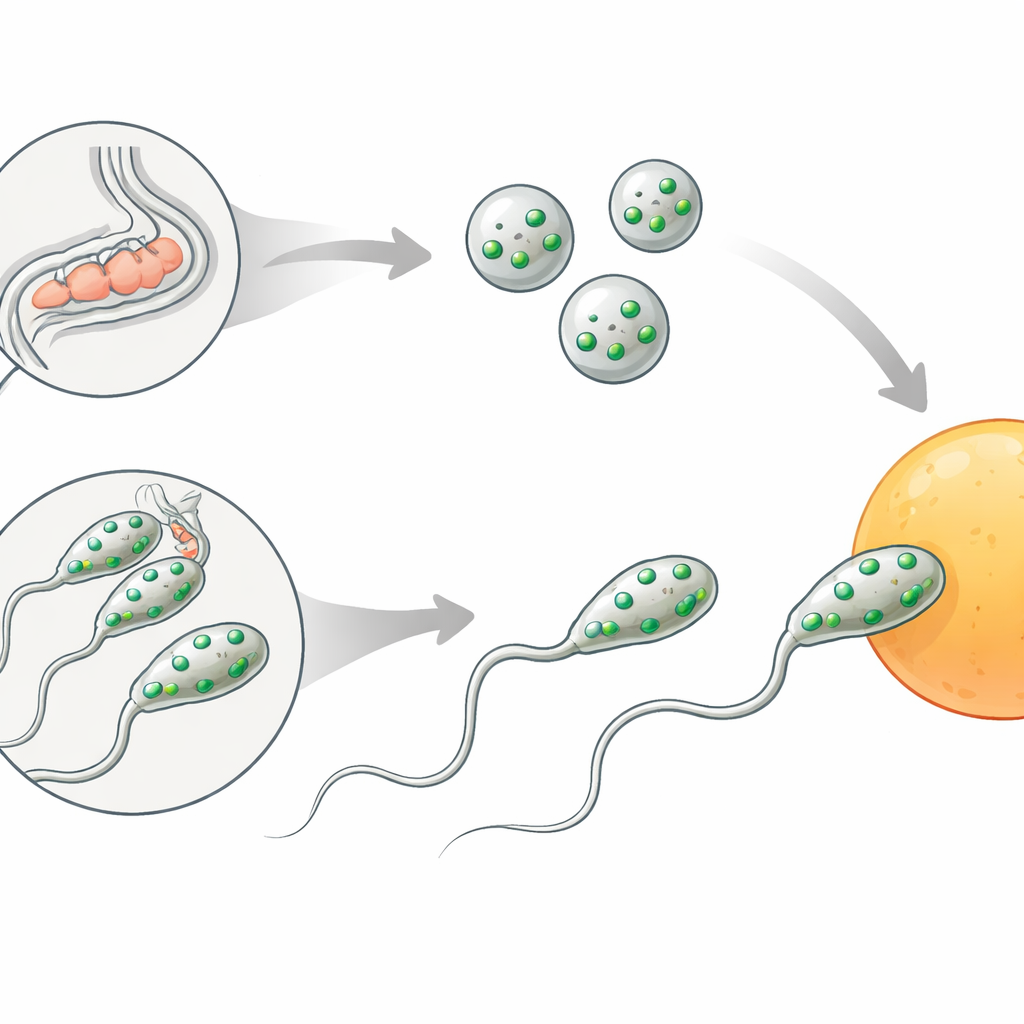
Een vruchtbaarheidsschakelaar verborgen in sperma
De auteurs richtten zich op een eerder niet-gekarakteriseerd gen, nu spe-56 genoemd. Wormen zonder spe-56 produceren normale aantallen sperma en vertonen geen duidelijke defecten in lichaamsvorm, beweging of eierproductie. Toch zijn deze dieren vrijwel volledig onvruchtbaar wanneer ze op hun eigen sperma moeten vertrouwen: ze leggen onbevruchte oöcyten die in de baarmoeder degenereren. Wanneer gemuteerde hermafrodieten worden gepaard met normale mannetjes, wordt de vruchtbaarheid hersteld, wat bewijst dat hun eieren en voortplantingskanaal werken en dat het probleem in hun eigen sperma ligt. Evenzo kunnen spe-56 mutantmannetjes paren en sperma normaal overdragen, maar hun sperma krijgen geen nageslacht, wat opnieuw wijst op een sperma-intrinsiek defect.
Wanneer de fusie stap faalt
Nadere beschouwing toonde aan dat spe-56 mutant-sperma vastlopen tijdens activatie. Onder de microscoop ziet hun ronde uitgangsvorm er normaal uit, maar na activatie groeien ze slechts korte, stompige pseudopodia en bewegen ze slecht. Met een fluorescent kleurstof die membraanfusieplaatsen markeert, zagen de onderzoekers heldere plekken langs het oppervlak van normaal sperma, die aangeven waar interne organellen met het buitenmembraan waren gefuseerd. Daarentegen toonden spe-56 mutant-spermacellen een glad, uniform signaal zonder fusiepuncten, wat onthult dat de cruciale fusiestap mislukte. Genetische tests plaatsten spe-56 stroomafwaarts van bekende regulatoren van sperma-activatie, wat betekent dat het activatiesignaal nog aankomt maar zonder SPE-56 niet kan worden omgezet in de volledige structurele verandering.
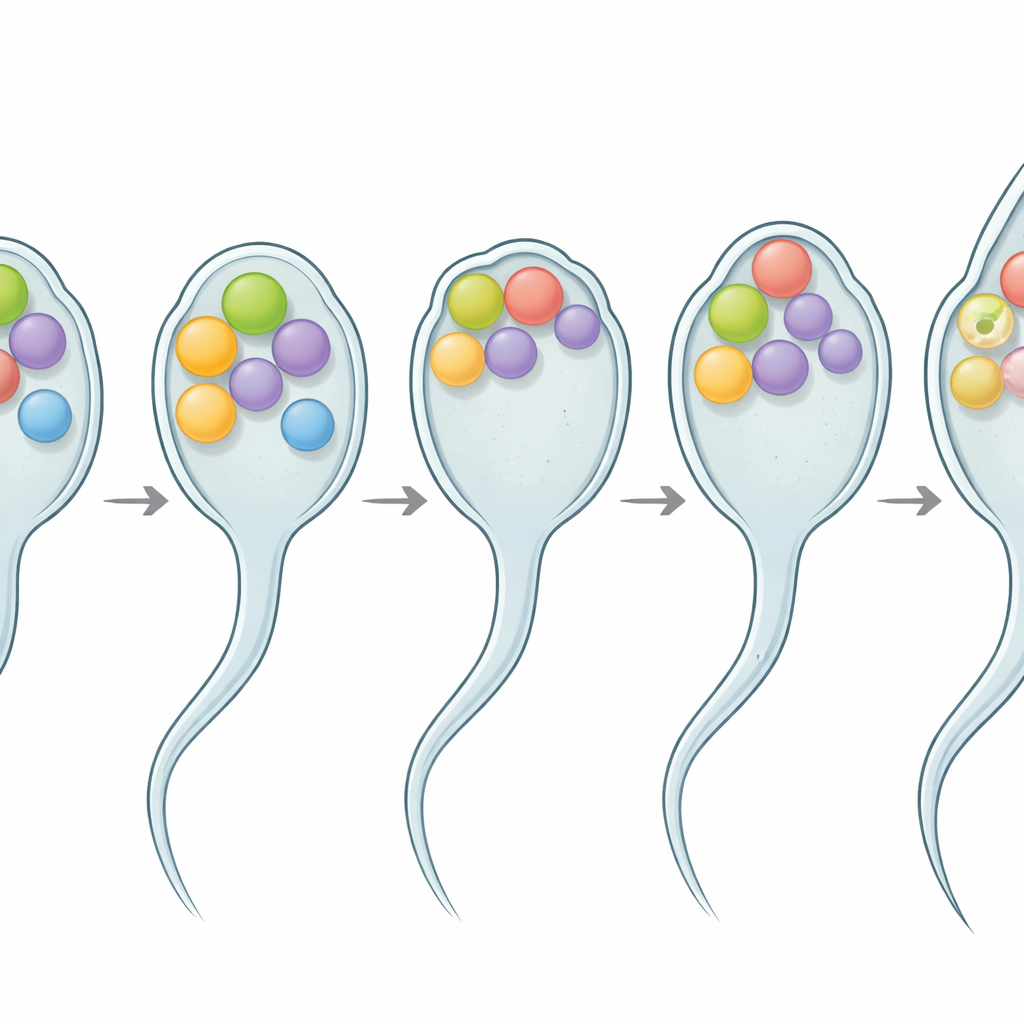
Een flexibel eiwit op het fusieoppervlak
Biochemisch en beeldvormend werk toonde dat SPE-56 een enkelvoudig door het membraan gaand eiwit is dat zich voornamelijk op de membranen van die interne organellen in sperma bevindt. Het staartgedeelte, dat in het celinterieur uitsteekt, mist een vaste vorm en gedraagt zich in plaats daarvan als een “intrinsiek gedesorganiseerd” segment—een slappe, flexibele keten in plaats van een starre scaffold. Dergelijke gedesorganiseerde regio’s worden steeds meer erkend als krachtige hulpmiddelen die cellen gebruiken om membranen te buigen, te herschikken en te fuseren. Hier ondermijnde het verwijderen van delen van deze flexibele staart geleidelijk de vruchtbaarheid, vooral bij hogere temperaturen, zonder te veranderen hoeveel sperma werd geproduceerd. Hoe meer van de staart werd verwijderd, hoe ernstiger het vruchtbaarheidsverlies, wat suggereert dat lengte en flexibiliteit helpen om sperma functioneel te houden bij temperatuurfluctuaties.
Hoe structurele soepelheid het leven kan ondersteunen
Al met al onthult de studie SPE-56 als een sleutelspeler in de laatste fase van sperma-activatie in C. elegans. Zonder dit eiwit voltooien spermacellen zelden de membraanfusiestap of vormen ze een goed functionerende kruipende pseudopod, en bevruchting vindt bijna nooit plaats. De bevindingen ondersteunen een breder idee: flexibele, gedesorganiseerde eiwitreeksen kunnen fungeren als aanpasbare "moleculaire schokdempers" die membranen helpen samenkomen, net genoeg destabiliseren om te fuseren en toch integriteit behouden. Door te laten zien hoe zo’n eiwit de spermafunctie over verschillende temperaturen in een eenvoudige worm bewaart, wijst dit werk op een mogelijk geconserveerde, evolutionair oude strategie die kan helpen dat sperma—en andere celtypen—betrouwbaar blijven in een veranderende wereld.
Bronvermelding: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Trefwoorden: sperma-activatie, membraanfusie, intrinsiek gedesorganiseerde eiwitten, Caenorhabditis elegans, vruchtbaarheid