Clear Sky Science · pt
A proteína intrinsecamente desordenada SPE-56 é necessária para exocitose tipo acrosomal e fertilidade em Caenorhabditis elegans
Por que vermes minúsculos podem nos ensinar sobre fertilidade
A fertilidade depende de um momento dramático em que um espermatozoide passa de uma forma silenciosa e de armazenamento para uma máquina ativa capaz de fundir-se ao ovo. Este estudo usa o nematoide microscópico Caenorhabditis elegans para revelar como uma proteína espermática pouco conhecida, SPE-56, ajuda a conduzir essa transição. Como muitos dos passos básicos da ativação espermática e da fusão de membranas são compartilhados entre os animais, entender essa proteína em vermes pode lançar luz sobre por que espermatozoides falham em outras espécies, incluindo humanos.
De célula reprodutiva silenciosa a nadadora ativa
Em ambos os sexos do verme, os espermatozoides começam como células arredondadas e simples chamadas espermátides. Para se tornarem capazes de fertilizar, elas passam por uma transformação conhecida como espermiogênese. Duas alterações são cruciais: sacos internos chamados organelas membranosas fundem-se com a superfície externa do espermatozoide, e um “pé” flexível chamado pseudópode cresce, permitindo que a célula rasteje em direção ao ovo. Esses passos lembram a reação acrossômica em espermatozoides humanos e de outros mamíferos, quando um compartimento especial despeja seu conteúdo e a superfície do espermatozoide é remodelada pouco antes da fertilização.
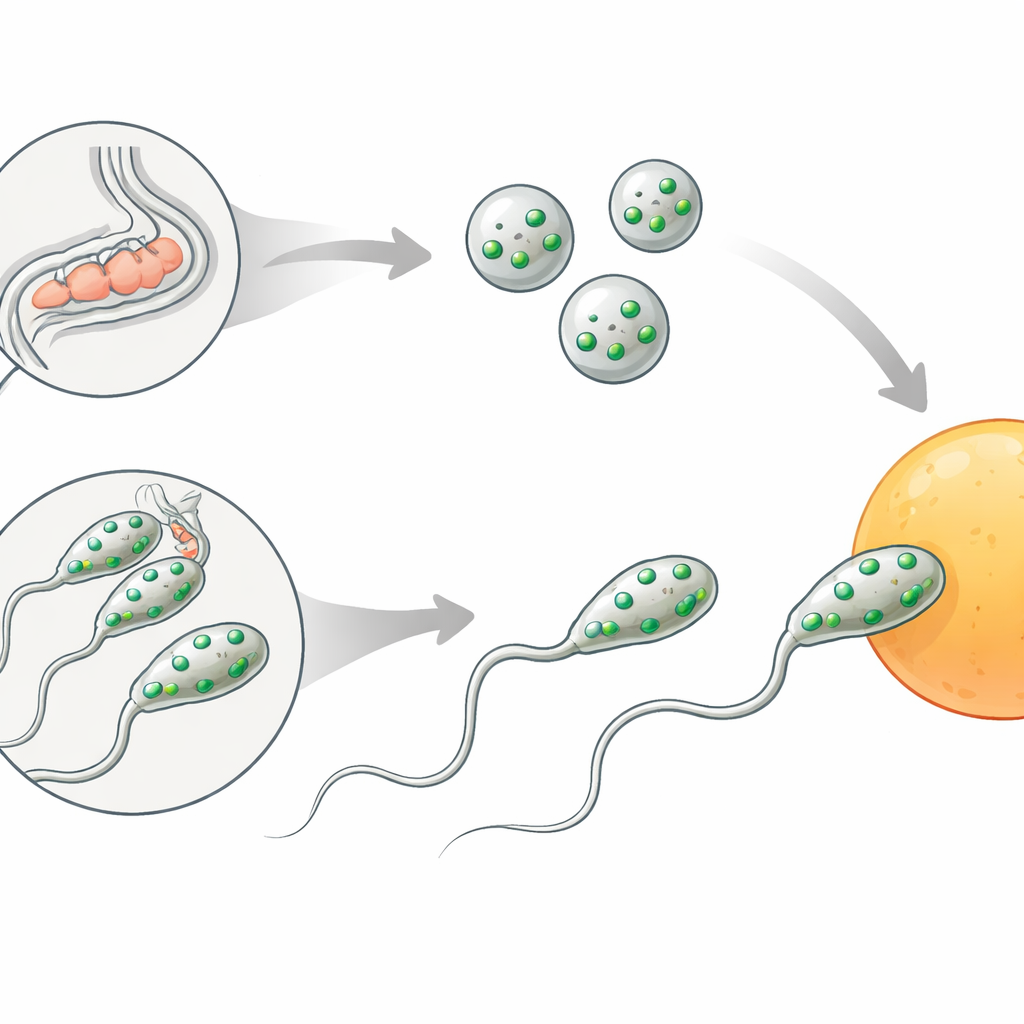
Um interruptor de fertilidade escondido no esperma
Os autores se concentraram em um gene anteriormente não caracterizado, agora chamado spe-56. Vermes sem spe-56 produzem números normais de espermatozoides e não mostram defeitos óbvios na forma do corpo, movimento ou produção de óvulos. Ainda assim, esses animais são quase completamente estéreis quando dependem de seus próprios espermatozoides: eles põem oócitos não fertilizados que degeneram no útero. Quando hermafroditas mutantes são acasaladas com machos normais, a fertilidade é restaurada, provando que seus óvulos e trato reprodutor funcionam bem e que o problema reside nos próprios espermatozoides. Da mesma forma, machos mutantes spe-56 podem acasalar e transferir esperma normalmente, mas seus espermatozoides não geram descendentes, apontando novamente para um defeito intrínseco ao esperma.
Quando a etapa de fusão falha
Exames mais detalhados mostraram que os espermatozoides mutantes spe-56 emperram durante a ativação. Ao microscópio, sua forma arredondada inicial parece normal, mas após a ativação eles crescem apenas pseudópodes curtos e toscos e se movem mal. Usando um corante fluorescente que destaca sítios de fusão de membranas, os pesquisadores observaram pontos brilhantes ao longo da superfície dos espermatozoides normais, marcando onde as organelas internas haviam se fundido com a membrana externa. Em contraste, os espermatozoides mutantes spe-56 mostraram um sinal suave e uniforme sem pontuações de fusão, revelando que a etapa crucial de fusão falhou. Testes genéticos posicionaram spe-56 a montante dos reguladores conhecidos de ativação espermática, o que significa que o sinal de ativação ainda chega, mas não pode ser traduzido em mudança estrutural completa sem a SPE-56.
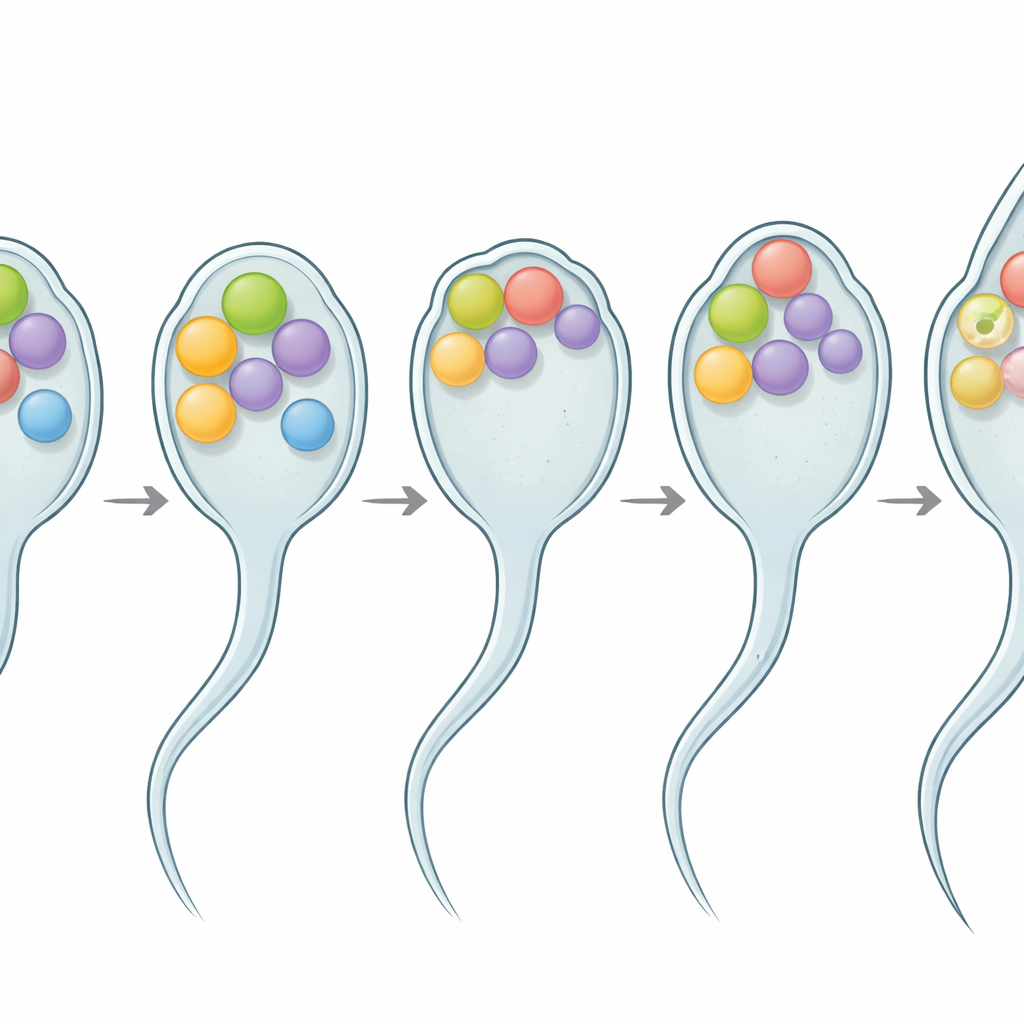
Uma proteína flexível na interface de fusão
Trabalhos bioquímicos e de imagem mostraram que a SPE-56 é uma proteína de membrana de passagem única que se localiza principalmente nas membranas dessas organelas internas nos espermatozoides. Sua região carboxi-terminal, que se estende para o interior da célula, não apresenta uma forma rígida e comporta-se como um segmento “intrinsecamente desordenado” — uma cadeia mole e flexível em vez de um andaime fixo. Tais regiões desordenadas são cada vez mais reconhecidas como ferramentas poderosas que as células usam para curvar, remodelar e fundir membranas. Aqui, a deleção de partes dessa cauda flexível gradualmente comprometeu a fertilidade, especialmente em temperaturas mais altas, sem alterar a quantidade de espermatozoides produzidos. Quanto maior a porção removida da cauda, mais severa a perda de fertilidade, sugerindo que seu comprimento e flexibilidade ajudam os espermatozoides a manterem a funcionalidade diante de flutuações de temperatura.
Como a frouxidão estrutural pode sustentar a vida
No conjunto, o estudo revela a SPE-56 como um agente-chave na etapa final da ativação espermática em C. elegans. Sem ela, os espermatozoides raramente completam a etapa de fusão de membranas ou formam um pseudópode de locomoção adequado, e a fertilização quase nunca ocorre. As descobertas sustentam uma ideia mais ampla: regiões proteicas flexíveis e desordenadas podem atuar como “amortecedores moleculares” adaptáveis que ajudam as membranas a se aproximarem, a desestabilizarem o suficiente para fundir-se e ainda manterem a integridade. Ao mostrar como tal proteína preserva a função espermática em diferentes temperaturas em um verme simples, este trabalho aponta para uma estratégia possivelmente conservada e evolutivamente antiga que pode ajudar espermatozoides — e outros tipos celulares — a permanecerem confiáveis em um mundo em mudança.
Citação: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Palavras-chave: ativação do espermatozoide, fusão de membranas, proteínas intrinsecamente desordenadas, Caenorhabditis elegans, fertilidade