Clear Sky Science · pl
Białko wewnętrznie nieuporządkowane SPE-56 jest wymagane do egzocytozy przypominającej akrosomę i płodności u Caenorhabditis elegans
Dlaczego maleńkie nicienie mogą uczyć nas o płodności
Płodność zależy od dramatycznego momentu, gdy plemnik przełącza się z cichej formy magazynowej w aktywną maszynę łączącą się z jajem. W tym badaniu wykorzystano mikroskopijnego nicienia Caenorhabditis elegans, aby ujawnić, jak mało znane białko plemnikowe SPE-56 pomaga napędzać tę przemianę. Ponieważ wiele podstawowych kroków aktywacji plemników i fuzji błon jest zachowanych u różnych zwierząt, zrozumienie funkcji tego białka u robaków może rzucić światło na przyczyny niepowodzeń plemników u innych gatunków, w tym u ludzi.
Od cichej komórki rozrodczej do aktywnego pływaka
U obu płci nicieni plemniki zaczynają jako proste okrągłe komórki zwane spermatydami. Aby stać się zdolnymi do zapłodnienia, muszą przejść przemianę zwaną spermiogenezą. Kluczowe są dwa zmiany: wewnętrzne pęcherzyki zwane organellami błoniastymi łączą się z zewnętrzną powierzchnią plemnika, a giętka „stopa” zwana pseudopodem wyrasta, pozwalając komórce pełzać w stronę jaja. Kroki te przypominają reakcję akrosomalną u człowieka i innych ssaków, gdy specjalna przestrzeń opróżnia swą zawartość, a powierzchnia plemnika zostaje przeistoczona tuż przed zapłodnieniem.
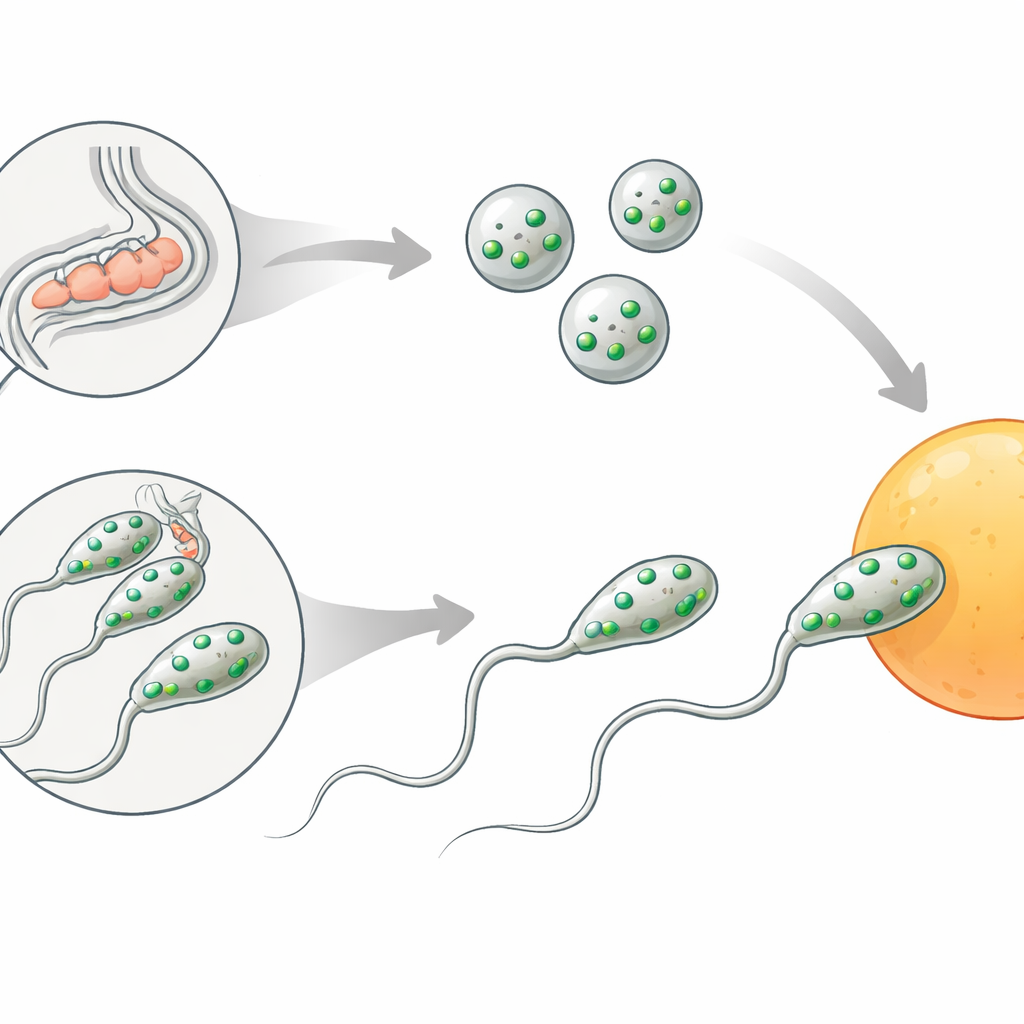
Przełącznik płodności ukryty w plemnikach
Autorzy skupili się na dotąd nieopisanym genie, nazwanym teraz spe-56. Robaki pozbawione spe-56 wytwarzają normalne liczby plemników i nie wykazują widocznych defektów w kształcie ciała, ruchu czy produkcji jaj. Mimo to zwierzęta te są niemal całkowicie bezpłodne, gdy polegają na własnych plemnikach: składają niezapłodnione oocyty, które degenerują w macicy. Gdy mutantyczne hermafrodyty są kryte przez normalnych samców, płodność wraca, co dowodzi, że ich jaja i drogi rozrodcze działają poprawnie, a problem leży w ich własnych plemnikach. Podobnie, samce spe-56 mogą kopulować i normalnie przekazywać plemniki, ale ich plemniki nie wydają potomstwa, co ponownie wskazuje na defekt wewnątrz plemnika.
Gdy etap fuzji zawodzi
Bardziej wnikliwa analiza wykazała, że plemniki mutantów spe-56 zatrzymują się podczas aktywacji. Pod mikroskopem ich początkowa, okrągła postać wygląda normalnie, ale po aktywacji rozwijają jedynie krótkie, tępe pseudopody i poruszają się słabo. Przy użyciu barwnika fluorescencyjnego uwidaczniającego miejsca fuzji błon, badacze obserwowali jasne punkty na powierzchni normalnych plemników, oznaczające miejsca, gdzie organelle wewnętrzne scaliły się z zewnętrzną błoną. W przeciwieństwie do tego plemniki mutantów spe-56 wykazywały gładki, jednorodny sygnał bez punktów fuzji, ujawniając, że kluczowy etap łączenia się błon zawiódł. Testy genetyczne umieściły spe-56 poniżej znanych regulatorów aktywacji plemników, co oznacza, że sygnał aktywacyjny dociera, ale bez SPE-56 nie może zostać przekształcony w pełną zmianę strukturalną.
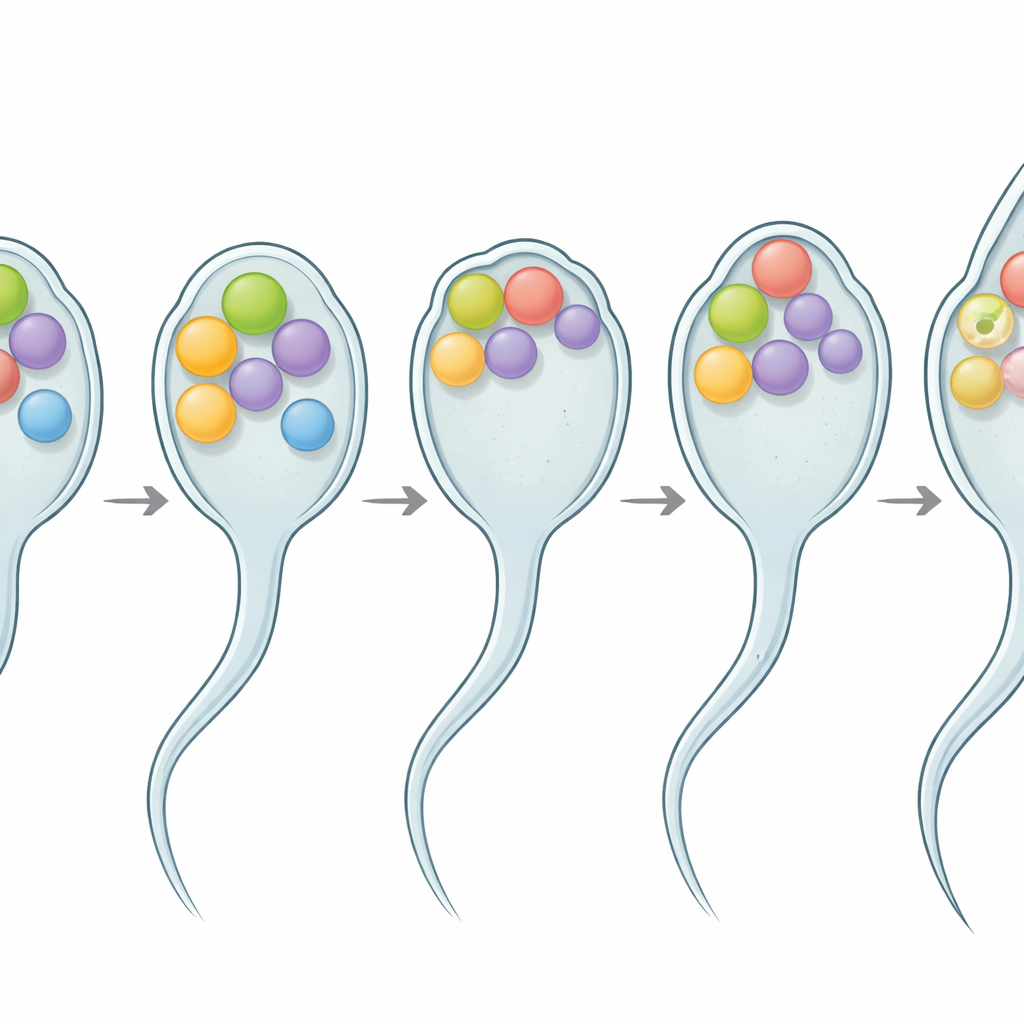
Elastyczne białko na granicy fuzji
Badania biochemiczne i obrazowanie wykazały, że SPE-56 jest białkiem przechodzącym przez błonę z jedną pętlą, które lokalizuje się głównie na błonach tych wewnętrznych organelli w plemnikach. Jego ogon, wystający do wnętrza komórki, nie ma sztywnej struktury, lecz zachowuje się jak segment „wewnętrznie nieuporządkowany” — wiotki, elastyczny łańcuch zamiast stałego rusztowania. Takie nieuporządkowane regiony są coraz częściej rozpoznawane jako potężne narzędzia, które komórki wykorzystują do wyginania, przebudowy i łączenia błon. Tutaj usuwanie części tego elastycznego ogona stopniowo osłabiało płodność, zwłaszcza w wyższych temperaturach, bez zmiany liczby produkowanych plemników. Im więcej usunięto ogona, tym poważniejsza była utrata płodności, co sugeruje, że jego długość i elastyczność pomagają plemnikom zachować funkcję przy wahaniach temperatury.
Jak strukturalna luźność może wspierać życie
Podsumowując, badanie ujawnia SPE-56 jako kluczowego wykonawcę na końcowym etapie aktywacji plemników u C. elegans. Bez niego plemniki rzadko kończą etap fuzji błon ani nie tworzą właściwego pseudopodu pełzającego, a zapłodnienie prawie nigdy nie zachodzi. Wyniki wspierają szerszą ideę: elastyczne, nieuporządkowane regiony białek mogą działać jako adaptowalne „molekularne amortyzatory”, pomagające błonom zbliżyć się, destabilizować na tyle, by złączyć się, a jednocześnie zachować integralność. Pokazując, jak takie białko zachowuje funkcję plemników w różnych temperaturach u prostego robaka, praca ta wskazuje na potencjalnie zachowaną, ewolucyjnie dawną strategię, która może pomagać plemnikom — i innym typom komórek — pozostać niezawodnymi w zmieniającym się świecie.
Cytowanie: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Słowa kluczowe: aktywacja plemników, fuzja błon, białka wewnętrznie nieuporządkowane, Caenorhabditis elegans, płodność