Clear Sky Science · fr
La protéine intrinsèquement désordonnée SPE-56 est nécessaire à l’exocytose de type acrosomale et à la fertilité chez Caenorhabditis elegans
Pourquoi de minuscules vers peuvent nous instruire sur la fertilité
La fertilité dépend d’un moment dramatique où un spermatozoïde passe d’une forme silencieuse et stockée à une machine active capable de fusionner avec l’ovule. Cette étude utilise le nématode microscopique Caenorhabditis elegans pour révéler comment une protéine spermatique peu connue, SPE-56, aide à déclencher cette transition. Parce que de nombreuses étapes fondamentales de l’activation des spermatozoïdes et de la fusion membranaire sont communes à de nombreux animaux, comprendre cette protéine chez le ver peut éclairer les raisons d’échecs spermiques dans d’autres espèces, y compris les humains.
De la cellule-dormance au nageur actif
Chez les deux sexes du ver, les spermatozoïdes débutent comme de simples cellules rondes appelées spermatides. Pour devenir capables de féconder, elles doivent subir une transformation appelée spermiogenèse. Deux changements sont cruciaux : des sacs internes appelés organites membranaires fusionnent avec la surface externe du spermatozoïde, et un « pied » flexible nommé pseudopode se déploie, permettant à la cellule de ramper vers l’œuf. Ces étapes ressemblent à la réaction acrosomale chez les spermatozoïdes humains et d’autres mammifères, où un compartiment spécialisé vide son contenu et la surface du spermatozoïde est remodelée juste avant la fécondation.
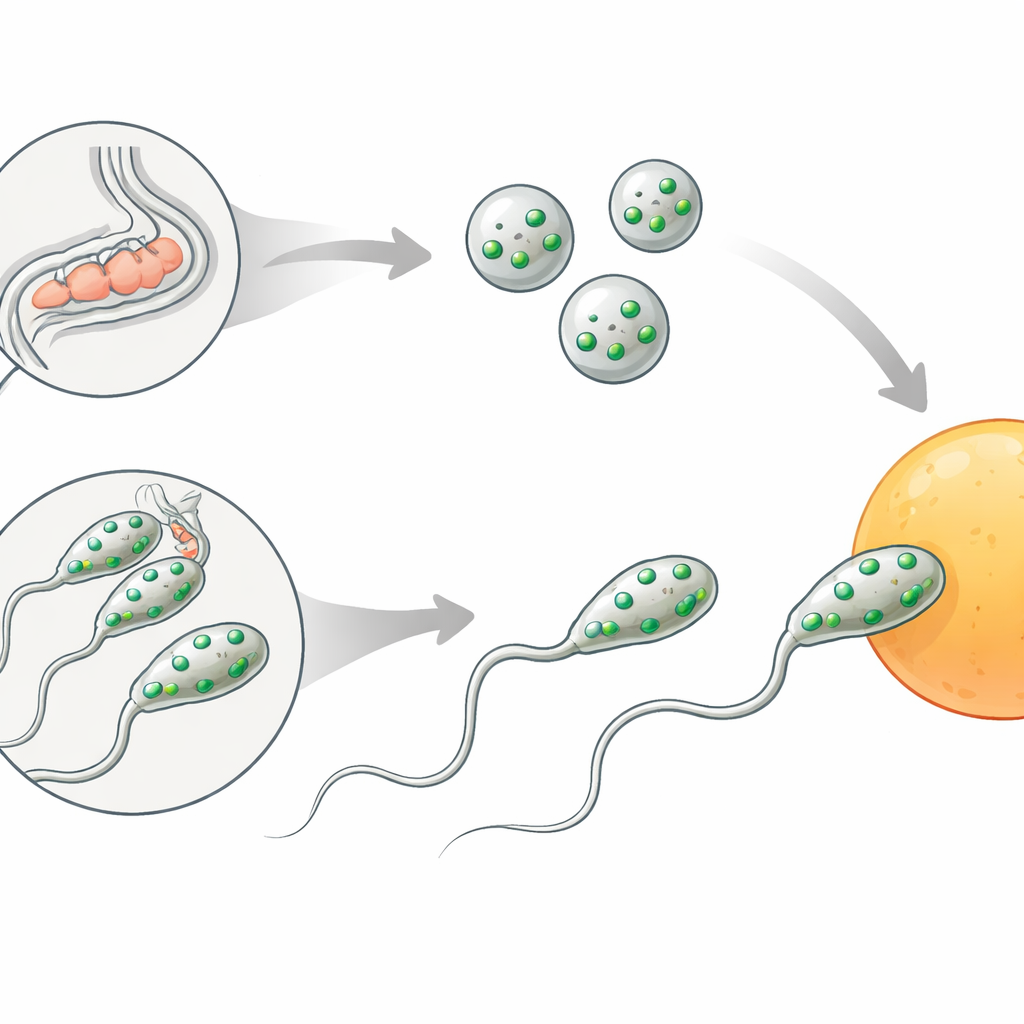
Un interrupteur de fertilité caché dans le spermatozoïde
Les auteurs se sont concentrés sur un gène auparavant non caractérisé, désormais nommé spe-56. Les vers dépourvus de spe-56 produisent un nombre normal de spermatozoïdes et ne présentent pas de défauts évidents de morphologie, de mobilité ou de production d’ovules. Pourtant, ces animaux sont presque totalement stériles lorsqu’ils dépendent de leurs propres spermatozoïdes : ils pondent des ovocytes non fécondés qui dégénèrent dans l’utérus. Lorsque des hermaphrodites mutants sont accouplés avec des mâles normaux, la fertilité est rétablie, ce qui prouve que leurs ovules et leur tractus reproducteur fonctionnent correctement et que le problème vient de leurs propres spermatozoïdes. De même, les mâles mutants spe-56 peuvent s’accoupler et transférer des spermatozoïdes normalement, mais leurs spermatozoïdes ne donnent pas naissance à une progéniture, ce qui indique encore un défaut intrinsèque aux spermatozoïdes.
Quand l’étape de fusion échoue
Un examen plus poussé a montré que les spermatozoïdes mutants spe-56 bloquent leur activation. Au microscope, leur forme ronde initiale semble normale, mais après activation ils ne développent que des pseudopodes courts et trapus et se déplacent mal. En utilisant un colorant fluorescent qui met en évidence les sites de fusion membranaire, les chercheurs ont observé des points lumineux le long de la surface des spermatozoïdes normaux, marquant les sites où les organites internes avaient fusionné avec la membrane externe. En revanche, les spermatozoïdes mutants spe-56 montraient un signal uniforme et lisse sans poncta de fusion, révélant que l’étape cruciale de fusion avait échoué. Des tests génétiques ont placé spe-56 en aval des régulateurs connus de l’activation des spermatozoïdes, ce qui signifie que le signal d’activation parvient toujours mais ne peut pas être traduit en changement structural complet sans SPE-56.
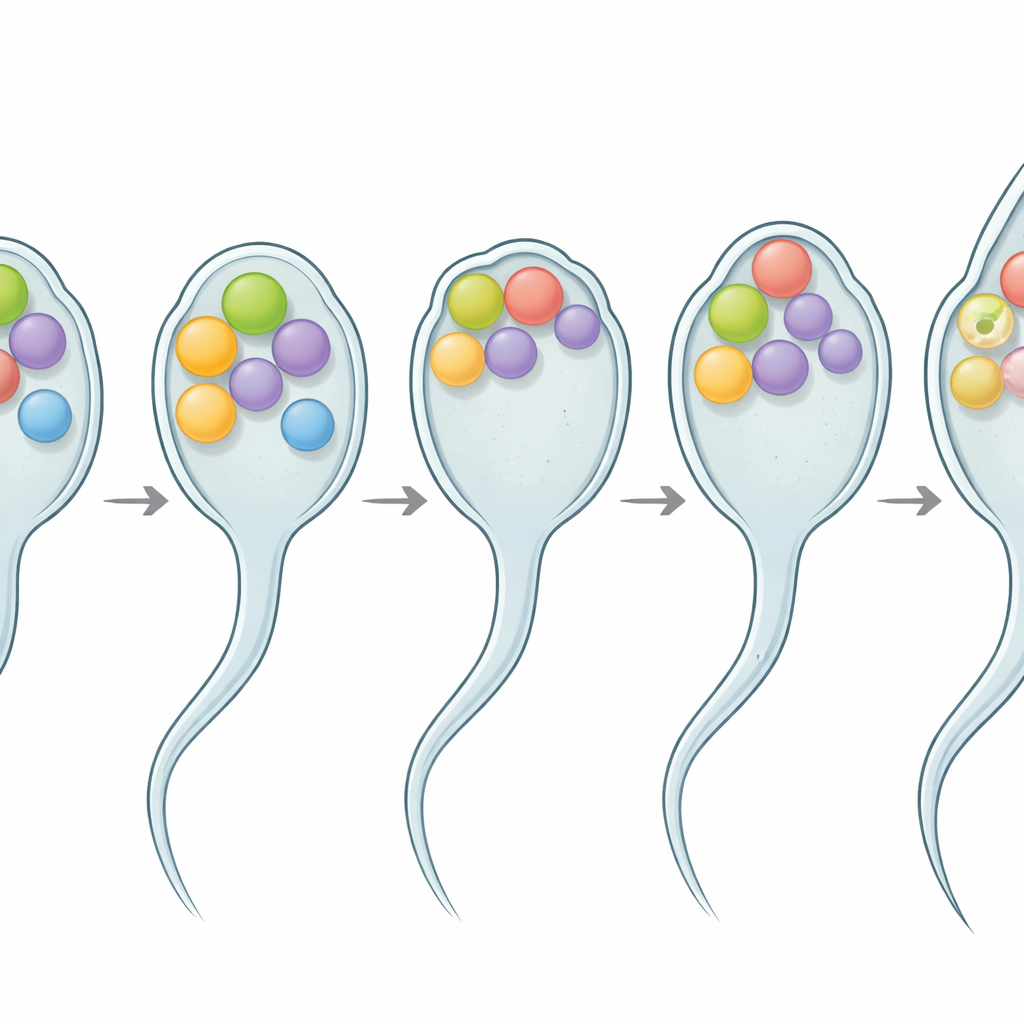
Une protéine flexible à l’interface de fusion
Des travaux biochimiques et d’imagerie ont montré que SPE-56 est une protéine transmembranaire à passage unique qui se localise principalement aux membranes de ces organites internes dans les spermatozoïdes. Sa région en queue, qui s’étend vers l’intérieur de la cellule, n’a pas de forme rigide et se comporte plutôt comme un segment « intrinsèquement désordonné » : une chaîne souple et flexible plutôt qu’un échafaudage fixe. De telles régions désordonnées sont de plus en plus reconnues comme des outils puissants que les cellules utilisent pour courber, remodeler et fusionner les membranes. Ici, la suppression de parties de cette queue flexible a progressivement affaibli la fertilité, en particulier à des températures plus élevées, sans modifier le nombre de spermatozoïdes produits. Plus la queue était raccourcie, plus la perte de fertilité était sévère, suggérant que sa longueur et sa flexibilité aident les spermatozoïdes à rester fonctionnels malgré les fluctuations de température.
Comment la souplesse structurelle peut soutenir la vie
Dans l’ensemble, l’étude révèle SPE-56 comme un acteur clé à l’étape finale de l’activation des spermatozoïdes chez C. elegans. Sans elle, les spermatozoïdes complètent rarement l’étape de fusion membranaire ni ne forment un pseudopode de déplacement adéquat, et la fécondation n’a presque jamais lieu. Les résultats soutiennent une idée plus large : les régions protéiques flexibles et désordonnées peuvent agir comme des « amortisseurs moléculaires » adaptables qui aident les membranes à se rapprocher, à se destabiliser juste ce qu’il faut pour fusionner, tout en maintenant l’intégrité. En montrant comment une telle protéine préserve la fonction spermatique à travers des variations de température chez un ver simple, ce travail pointe vers une stratégie potentiellement conservée et évolutivement ancienne qui peut aider les spermatozoïdes — et d’autres types cellulaires — à rester fiables dans un monde changeant.
Citation: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Mots-clés: activation des spermatozoïdes, fusion membranaire, protéines intrinsèquement désordonnées, Caenorhabditis elegans, fertilité