Clear Sky Science · it
La proteina intrinsecamente disordinata SPE-56 è necessaria per l’esocitosi di tipo acrosomiale e la fertilità in Caenorhabditis elegans
Perché i vermi minuscoli ci insegnano sulla fertilità
La fertilità dipende da un momento drammatico in cui una cellula spermatozoide passa da una forma silente e di deposito a una macchina attiva capace di fondersi con l’uovo. Questo studio utilizza il vermicello microscopico Caenorhabditis elegans per rivelare come una proteina spermática poco nota, SPE-56, contribuisca a guidare questa transizione. Poiché molti dei passaggi fondamentali dell’attivazione degli spermatozoi e della fusione di membrane sono condivisi tra gli animali, comprendere questa proteina nei vermi può fare luce sui motivi per cui gli spermatozoi falliscono in altre specie, compresa l’uomo.
Da cellula seme tranquilla a nuotatore attivo
In entrambi i sessi del verme, gli spermatozoi iniziano come semplici cellule tonde chiamate spermatidi. Per diventare capaci di fecondare, queste devono subire un restyling noto come spermiogenesi. Due cambiamenti sono cruciali: sacche interne chiamate organelli membranosi si fondono con la superficie esterna dello spermatozoo, e una “piede” flessibile chiamata pseudopodio si estende, permettendo alla cellula di strisciare verso l’uovo. Questi passaggi assomigliano alla reazione acrosomiale negli spermatozoi umani e di altri mammiferi, in cui un compartimento speciale svuota il suo contenuto e la superficie dello spermatozoo viene rimodellata poco prima della fertilizzazione.
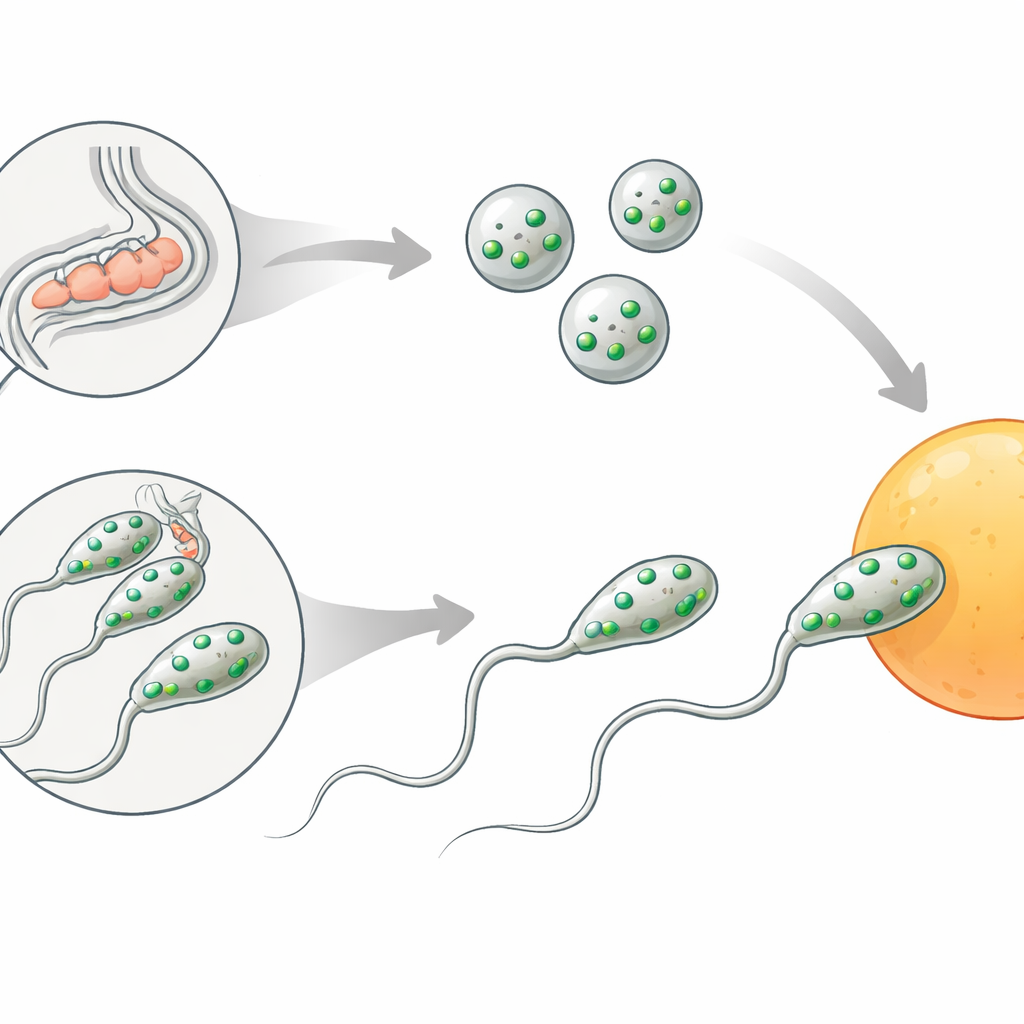
Un interruttore di fertilità nascosto negli spermatozoi
Gli autori si sono concentrati su un gene precedentemente non caratterizzato, ora chiamato spe-56. I vermi privi di spe-56 producono un numero normale di spermatozoi e non mostrano difetti evidenti nella forma del corpo, nel movimento o nella produzione di uova. Eppure questi animali sono quasi completamente sterili quando si affidano ai loro spermatozoi: depongono oociti non fecondati che degenerano nell’utero. Quando gli ermafroditi mutanti vengono accoppiati con maschi normali, la fertilità è ripristinata, dimostrando che le loro uova e il tratto riproduttivo funzionano correttamente e che il problema risiede negli spermatozoi stessi. Allo stesso modo, i maschi mutanti per spe-56 possono accoppiarsi e trasferire spermatozoi normalmente, ma i loro spermatozoi non generano prole, indicando ancora una volta un difetto intrinseco dello spermatozoo.
Quando il passo della fusione fallisce
Un esame più attento ha mostrato che gli spermatozoi mutanti spe-56 si bloccano durante l’attivazione. Al microscopio, la loro forma tondeggiante iniziale appare normale, ma dopo l’attivazione sviluppano solo pseudopodi corti e tozzi e si muovono male. Utilizzando un colorante fluorescente che evidenzia i siti di fusione delle membrane, i ricercatori hanno osservato punti luminosi sulla superficie degli spermatozoi normali, che segnano dove gli organelli interni si erano fusi con la membrana esterna. Al contrario, gli spermatozoi spe-56 mutanti mostravano un segnale liscio e uniforme senza puntini di fusione, rivelando che il cruciale passo di fusione era fallito. Test genetici hanno collocato spe-56 a valle dei noti regolatori dell’attivazione degli spermatozoi, il che significa che il segnale di attivazione arriva ancora ma non può essere tradotto in un cambiamento strutturale completo senza SPE-56.
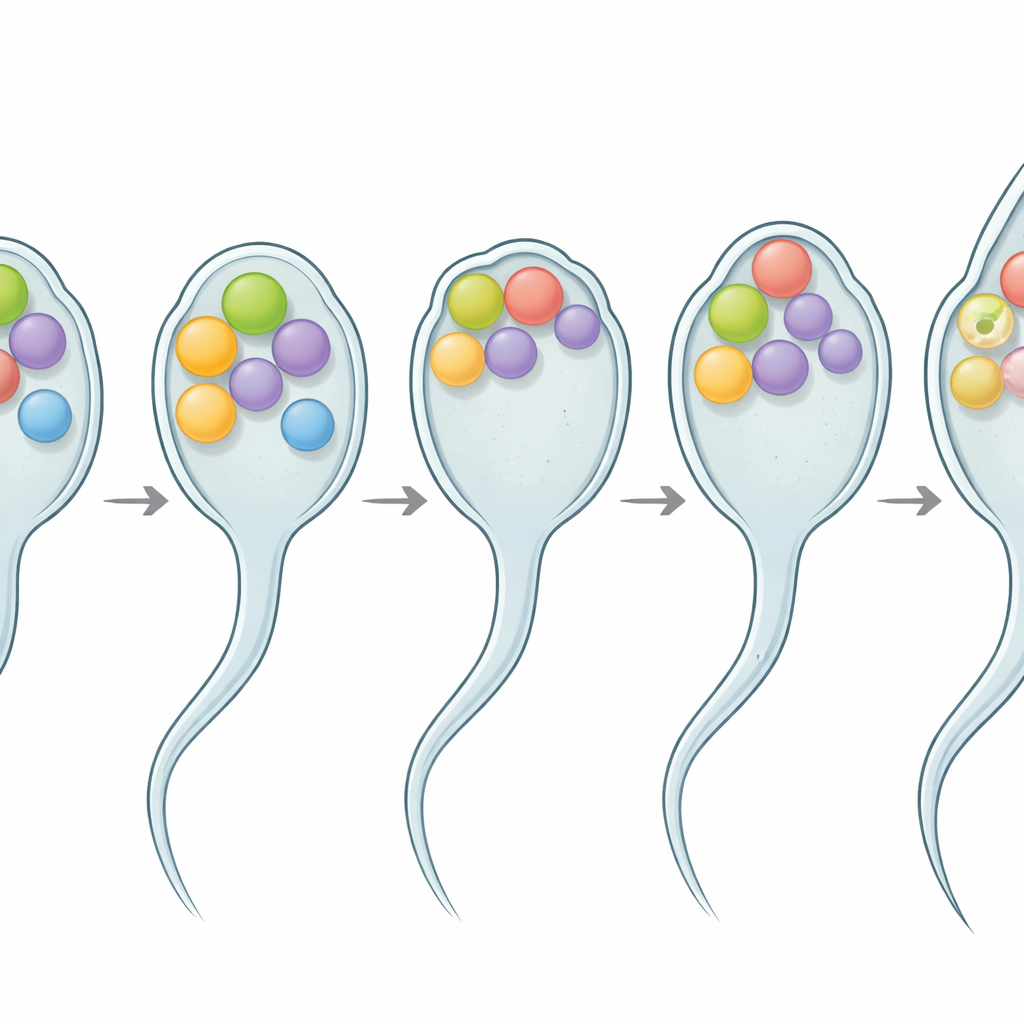
Una proteina flessibile all’interfaccia di fusione
Lavoro biochimico e imaging hanno mostrato che SPE-56 è una proteina di membrana a passaggio singolo che si trova principalmente sulle membrane di quegli organelli interni negli spermatozoi. La sua regione a coda, che si estende verso l’interno della cellula, manca di una forma rigida e si comporta invece come un segmento “intrinsecamente disordinato” — una catena floscia e flessibile piuttosto che uno scaffold fisso. Tali regioni disordinate sono sempre più riconosciute come strumenti potenti che le cellule usano per piegare, rimodellare e fondere membrane. Qui, la rimozione di parti di questa coda flessibile ha gradualmente compromesso la fertilità, soprattutto a temperature più alte, senza cambiare il numero di spermatozoi prodotti. Più porzioni della coda venivano eliminate, più grave era la perdita di fertilità, suggerendo che la sua lunghezza e flessibilità aiutano gli spermatozoi a restare funzionali attraverso variazioni di temperatura.
Come la scioltezza strutturale può sostenere la vita
Nel complesso, lo studio rivela SPE-56 come un operatore chiave nell’ultima fase dell’attivazione degli spermatozoi in C. elegans. Senza di essa, gli spermatozoi completano raramente il passo di fusione delle membrane o formano un pseudopodio adatto alla locomozione, e la fertilizzazione quasi mai avviene. I risultati supportano un’idea più ampia: le regioni proteiche flessibili e disordinate possono agire come “ammortizzatori molecolari” adattabili che aiutano le membrane ad avvicinarsi, destabilizzarsi il giusto necessario per fondersi e mantenere comunque l’integrità. Mostrando come una tale proteina preservi la funzione degli spermatozoi a diverse temperature in un verme semplice, questo lavoro indica una strategia potenzialmente conservata ed evolutivamente antica che può aiutare gli spermatozoi — e altri tipi cellulari — a rimanere affidabili in un mondo che cambia.
Citazione: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Parole chiave: attivazione degli spermatozoi, fusione di membrane, proteine intrinsecamente disordinate, Caenorhabditis elegans, fertilità