Clear Sky Science · de
Das intrinsisch ungeordnete Protein SPE-56 ist für akrosom‑ähnliche Exozytose und Fruchtbarkeit in Caenorhabditis elegans erforderlich
Warum winzige Würmer uns etwas über Fruchtbarkeit lehren können
Fruchtbarkeit hängt von einem dramatischen Moment ab, in dem eine Samenzelle von einer ruhigen, Speicherform in eine aktive, mit Eizellen verschmelzende Maschine umschaltet. Diese Studie nutzt den mikroskopischen Fadenwurm Caenorhabditis elegans, um zu zeigen, wie ein wenig bekanntes Spermienprotein, SPE‑56, diesen Übergang unterstützt. Da viele grundlegende Schritte der Spermienaktivierung und Membranfusion bei Tieren ähnlich sind, kann das Verständnis dieses Proteins bei Würmern Aufschluss darüber geben, warum Spermien auch bei anderen Arten, einschließlich des Menschen, versagen.
Vom ruhenden Keim zur aktiven Schwimmerzelle
Bei beiden Geschlechtern der Würmer beginnen Spermien als einfache, runde Zellen, sogenannte Spermatiden. Um befruchtungsfähig zu werden, müssen diese eine Umwandlung durchlaufen, die als Spermiogenese bezeichnet wird. Zwei Veränderungen sind entscheidend: Innere Bläschen, die membranösen Organellen, verschmelzen mit der Außenfläche des Spermiums, und ein flexibler „Fuß“, das Pseudopod, wächst heraus, sodass die Zelle zum Ei kriechen kann. Diese Schritte ähneln der Akrosomreaktion bei menschlichen und anderen Säugetierspermien, bei der ein spezielles Kompartiment seinen Inhalt entleert und die Oberfläche des Spermiums kurz vor der Befruchtung umgestaltet wird.
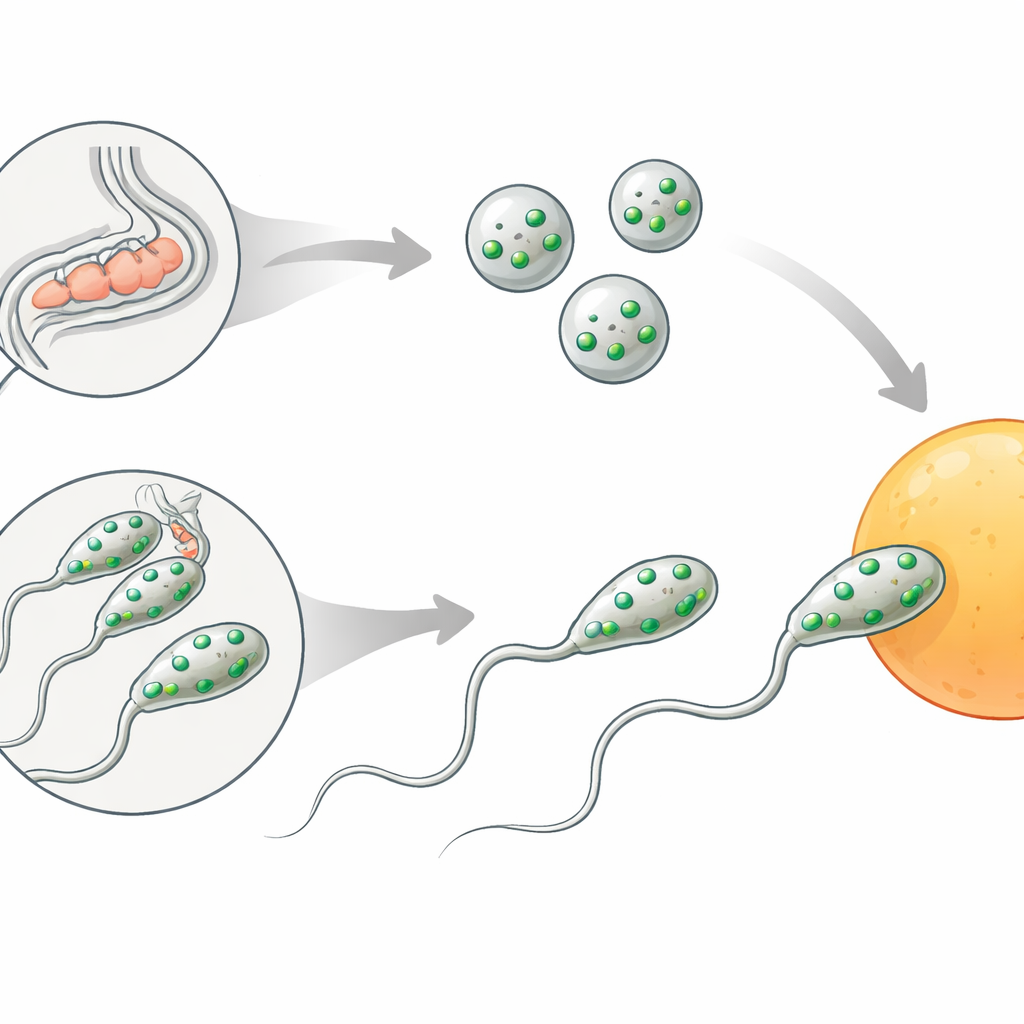
Ein Fruchtbarkeitsschalter, verborgen im Spermium
Die Autorinnen und Autoren konzentrierten sich auf ein zuvor nicht charakterisiertes Gen, das nun spe‑56 genannt wird. Würmer ohne spe‑56 produzieren normale Mengen an Spermien und zeigen keine offensichtlichen Defekte in Körperform, Bewegung oder Eiproduktion. Dennoch sind diese Tiere fast vollständig steril, wenn sie auf eigene Spermien angewiesen sind: Sie legen unbefruchtete Oozyten ab, die in der Gebärmutter degenerieren. Wenn mutante Hermaphroditen mit normalen Männchen gepaart werden, stellt sich die Fruchtbarkeit wieder her, was beweist, dass ihre Eizellen und der Fortpflanzungstrakt in Ordnung sind und das Problem in ihren eigenen Spermien liegt. Ebenso können spe‑56‑mutante Männchen paaren und Spermien normal übertragen, doch ihre Spermien zeugen keine Nachkommen, was wiederum auf einen spermienintrinsischen Defekt hindeutet.
Wenn der Fusionsschritt scheitert
Genauere Untersuchungen zeigten, dass spe‑56‑mutante Spermien während der Aktivierung steckenbleiben. Unter dem Mikroskop wirkt ihre runde Ausgangsform normal, doch nach der Aktivierung bilden sie nur kurze, stubbige Pseudopoden und bewegen sich schlecht. Mit einem fluoreszierenden Farbstoff, der Membranfusionsstellen hervorhebt, beobachteten die Forschenden helle Punkte entlang der Oberfläche normaler Spermien, die markieren, wo interne Organellen mit der Außenmembran verschmolzen waren. Im Gegensatz dazu zeigten spe‑56‑mutante Spermien ein glattes, gleichmäßiges Signal ohne solche Fusionspunkte, was enthüllte, dass der entscheidende Fusionsschritt fehlgeschlagen war. Genetische Tests ordneten spe‑56 stromabwärts bekannter Aktivierungsregulatoren ein, was bedeutet, dass das Aktivierungssignal zwar ankommt, aber ohne SPE‑56 nicht in die vollständige strukturelle Umgestaltung umgesetzt werden kann.
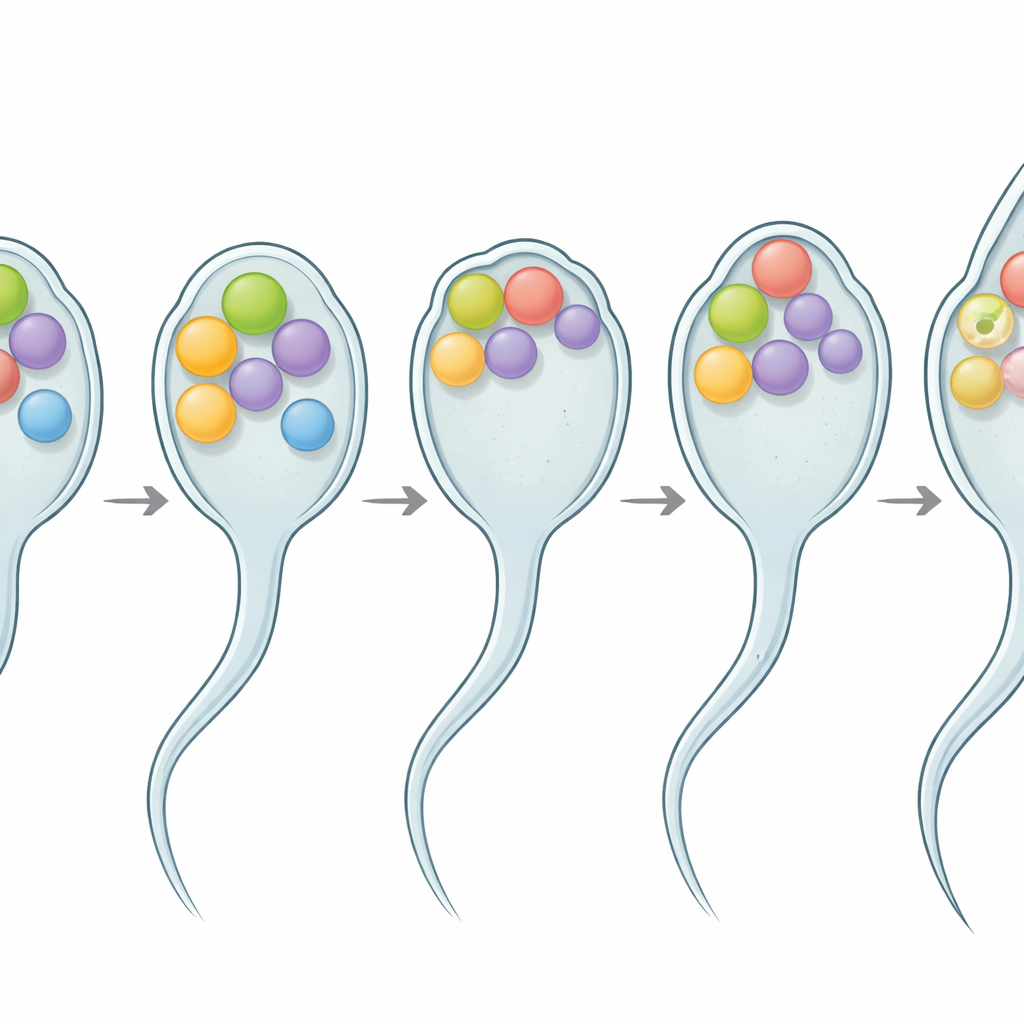
Ein flexibles Protein an der Fusionsschnittstelle
Biochemische und bildgebende Arbeiten zeigten, dass SPE‑56 ein einstufiges Membranprotein ist, das vornehmlich auf den Membranen jener internen Organellen in Spermien sitzt. Sein Schwanzbereich, der ins Zellinnere ragt, fehlt eine feste Form und verhält sich stattdessen wie ein „intrinsisch ungeordneter“ Abschnitt — eine schlaffe, flexible Kette statt eines starren Gerüsts. Solche ungeordneten Regionen werden zunehmend als kraftvolle Werkzeuge erkannt, die Zellen nutzen, um Membranen zu biegen, umzubauen und zu fusionieren. Hier untergrub das Entfernen von Teilen dieses flexiblen Schwanzes schrittweise die Fruchtbarkeit, insbesondere bei höheren Temperaturen, ohne die Spermienzahl zu verändern. Je mehr vom Schwanz entfernt wurde, desto ausgeprägter war der Fruchtbarkeitsverlust, was darauf hindeutet, dass Länge und Flexibilität helfen, die Funktion der Spermien bei Temperaturschwankungen zu erhalten.
Wie strukturelle Lockerheit Leben stützen kann
Insgesamt zeigt die Studie SPE‑56 als einen Schlüsselakteur in der letzten Phase der Spermienaktivierung in C. elegans. Ohne dieses Protein schließen Spermien den Membranfusionsschritt kaum ab oder bilden kein richtiges kriechendes Pseudopod, und eine Befruchtung findet fast nie statt. Die Ergebnisse stützen eine weiter gefasste Idee: Flexible, ungeordnete Proteinregionen können als anpassungsfähige „molekulare Stoßdämpfer“ wirken, die Membranen zusammenbringen, sie gerade ausreichend destabilisieren, damit sie verschmelzen, und dabei dennoch die Integrität bewahren. Indem gezeigt wird, wie ein solches Protein die Funktion von Spermien bei unterschiedlichen Temperaturen in einem einfachen Wurm erhält, deutet diese Arbeit auf eine potenziell konservierte, evolutionär alte Strategie hin, die Spermien — und andere Zelltypen — in einer sich wandelnden Welt zuverlässig bleiben lässt.
Zitation: Gottschling, DC., Eiser, S. & Döring, F. The intrinsically disordered protein SPE-56 is required for acrosomal-like exocytosis and fertility in Caenorhabditis elegans. Sci Rep 16, 12062 (2026). https://doi.org/10.1038/s41598-026-47896-7
Schlüsselwörter: Spermaaktivierung, Membranfusion, intrinsisch ungeordnete Proteine, Caenorhabditis elegans, Fruchtbarkeit