Clear Sky Science · sv
Partikellösningshastighet styr makrofagrespons och läkemedelsfrisättning från mesoporösa kiselförande inhalationsbärare
Varför små lungbärare spelar roll
Att andas in medicin direkt till lungorna är ett lockande sätt att behandla sjukdomar som tuberkulos samtidigt som många systemiska biverkningar undviks. Denna studie undersöker en ny klass av små porösa kiselpartiklar utformade att fungera som "dubbelskala"-bärare: de når lungorna som mikroskopiska korn men löser sedan upp sig till mycket mindre nanopartiklar i lungvätska. Forskarna ställde två praktiska frågor: hur säkra är dessa partiklar för viktiga immunceller i lungorna, och hur styr upplösningshastigheten både cellernas respons och hur ett tuberkulosläkemedel frisätts över tid?
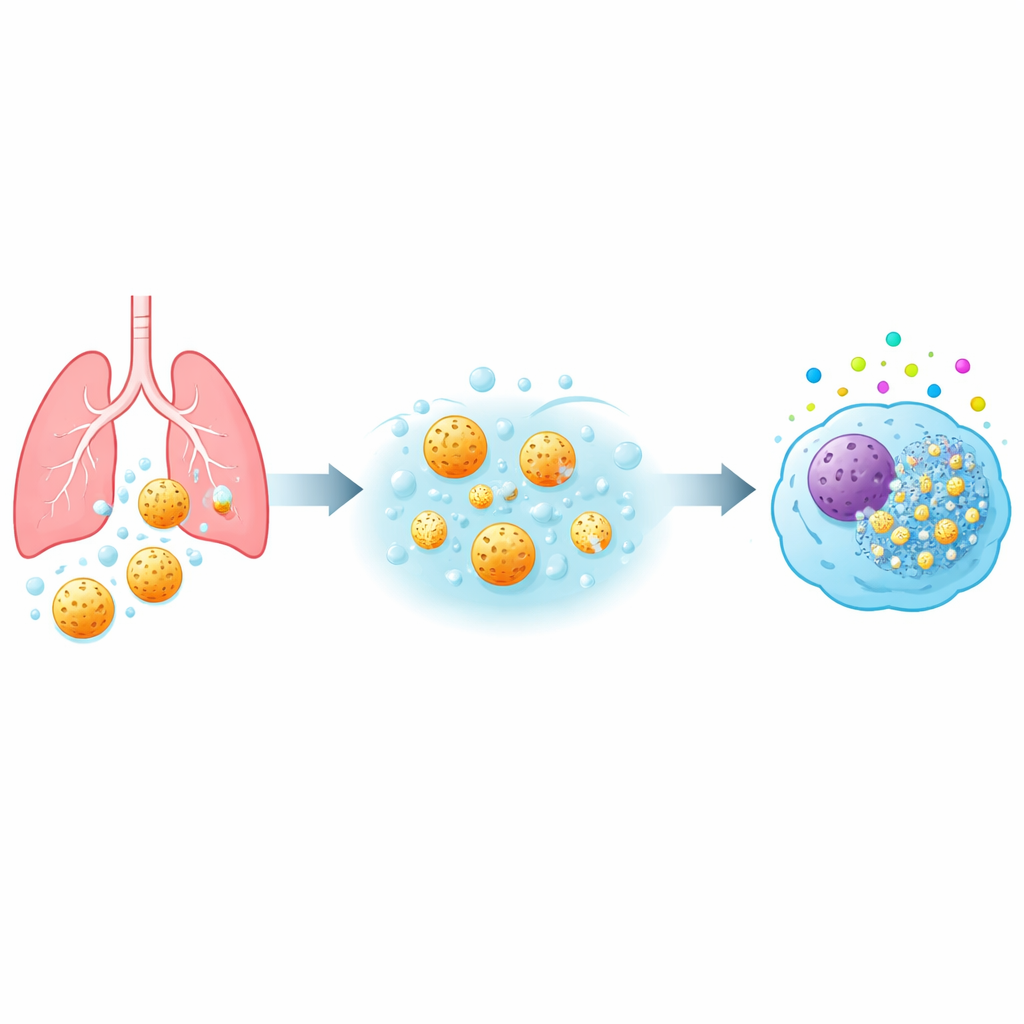
Från luftvägar till immunceller
När damm eller läkemedel når de djupa delarna av lungan möter det först de alveolära makrofagerna—immunceller som patrullerar luftblåsorna och fagocyterar främmande material. Teamet studerade tre typer av mesoporösa kiselpartiklar (benämnda MSP-I, MSP-II och MSP-III) som hade samma övergripande storlek men olika interna porstrukturer och, avgörande, olika upplösningshastigheter i lungliknande vätska. De exponerade flera mänskliga makrofagmodeller, inklusive primära celler från blodgivare och en standard cellinje, för ett brett spektrum av partikeldoser och kontakttider. Genom att mäta mitokondrieaktivitet, membranskada, inflammatoriska signaler och oxidativ stress byggde de en detaljerad säkerhetsprofil för varje partikeltyp.
Hur snabbupplösande partiklar formar säkerheten
Över alla makrofagtyper höll korta 4-timmars exponeringar för partiklarna, även vid relativt höga doser, cellernas mitokondrieaktivitet över 50 %-tröskeln som ofta används för att indikera allvarlig skada. Ingen av partiklarna utlöste frisättning av den centrala inflammatoriska signalen TNF-α, vilket tyder på att de inte framkallade en stark immunvarning under dessa förhållanden. När partiklarna dock placerades i simulerad lungvätska som fick dem att långsamt brytas ner framträdde ett viktigt mönster: när mikropartiklarna eroderade och skapade moln av nanopartiklar ökade toxiciteten. Snabbare upplösande partiklar var mer skadliga vid tidiga tidpunkter, men efter 24 timmar konvergerade alla tre typer till liknande toksicitetsnivåer, vilket nära följde hur lång tid varje partikel behövde för att lösas upp till hälften. Med andra ord bestämde upplösningshastigheten i praktiken tidpunkten för maximal cellstress.
Sköldande partiklar med lungproteiner
Verkliga lungor är inte bara saltlösning—de är rika på proteiner som albumin, det mest förekommande proteinet i lungvätskan. Forskarna efterliknade detta genom att tillsätta serumproteiner eller renat albumin till den lungliknande vätskan. Detta proteinskal, ofta kallat en "proteinkorona", dämpade kiselsubstansens påverkan på makrofagerna, särskilt vid lägre doser. Vid den lägsta observerade skadliga effektdosen på 0,06 mg/mL kunde albumin höja mitokondrieaktiviteten tillbaka till ett intervall som anses icke-skadligt enligt standardriktlinjer. Vid högre doser avtog skyddet, men resultaten visar att lungans naturliga proteinmiljö signifikant kan förbättra den upplevda biokompatibiliteten hos dessa inhalerade bärare.
Koppla partikelnedbrytning till stressignaler
För att förstå hur partikelbeteende inne i cellerna leder till skada mätte teamet reaktiva syrearter (ROS)—kemiskt reaktiva molekyler ofta förknippade med stressvägar—och kontrollerade om lysosomerna, de sura återvinningskompartmenten inne i cellerna, började läcka. Vid den låga referensdosen 0,06 mg/mL låg ROS-nivåer och lysosomal läckage nära normala. Vid högre doser, särskilt med den snabbast upplösande partikeln (MSP-I), ökade både ROS och lysosomal permeabilisering, förenligt med ett scenario där snabb partikelerosion och ackumulering av nanopartiklar belastar cellernas försvar. Ändå producerade partiklarna inte stark frisättning av inflammatoriska cytokiner även under dessa mer stressande förhållanden, vilket pekar på en nyanserad, koncentrations- och tidsberoende respons snarare än en enkel "på/av"-toxicitet.
Att leverera tuberkulosläkemedel över tid
Utöver säkerhet undersökte studien hur partikelegenskaper styr frisättningen av clofazimin, ett antibiotikum som används mot tuberkulos. Både en snabbupplösande bärare (MSP-I) och en långsammare (MSP-III) laddades med små mängder läkemedel och nedsänktes i lungliknande vätska innehållande ett lungsurfaktantlipid. MSP-I frigjorde läkemedlet mycket snabbt och genererade en kortvarig övermättad lösning—höga läkemedelsnivåer som sedan sjönk när läkemedlet sannolikt kristalliserade ut. MSP-III å andra sidan gav något långsammare initial frisättning men en mer stabil läkemedelskoncentration över många timmar. I båda fallen översteg löst clofazimin de koncentrationer som är kända för att döda tuberkulusbakterier, men den långsammare partikeln stödde en mer uthållig exponering som kan vara bättre lämpad för långvariga lungterapier.
Vad detta betyder för framtida inhalationsläkemedel
För en lekmansläsare är huvudbudskapet att hur snabbt dessa porösa kiselbärare löses upp i lungvätska fungerar som en huvudregulator för både säkerhet och prestanda. Vid eller under en dos på 0,06 mg/mL orsakade partiklarna liten mitokondrieskada, måttlig oxidativ stress och ingen tydlig inflammatorisk topp i mänskliga makrofagmodeller, särskilt när en realistisk lungproteinumgivning fanns närvarande. Snabbt upplösande partiklar levererade läkemedel snabbare men genererade också skarpare, tidigare stressignaler, medan långsammare upplösande partiklar gav en mjukare, mer förlängd läkemedelsfrisättning. Dessa insikter tyder på att noggrann justering av partikelporositet och upplösningshastighet kan skapa inhalationsbehandlingar som kombinerar effektiv deposition djupt i lungan, intracellulär läkemedelsleverans och acceptabla säkerhetsmarginaler—ett lovande steg mot bättre terapier för respiratoriska infektioner som tuberkulos.
Citering: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Nyckelord: pulmonal läkemedelsleverans, mesoporösa kiselpartiklar, alveolära makrofager, nanopartikelupplösning, clofazimin