Clear Sky Science · de
Partikelauflösungsrate steuert Makrophagenreaktion und Wirkstofffreisetzung aus mesoporösen Silika-Aerosolträgern
Warum winzige Lungenträger wichtig sind
Direktes Einbringen von Medikamenten in die Lunge ist ein vielversprechender Weg, Krankheiten wie Tuberkulose zu behandeln, während systemische Nebenwirkungen reduziert werden. Diese Studie untersucht eine neue Klasse winziger poröser Silikapartikel, die als „Dual-Skalen“-Träger dienen sollen: sie gelangen als mikroskopische Körnchen in die Lunge und lösen sich dann in der Lungenflüssigkeit zu deutlich kleineren Nanopartikeln auf. Die Forscher stellten zwei praktische Fragen: Wie sicher sind diese Partikel für zentrale Immunzellen der Lunge, und wie steuert die Auflösungsrate die Zellantworten sowie die zeitliche Freisetzung eines Tuberkulosewirkstoffs?
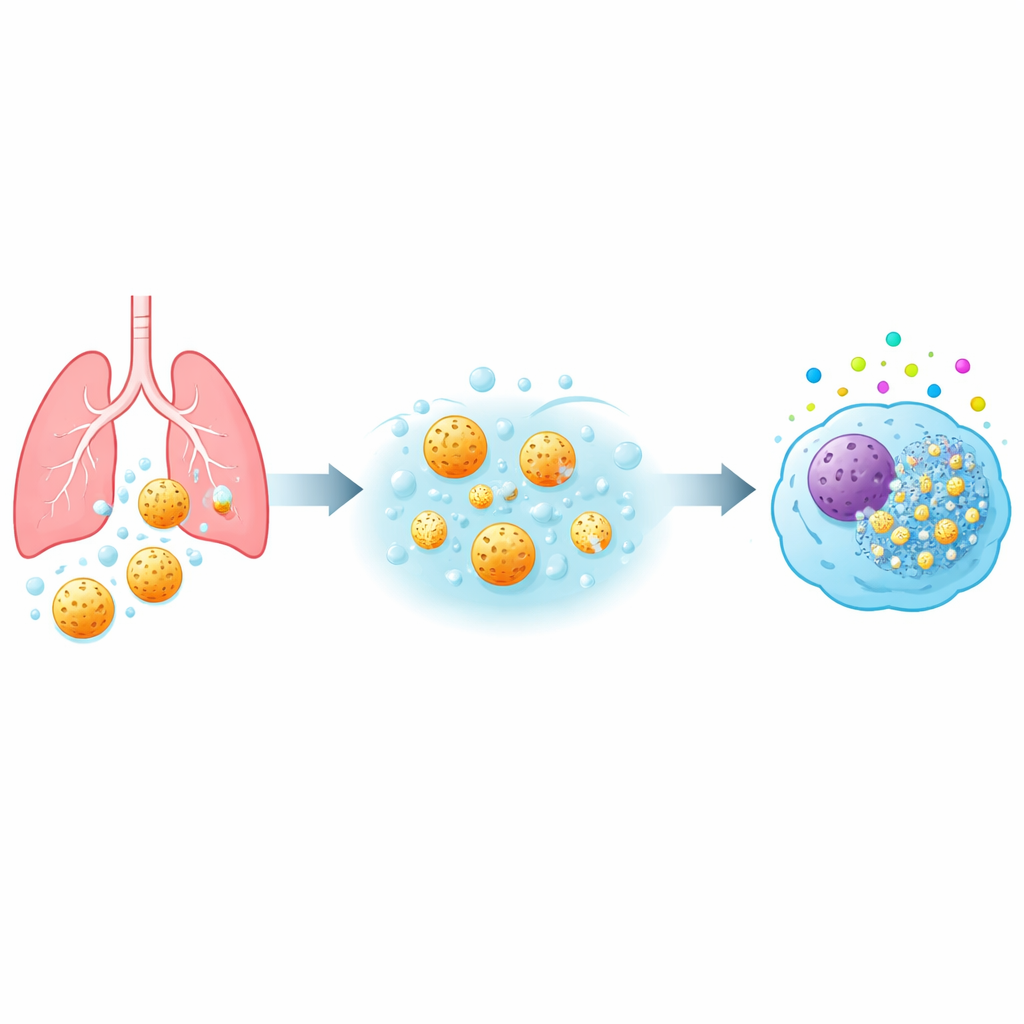
Von den Atemwegen zu den Immunzellen
Wenn Staub oder Arzneistoffe die tiefe Lunge erreichen, treffen sie zuerst auf alveoläre Makrophagen—Immunzellen, die die Lungenbläschen überwachen und Fremdstoffe aufnehmen. Das Team untersuchte drei Typen mesoporöser Silikapartikel (bezeichnet als MSP-I, MSP-II und MSP-III), die in der Gesamtgröße ähnlich waren, sich aber in der inneren Porenstruktur und vor allem in der Auflösungsgeschwindigkeit in lungenähnlicher Flüssigkeit unterschieden. Sie setzten mehrere menschliche Makrophagenmodelle—darunter primäre Zellen von Blutspendern und eine Standardzelllinie—einer breiten Palette von Partikeldosen und Kontaktzeiten aus. Durch Messung der mitochondrialen Aktivität, Membranschädigung, inflammatorischer Signale und oxidativem Stress erstellten sie für jeden Partikeltyp ein detailliertes Sicherheitsprofil.
Wie schnellauflösende Partikel die Sicherheit formen
Über alle Makrophagentypen hinweg blieben bei kurzen 4-stündigen Expositionen gegenüber den Partikeln, selbst bei relativ hohen Dosen, die mitochondriale Aktivität über der 50%-Schwelle, die oft als Grenze für schwere Schäden verwendet wird. Keiner der Partikel löste die Freisetzung des wichtigen Entzündungssignals TNF-α aus, was darauf hindeutet, dass unter diesen Bedingungen kein starker Immunalarm ausgelöst wurde. Sobald die Partikel jedoch in einer simulierten Lungenflüssigkeit platziert wurden, die sie langsam abbaut, zeigte sich ein wichtiges Muster: Während die Mikropartikel erosiv zerfielen und Nanopartikelwolken bildeten, stieg die Toxizität. Schnellauflösende Partikel waren zu frühen Zeitpunkten schädlicher, aber nach 24 Stunden konvergierten alle drei Typen zu ähnlichen Toxizitätsniveaus, die eng mit der Zeitspanne korrelierten, die jedes Partikel für das halbseitige Auflösen benötigte. Anders ausgedrückt bestimmte die Auflösungsrate praktisch das Timing des maximalen zellulären Stresses.
Abschirmung der Partikel durch Lungenproteine
Die reale Lunge ist nicht nur Salzwasser—sie enthält zahlreiche Proteine wie Albumin, das häufigste Protein in der Lungenflüssigkeit. Die Forscher ahmten dies nach, indem sie Serumproteine oder gereinigtes Albumin zur lungenähnlichen Flüssigkeit hinzufügten. Diese Proteinhülle, oft „Protein-Corona“ genannt, milderte die Auswirkungen der Silikaträger auf Makrophagen ab, insbesondere bei niedrigeren Dosen. Bei der niedrigsten beobachteten schadensrelevanten Dosis von 0,06 mg/mL konnte Albumin die mitochondriale Aktivität wieder in einen Bereich anheben, der in Standardrichtlinien als nicht schädlich gilt. Bei höheren Dosen ließ der Schutz nach, doch die Ergebnisse zeigen, dass die natürliche Proteinumgebung in der Lunge die scheinbare Biokompatibilität dieser inhalierten Träger deutlich verbessern kann.
Verknüpfung von Partikelabbau mit Stresssignalen
Um tiefer zu verstehen, wie sich das Partikelverhalten in Zellen zu Schäden führt, maßen die Forscher reaktive Sauerstoffspezies (ROS)—chemisch reaktive Moleküle, die oft mit Stresswegen verbunden sind—und prüften, ob Lysosomen, die sauren Recyclingkompartimente der Zelle, zu lecken begannen. Bei der niedrigen Bezugsdosis von 0,06 mg/mL blieben ROS-Level und lysosomale Permeabilisierung nahe dem Normalwert. Bei höheren Dosen, speziell mit dem am schnellsten auflösenden Partikel (MSP-I), nahmen sowohl ROS als auch lysosomale Durchlässigkeit zu, was zu einem Szenario passt, in dem rascher Partikelabbau und Anreicherung von Nanopartikeln die zellulären Abwehrmechanismen belasten. Dennoch führten selbst unter diesen belastenderen Bedingungen die Partikel nicht zu einer starken Freisetzung inflammatorischer Zytokine, was auf eine nuancierte, konzentrations- und zeitabhängige Reaktion statt einer einfachen Ein/Aus-Toxizität hinweist.
Wirkstofffreisetzung für Tuberkulose über die Zeit
Über die Sicherheit hinaus untersuchte die Studie, wie Partikeleigenschaften die Freisetzung von Clofazimin—einem gegen Tuberkulose eingesetzten Antibiotikum—steuern. Sowohl ein schnellauflösender Träger (MSP-I) als auch ein langsamerer (MSP-III) wurden mit geringen Wirkstoffmengen beladen und in lungenähnliche Flüssigkeit mit einem Lungenoberflächenlipid (Surfactant) getaucht. MSP-I setzte das Medikament sehr rasch frei und erzeugte eine kurzlebige übersättigte Lösung—hohe Wirkstoffkonzentrationen, die dann zurückgingen, vermutlich weil der Wirkstoff auskristallisierte. MSP-III hingegen zeigte eine etwas langsamere Anfangsfreisetzung, sorgte aber über viele Stunden für stabilere Wirkstoffkonzentrationen. In beiden Fällen lagen die gelösten Clofazimin-Spiegel über den Konzentrationen, die für das Abtöten von Tuberkulosebakterien bekannt sind; der langsamere Partikel unterstützte jedoch eine dauerhaftere Exposition, die für langanhaltende Lungentherapien vorteilhafter sein könnte.
Was das für künftige inhaliere Arzneimittel bedeutet
Für eine nichtfachliche Leserschaft lautet die Kernbotschaft, dass die Auflösungsrate dieser porösen Silikaträger in Lungenflüssigkeit als Hauptregler für Sicherheit und Wirksamkeit fungiert. Bei oder unter einer Dosis von 0,06 mg/mL verursachten die Partikel nur geringe mitochondriale Schäden, moderaten oxidativen Stress und keinen klaren inflammatorischen Ausschlag in humanen Makrophagenmodellen, insbesondere wenn eine realistische lungenspezifische Proteinumgebung vorhanden war. Schnellauflösende Partikel setzten Wirkstoff schneller frei, erzeugten aber auch stärkere, frühere Stresssignale, während langsamer auflösende Partikel eine gleichmäßigere, länger anhaltende Wirkstofffreisetzung ermöglichten. Diese Erkenntnisse legen nahe, dass durch sorgfältiges Abstimmen von Porosität und Auflösungsrate Partikel entwickelt werden können, die eine effiziente Ablagerung in der tiefen Lunge, intrazelluläre Wirkstoffabgabe und akzeptable Sicherheitsmargen kombinieren—ein vielversprechender Schritt hin zu besseren Therapien für Atemwegsinfektionen wie Tuberkulose.
Zitation: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Schlüsselwörter: pulmonale Wirkstofffreisetzung, mesoporöse Silikapartikel, alveoläre Makrophagen, Nanopartikelauflösung, Clofazimin