Clear Sky Science · pl
Prędkość rozpuszczania cząstek kontroluje odpowiedź makrofagów i uwalnianie leku z mezoporowatych krzemianowych nośników do inhalacji
Dlaczego małe nośniki do płuc mają znaczenie
Dostarczanie leków bezpośrednio do płuc to atrakcyjna metoda leczenia chorób, takich jak gruźlica, pozwalająca uniknąć wielu ogólnoustrojowych skutków ubocznych. W tym badaniu opisano nową klasę drobnych porowatych cząstek krzemionkowych zaprojektowanych jako nośniki „o podwójnej skali”: wprowadzane do płuc jako mikroskopijne ziarna, a następnie rozpuszczające się w płynach płucnych do znacznie mniejszych nanocząstek. Naukowcy postawili dwa praktyczne pytania: jak bezpieczne są te cząstki dla kluczowych komórek odpornościowych w płucach oraz jak szybkość ich rozpuszczania wpływa zarówno na reakcje komórek, jak i na to, jak lek przeciwgruźliczy jest uwalniany w czasie?
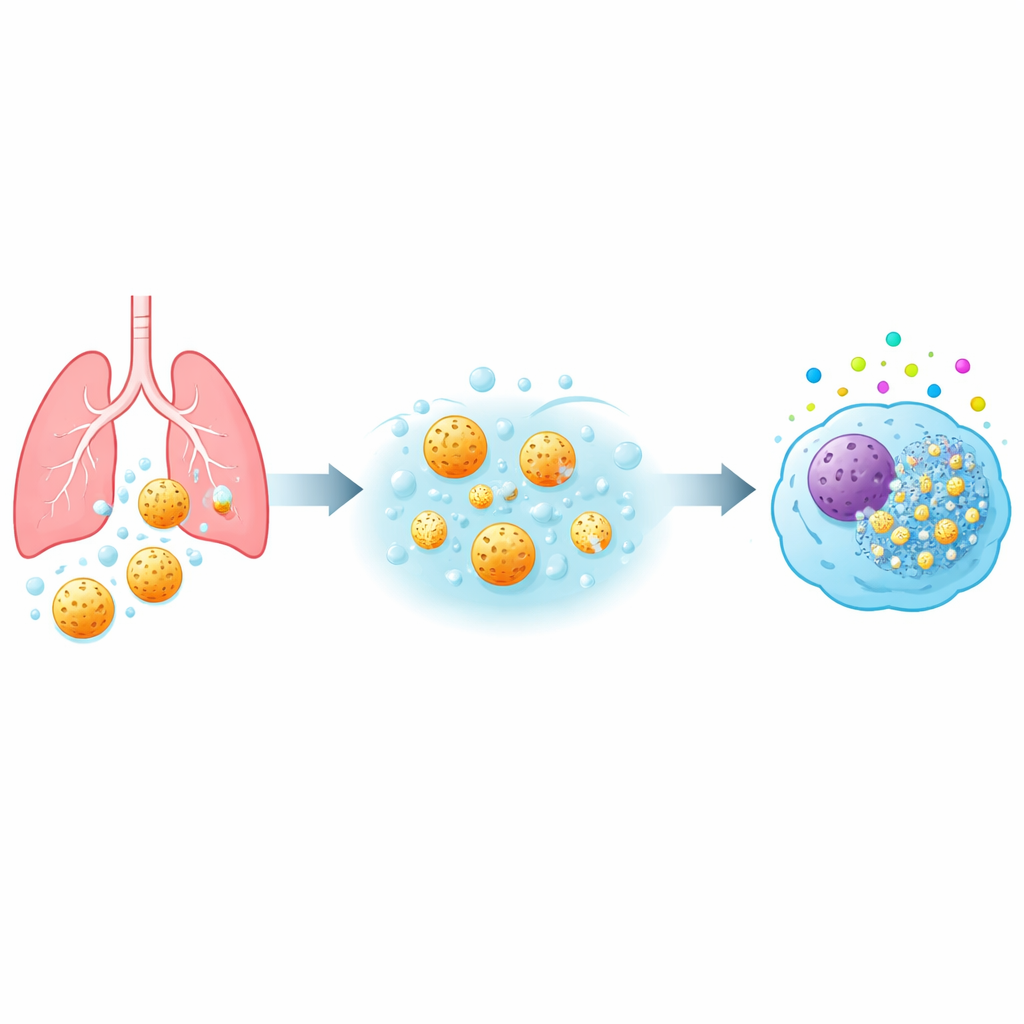
Od dróg oddechowych do komórek odpornościowych
Kiedy kurz lub lek docierają do głębokich części płuc, pierwszymi komórkami, które je napotykają, są makrofagi pęcherzykowe — komórki odpornościowe patrolujące pęcherzyki i pochłaniające obce cząstki. Zespół przebadał trzy typy mezoporowatych cząstek krzemionkowych (oznaczanych MSP-I, MSP-II i MSP-III), które miały podobny rozmiar zewnętrzny, lecz różniły się strukturą porów wewnętrznych i, co istotne, tempem rozpuszczania w płynie przypominającym płyn płucny. Eksponowano na nie kilka modeli ludzkich makrofagów, w tym komórki pierwotne od dawców krwi oraz standardową linię laboratoryjną, przy szerokim zakresie dawek i czasów kontaktu. Poprzez pomiar aktywności mitochondriów, uszkodzeń błony, sygnałów zapalnych i stresu oksydacyjnego zbudowano szczegółowy profil bezpieczeństwa dla każdego typu cząstek.
Jak szybko rozpuszczające się cząstki kształtują bezpieczeństwo
We wszystkich badanych typach makrofagów krótkie, 4‑godzinne ekspozycje na cząstki, nawet przy stosunkowo dużych dawkach, utrzymywały aktywność mitochondrialną powyżej progu 50%, który często służy do wykrywania poważnych uszkodzeń. Żadna z cząstek nie wywołała uwolnienia kluczowego sygnału zapalnego TNF-α, co sugeruje, że w tych warunkach nie prowokowały silnej reakcji zapalnej. Jednak po umieszczeniu cząstek w symulowanym płynie płucnym, który prowokuje ich powolne rozkładanie, ujawnił się ważny wzorzec: w miarę erozji mikropartikelów i powstawania chmur nanocząstek toksyczność rosła. Cząstki rozpuszczające się szybciej były bardziej szkodliwe w początkowych punktach czasowych, ale po 24 godzinach wszystkie trzy typy zbliżały się do podobnego poziomu toksyczności, ściśle korelując z czasem potrzebnym każdej cząstce na rozpuszczenie się w połowie. Innymi słowy, szybkość rozpuszczania ustalała w praktyce synchronizację szczytowego stresu komórkowego.
Osłanianie cząstek białkami płuc
Prawdziwe płuca to nie sama woda z solą — są bogate w białka, takie jak albumina, będąca najobficiej występującym białkiem w płynie płucnym. Badacze odtworzyli to, dodając białka surowicy lub oczyszczoną albuminę do płynu przypominającego płyn płucny. Ta powłoka białkowa, często nazywana „koroną białkową”, złagodziła wpływ nośników krzemionkowych na makrofagi, zwłaszcza przy niższych dawkach. Przy najniższym zaobserwowanym poziomie wywołującym efekt niepożądany 0,06 mg/mL albumina była w stanie podnieść aktywność mitochondrialną z powrotem do zakresu uznawanego za niegroźny według standardowych wytycznych. Przy wyższych dawkach ochrona malała, ale wyniki pokazują, że naturalne środowisko białkowe w płucach może istotnie poprawić pozorną biokompatybilność tych inhalowanych nośników.
Łączenie rozpadu cząstek z sygnałami stresu
Aby głębiej zbadać, jak zachowanie cząstek wewnątrz komórek prowadzi do uszkodzeń, zespół mierzył poziomy reaktywnych form tlenu (ROS) — chemicznie agresywnych cząsteczek często związanych ze szlakami stresu — i sprawdzał, czy lizosomy, kwaśne kompartamenty recyklingowe komórek, zaczynają przeciekać. Przy niskiej referencyjnej dawce 0,06 mg/mL poziomy ROS i przepuszczalność lizosomalna pozostawały bliskie normy. Przy wyższych dawkach, szczególnie dla najszybciej rozpuszczającej się cząstki (MSP-I), zarówno ROS, jak i permeabilizacja lizosomów wzrastały, zgodnie ze scenariuszem, w którym szybka erozja cząstek i nagromadzenie nanocząstek obciążają mechanizmy obronne komórki. Mimo to, nawet w tych bardziej stresujących warunkach, cząstki nie wywołały silnego uwolnienia cytokin zapalnych, co wskazuje na złożoną odpowiedź zależną od stężenia i czasu, a nie prostą odpowiedź „włącz/wyłącz”.
Dostarczanie leków przeciwgruźliczych w czasie
Poza oceną bezpieczeństwa, badanie analizowało, jak właściwości cząstek kontrolują uwalnianie klofaziminy, antybiotyku stosowanego przeciw gruźlicy. Zarówno szybko rozpuszczający się nośnik (MSP-I), jak i wolniej rozpuszczający się (MSP-III) zostały załadowane niewielkimi ilościami leku i umieszczone w płynie przypominającym płyn płucny zawierającym lipid surfaktantu płucnego. MSP-I uwalniał lek bardzo szybko, tworząc krótkotrwałe, nadnasycone roztwory — wysokie stężenia leku, które następnie spadały w miarę prawdopodobnego krystalizowania się leku. MSP-III natomiast charakteryzował się nieco wolniejszym początkowym uwalnianiem, ale bardziej stabilnym stężeniem leku przez wiele godzin. W obu przypadkach rozpuszczone poziomy klofaziminy przekraczały stężenia znane jako bakteriobójcze dla prątków gruźlicy, lecz wolniej rozpuszczająca się cząstka zapewniała dłużej utrzymującą się ekspozycję, która może być korzystniejsza dla długotrwałych terapii płucnych.
Co to oznacza dla przyszłych leków wziewnych
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że szybkość rozpuszczania tych porowatych nośników krzemionkowych w płynie płucnym działa jak główny regulator zarówno bezpieczeństwa, jak i działania. Przy dawce równej lub niższej niż 0,06 mg/mL cząstki powodowały niewielkie uszkodzenia mitochondrialne, umiarkowany stres oksydacyjny i brak wyraźnego wzrostu reakcji zapalnej w modelach ludzkich makrofagów, zwłaszcza w obecności realistycznego środowiska białkowego płuc. Szybciej rozpuszczające się cząstki uwalniały lek szybciej, ale też generowały ostrzejsze, wcześniejsze sygnały stresu, podczas gdy wolniej rozpuszczające się dostarczały płynniejsze, wydłużone uwalnianie leku. Te ustalenia sugerują, że staranne dostrojenie porowatości i szybkości rozpuszczania cząstek może umożliwić tworzenie wziewnych terapii łączących efektywne osadzanie w głębokich partiach płuc, wewnątrzkomórkowe dostarczanie leku i akceptowalne marginesy bezpieczeństwa — obiecujący krok w kierunku lepszych terapii infekcji oddechowych, takich jak gruźlica.
Cytowanie: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Słowa kluczowe: dostarczanie leków do płuc, cząstki mezoporowatego krzemionkowego, makrofagi pęcherzykowe, rozpuszczanie nanocząstek, klofazimina