Clear Sky Science · pt
A taxa de dissolução das partículas controla a resposta dos macrófagos e a liberação de fármaco de transportadores de sílica mesoporosa para inalação
Por que pequenos transportadores pulmonares importam
Inalar o medicamento diretamente nos pulmões é uma forma atraente de tratar doenças como a tuberculose, evitando muitos efeitos colaterais sistêmicos. Este estudo explora uma nova classe de pequenas partículas porosas de sílica projetadas para atuar como transportadores “de dupla escala”: entram nos pulmões como grânulos microscópicos, mas depois se dissolvem em nanopartículas muito menores no fluido pulmonar. Os pesquisadores fizeram duas perguntas práticas: quão seguras são essas partículas para células imunes chave dos pulmões e como a velocidade de dissolução controla tanto as respostas celulares quanto a liberação no tempo de um fármaco contra tuberculose?
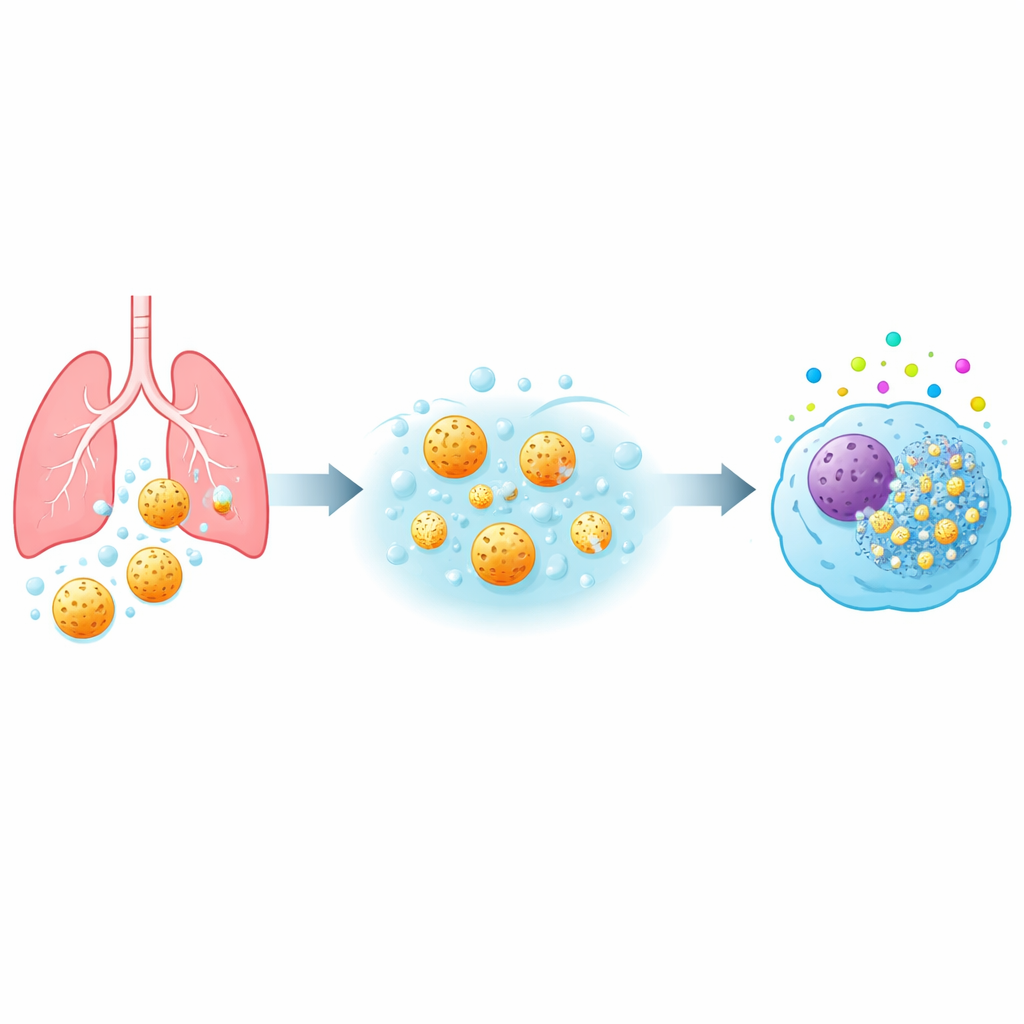
Das vias aéreas às células imunes
Quando qualquer poeira ou medicamento chega ao pulmão profundo, encontra primeiro os macrófagos alveolares — células imunes que patrulham os alvéolos e engolem material estranho. A equipe estudou três tipos de partículas de sílica mesoporosa (chamadas MSP-I, MSP-II e MSP-III) que tinham o mesmo tamanho geral, mas diferentes estruturas de poros internos e, crucialmente, diferentes velocidades de dissolução em fluido semelhante ao pulmonar. Eles expuseram vários modelos de macrófagos humanos, incluindo células primárias de doadores de sangue e uma linha celular padrão de laboratório, a uma ampla faixa de doses e tempos de contato. Medindo atividade mitocondrial, dano da membrana, sinais inflamatórios e estresse oxidativo, construíram um perfil de segurança detalhado para cada tipo de partícula.
Como partículas de rápida dissolução moldam a segurança
Em todos os tipos de macrófagos, exposições curtas de 4 horas às partículas, mesmo em doses relativamente altas, mantiveram a atividade mitocondrial das células acima do limiar de 50% frequentemente usado para sinalizar dano sério. Nenhuma das partículas desencadeou a liberação do principal sinal inflamatório TNF-α, sugerindo que, nessas condições, não provocaram um alarme imune forte. Contudo, quando as partículas foram colocadas em fluido simulado pulmonar que as faz degradar lentamente, apareceu um padrão importante: à medida que os micropartículas erodiam e criavam nuvens de nanopartículas, a toxicidade aumentava. Partículas que se dissolviam mais rápido foram mais nocivas em pontos temporais iniciais, mas após 24 horas os três tipos convergiram para níveis de toxicidade semelhantes, acompanhando de perto o tempo que cada partícula levou para dissolver-se pela metade. Em outras palavras, a taxa de dissolução definiu efetivamente o momento do pico de estresse celular.
Protegendo partículas com proteínas pulmonares
Pulmões reais não são apenas água salgada — são ricos em proteínas como a albumina, a proteína mais abundante no fluido pulmonar. Os pesquisadores imitaram isso adicionando proteínas séricas ou albumina purificada ao fluido semelhante ao pulmonar. Essa camada proteica, frequentemente chamada de “corona proteica”, atenuou o impacto dos transportadores de sílica nos macrófagos, especialmente em doses mais baixas. No menor nível observado de efeito adverso, 0,06 mg/mL, a albumina foi capaz de elevar a atividade mitocondrial de volta a uma faixa considerada não prejudicial segundo diretrizes padrão. Em doses mais altas, a proteção diminuiu, mas os resultados mostram que o ambiente proteico natural do pulmão pode melhorar significativamente a biocompatibilidade aparente desses transportadores inalados.
Ligando a quebra das partículas a sinais de estresse
Para entender melhor como o comportamento das partículas dentro das células leva a danos, a equipe mediu espécies reativas de oxigênio (ROS) — moléculas quimicamente agressivas frequentemente associadas a vias de estresse — e verificou se os lisossomos, os compartimentos ácidos de reciclagem dentro das células, começavam a vazar. Na dose de referência baixa de 0,06 mg/mL, os níveis de ROS e o vazamento lisossômico permaneceram próximos do normal. Em doses maiores, especialmente com a partícula de dissolução mais rápida (MSP-I), tanto ROS quanto a permeabilização lisossômica aumentaram, consistente com um cenário em que a rápida erosão das partículas e o acúmulo de nanopartículas pressionam as defesas celulares. Ainda assim, mesmo sob essas condições mais estressantes, as partículas não produziram forte liberação de citocinas inflamatórias, apontando para uma resposta sutil, dependente de concentração e tempo, em vez de uma toxicidade simples “liga/desliga”.
Liberação de fármacos contra tuberculose ao longo do tempo
Além da segurança, o estudo examinou como as propriedades das partículas controlam a liberação da clofazimina, um antibiótico usado contra a tuberculose. Tanto um transportador de rápida dissolução (MSP-I) quanto um mais lento (MSP-III) foram carregados com pequenas quantidades do fármaco e imersos em fluido semelhante ao pulmonar contendo um lipídio surfactante pulmonar. MSP-I liberou o fármaco muito rapidamente, gerando uma solução supersaturada de curta duração — níveis altos de droga que depois declinaram à medida que o fármaco provavelmente cristalizou. MSP-III, por contraste, produziu uma liberação inicial ligeiramente mais lenta, mas uma concentração de fármaco mais estável por muitas horas. Em ambos os casos, os níveis dissolvidos de clofazimina excederam as concentrações conhecidas por matar as bactérias da tuberculose, mas a partícula mais lenta sustentou uma exposição mais prolongada que pode ser mais adequada para terapias pulmonares de longa duração.
O que isso significa para futuros medicamentos inaláveis
Para um leitor leigo, a mensagem principal é que a velocidade com que esses transportadores de sílica porosa se dissolvem no fluido pulmonar funciona como um botão mestre para segurança e desempenho. Em ou abaixo da dose de 0,06 mg/mL, as partículas causaram pouco dano mitocondrial, estresse oxidativo modesto e nenhum surto inflamatório claro nos modelos de macrófagos humanos, especialmente quando um ambiente proteico pulmonar realista estava presente. Partículas que se dissolvem mais rápido liberaram o fármaco mais rapidamente, mas também geraram sinais de estresse mais nítidos e precoces, enquanto as de dissolução mais lenta produziram uma liberação de fármaco mais suave e prolongada. Essas informações sugerem que ajustar cuidadosamente a porosidade e a taxa de dissolução das partículas pode criar tratamentos inaláveis que combinam deposição eficiente no pulmão profundo, entrega intracelular de fármaco e margens de segurança aceitáveis — um passo promissor rumo a terapias melhores para infecções respiratórias como a tuberculose.
Citação: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Palavras-chave: liberação pulmonar de fármacos, partículas de sílica mesoporosa, macrófagos alveolares, dissolução de nanopartículas, clofazimina