Clear Sky Science · nl
Het oplossingssnelheid van de deeltjes bepaalt macrofagenrespons en geneesmiddelafgifte van mesoporeuze silica-inhalatiedragers
Waarom kleine longdragers belangrijk zijn
Geneesmiddelen rechtstreeks in de longen inademen is een aantrekkelijke manier om ziekten zoals tuberculose te behandelen, terwijl veel systemische bijwerkingen worden vermeden. Deze studie onderzoekt een nieuwe klasse van kleine poreuze silicadeeltjes die ontworpen zijn als "dual-scale" dragers: ze komen de longen binnen als microscopische korrels maar lossen vervolgens op in veel kleinere nanodeeltjes in longvocht. De onderzoekers stelden twee praktische vragen: hoe veilig zijn deze deeltjes voor belangrijke immuuncellen in de longen, en hoe bepaalt de snelheid waarmee ze oplossen zowel de celreacties als de tijdsafhankelijke afgifte van een tuberculosemedicijn?
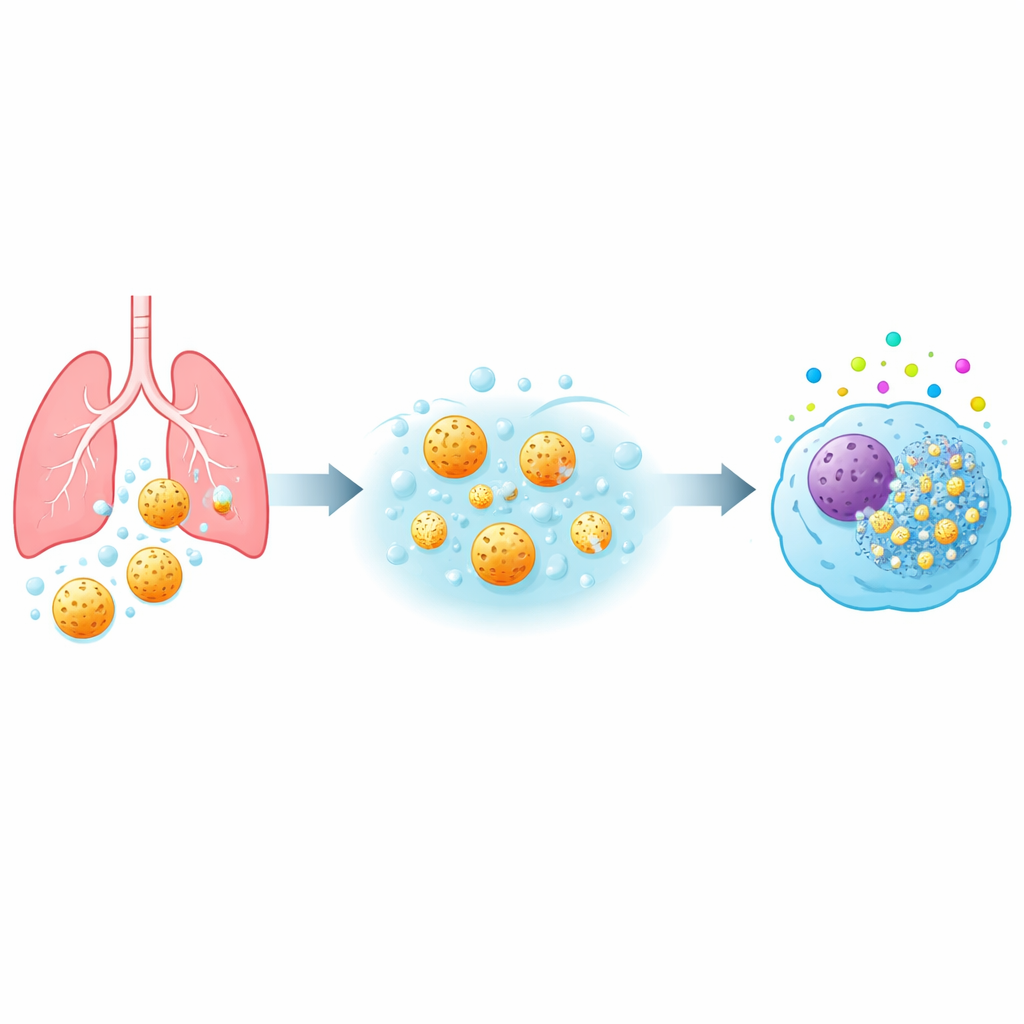
Van luchtwegen naar immuuncellen
Wanneer stof of een geneesmiddel de diepe long bereikt, komt het eerst in aanraking met alveolaire macrofagen—immuuncellen die de luchtzakjes bewaken en vreemd materiaal opnemen. Het team bestudeerde drie typen mesoporeuze silicadeeltjes (genoemd MSP-I, MSP-II en MSP-III) die dezelfde totale grootte hadden maar verschillende interne poriestructuren en, cruciaal, verschillende oplossnelheden in longachtig vocht. Ze brachten meerdere menselijke macrofagenmodellen bloot, inclusief primaire cellen van bloeddonoren en een standaard cellijn uit het laboratorium, aan een breed scala van deeltjesdoses en contacttijden. Door mitochondriale activiteit, membraanschade, ontstekingssignalen en oxidatieve stress te meten bouwden ze een gedetailleerd veiligheidsprofiel voor elk deeltje op.
Hoe snel oplossende deeltjes veiligheid vormen
Bij alle macrofagen types hielden korte blootstellingen van 4 uur aan de deeltjes, zelfs bij relatief hoge doses, de mitochondriale activiteit boven de 50%-drempel die vaak wordt gebruikt om ernstige schade te signaleren. Geen van de deeltjes veroorzaakte de afgifte van het belangrijke ontstekingssignaal TNF-α, wat suggereert dat ze onder deze condities geen sterke immuunalarmreactie uitlokten. Echter, wanneer de deeltjes in gesimuleerd longvocht werden geplaatst dat ze langzaam deed afbreken, verscheen een belangrijk patroon: naarmate de micropartikels erodeerden en wolken van nanodeeltjes creëerden, nam de toxiciteit toe. Sneller oplossende deeltjes waren schadelijker op vroege tijdstippen, maar na 24 uur convergeerden alle drie types naar vergelijkbare toxiciteitsniveaus, nauwkeurig volgend hoe lang elk deeltje nodig had om voor de helft op te lossen. Met andere woorden, de oplossnelheid bepaalde effectief het tijdstip van piekcelstress.
Deeltjes afschermen met longeiwitten
Reële longen zijn niet alleen zout water—ze zitten vol eiwitten zoals albumine, het meest voorkomende eiwit in longvocht. De onderzoekers imiteerden dit door serumeiwitten of gezuiverd albumine toe te voegen aan het longachtige vocht. Deze eiwitmantel, vaak een "protein corona" genoemd, verzachtte de impact van de silicadragers op macrofagen, vooral bij lagere doses. Bij de laagst waargenomen schadelijke concentratie van 0,06 mg/mL kon albumine de mitochondriale activiteit terugbrengen naar een bereik dat volgens gangbare richtlijnen als niet-schadelijk wordt beschouwd. Bij hogere doses vervaagde de bescherming, maar de resultaten tonen aan dat de natuurlijke eiwitomgeving in de long de schijnbare biocompatibiliteit van deze geïnhaleerde dragers aanzienlijk kan verbeteren.
Het koppelen van deeltjesafbraak aan stresssignalen
Om dieper te onderzoeken hoe het gedrag van de deeltjes binnen cellen leidt tot schade, maten de onderzoekers reactieve zuurstofsoorten (ROS)—chemisch agressieve moleculen die vaak met stressroutes geassocieerd zijn—en controleerden of lysosomen, de zure recyclingcompartimenten binnen cellen, begonnen te lekken. Bij de lage referentiedosering van 0,06 mg/mL bleven ROS-niveaus en lysosomale lekkage dicht bij normaal. Bij hogere doses, vooral met het snelst oplossende deeltje (MSP-I), namen zowel ROS als lysosomale permeabilisatie toe, wat overeenkomt met een scenario waarin snelle deeltjeserosie en ophoping van nanodeeltjes de cellulaire verdedigingen belasten. Toch produceerden de deeltjes zelfs onder deze meer stressvolle condities geen sterke afgifte van ontstekingscytokinen, wat wijst op een genuanceerde, concentratie- en tijdsafhankelijke respons in plaats van een eenvoudige "aan/uit" toxiciteit.
Geneesmiddelen tegen tuberculose over tijd afleveren
Naast veiligheid onderzocht de studie hoe deeltjeseigenschappen de afgifte van clofazimine, een antibioticum gebruikt tegen tuberculose, regelen. Zowel een snel oplossende drager (MSP-I) als een langzaam oplossende (MSP-III) werden geladen met kleine hoeveelheden van het geneesmiddel en ondergedompeld in longachtig vocht dat een longsurfaktantlipide bevatte. MSP-I gaf het geneesmiddel zeer snel vrij, waardoor een kortdurende oververzadigde oplossing ontstond—hoge geneesmiddelconcentraties die daarna daalden toen het geneesmiddel vermoedelijk uitkristalliseerde. MSP-III produceerde daarentegen een iets tragere initiële afgifte maar een stabielere geneesmiddelconcentratie over vele uren. In beide gevallen overschreden de gedissocieerde clofaziminewaarden de concentraties waarvan bekend is dat ze tuberculosebacteriën doden, maar het langzamer oplossende deeltje ondersteunde een meer blijvende blootstelling die mogelijk beter geschikt is voor langdurige longtherapieën.
Wat dit betekent voor toekomstige geïnhaleerde geneesmiddelen
Voor de niet‑specialistische lezer is de hoofdboodschap dat de oplossnelheid van deze poreuze silicadragers in longvocht fungeert als een hoofdregelaar voor zowel veiligheid als prestaties. Op of onder een dosis van 0,06 mg/mL veroorzaakten de deeltjes weinig mitochondriale schade, bescheiden oxidatieve stress en geen duidelijke ontstekingspiek in menselijke macrofagenmodellen, vooral wanneer een realistische longeiwitomgeving aanwezig was. Sneller oplossende deeltjes leverden geneesmiddel sneller af maar veroorzaakten ook scherpere, vroegtijdige stresssignalen, terwijl langzamer oplossende deeltjes een soepelere, meer langdurige geneesmiddelafgifte gaven. Deze inzichten suggereren dat het zorgvuldig afstemmen van de porositeit en oplossnelheid van deeltjes kan leiden tot geïnhaleerde behandelingen die efficiënte depositie in de diepe long, intracellulaire geneesmiddelafgifte en aanvaardbare veiligheidsmarges combineren—een veelbelovende stap naar betere therapieën voor luchtweginfecties zoals tuberculose.
Bronvermelding: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Trefwoorden: pulmonaire geneesmiddeltoediening, mesoporeuze silica deeltjes, alveolaire macrofagen, nanodeeltje oplossen, clofazimine