Clear Sky Science · fr
Le taux de dissolution des particules contrôle la réponse des macrophages et la libération de médicaments à partir de porteurs inhalés en silice mésoporeuse
Pourquoi les petits transporteurs pulmonaires comptent
Respirer un médicament directement dans les poumons est une voie attrayante pour traiter des maladies comme la tuberculose tout en évitant de nombreux effets indésirables systémiques. Cette étude explore une nouvelle catégorie de petites particules de silice poreuse conçues pour agir comme des transporteurs « à double échelle » : elles pénètrent dans les poumons sous forme de grains microscopiques puis se dissolvent en nanoparticules beaucoup plus petites dans le liquide pulmonaire. Les chercheurs ont posé deux questions pratiques : dans quelle mesure ces particules sont-elles sûres pour les cellules immunitaires clés des poumons, et comment la vitesse à laquelle elles se dissolvent contrôle-t-elle à la fois la réponse cellulaire et la libération d’un médicament antituberculeux au fil du temps ?
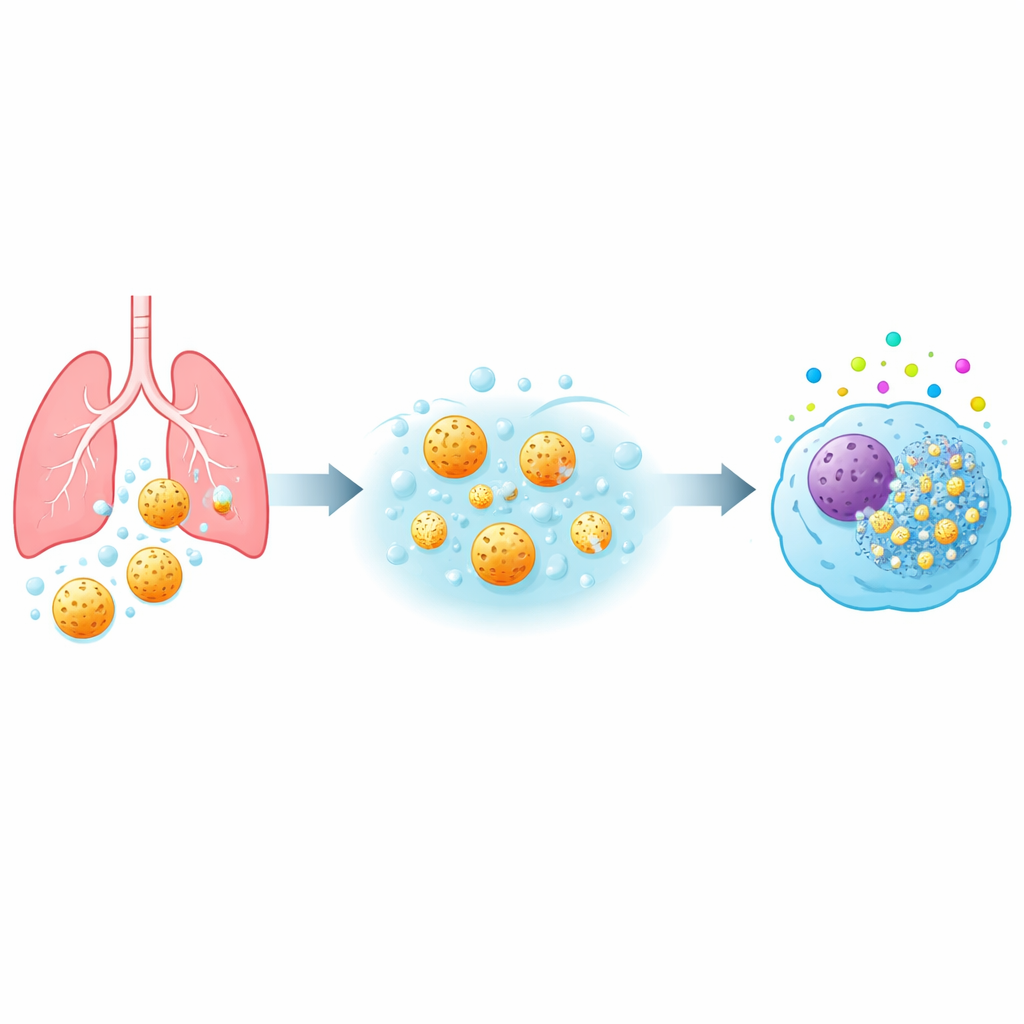
Des voies respiratoires aux cellules immunitaires
Lorsque toute poussière ou substance médicamenteuse atteint les zones profondes du poumon, elle rencontre d’abord les macrophages alvéolaires — des cellules immunitaires qui patrouillent les alvéoles et ingèrent les matériaux étrangers. L’équipe a étudié trois types de particules de silice mésoporeuse (appelées MSP-I, MSP-II et MSP-III) qui présentaient la même taille globale mais différaient par leur structure de pores interne et, de façon cruciale, par leur vitesse de dissolution dans un fluide simulant le poumon. Ils ont exposé plusieurs modèles de macrophages humains, y compris des cellules primaires issues de donneurs sanguins et une lignée cellulaire standard, à une large gamme de doses de particules et de temps de contact. En mesurant l’activité mitochondriale, les lésions membranaires, les signaux inflammatoires et le stress oxydatif, ils ont établi un profil de sécurité détaillé pour chaque type de particule.
Comment les particules à dissolution rapide façonnent la sécurité
Sur l’ensemble des types de macrophages, des expositions courtes de 4 heures aux particules, même à des doses relativement élevées, ont maintenu l’activité mitochondriale des cellules au-dessus du seuil de 50 % souvent utilisé pour signaler des dommages sérieux. Aucune des particules n’a déclenché la libération du signal inflammatoire clé TNF-α, ce qui suggère qu’elles n’ont pas provoqué d’alarme immune forte dans ces conditions. Cependant, lorsque les particules ont été placées dans un fluide pulmonaire simulé qui les fait se dégrader lentement, un schéma important est apparu : à mesure que les microparticules s’érodent et forment des nuages de nanoparticules, la toxicité augmente. Les particules à dissolution plus rapide étaient plus nuisibles aux premiers instants, mais après 24 heures les trois types convergeaient vers des niveaux de toxicité similaires, suivant de près le temps nécessaire à chaque particule pour se dissoudre à moitié. Autrement dit, la vitesse de dissolution fixe effectivement le calendrier du pic de stress cellulaire.
Protéger les particules avec les protéines pulmonaires
Les poumons réels ne sont pas du simple sel — ils sont riches en protéines telles que l’albumine, la protéine la plus abondante du fluide pulmonaire. Les chercheurs ont reproduit cela en ajoutant des protéines sériques ou de l’albumine purifiée au fluide simulant le poumon. Cette coque protéique, souvent appelée « corona protéique », a atténué l’impact des transporteurs en silice sur les macrophages, en particulier à faibles doses. Au niveau d’effet indésirable le plus bas observé de 0,06 mg/mL, l’albumine a été capable de ramener l’activité mitochondriale dans une fourchette considérée non nocive selon les lignes directrices standard. À des doses plus élevées, la protection s’est estompée, mais les résultats montrent que l’environnement protéique naturel du poumon peut améliorer considérablement la biocompatibilité apparente de ces transporteurs inhalés.
Relier la dégradation des particules aux signaux de stress
Pour approfondir la manière dont le comportement des particules à l’intérieur des cellules conduit aux dommages, l’équipe a mesuré les espèces réactives de l’oxygène (ROS) — des molécules chimiquement agressives souvent associées aux voies de stress — et a vérifié si les lysosomes, les compartiments acides de recyclage à l’intérieur des cellules, commençaient à fuir. À la faible dose de référence de 0,06 mg/mL, les niveaux de ROS et la perméabilisation lysosomale sont demeurés proches de la normale. À des doses plus élevées, en particulier avec la particule à dissolution la plus rapide (MSP-I), à la fois les ROS et la perméabilisation lysosomale ont augmenté, ce qui concorde avec un scénario où l’érosion rapide des particules et l’accumulation de nanoparticules mettent à rude épreuve les défenses cellulaires. Pourtant, même dans ces conditions plus stressantes, les particules n’ont pas induit une forte libération de cytokines inflammatoires, ce qui indique une réponse nuancée dépendante de la concentration et du temps plutôt qu’une toxicité binaire « marche/arrêt ».
Libérer des médicaments antituberculeux au fil du temps
Au-delà de la sécurité, l’étude a examiné comment les propriétés des particules contrôlent la libération de la clofazimine, un antibiotique utilisé contre la tuberculose. Un transporteur à dissolution rapide (MSP-I) et un autre plus lent (MSP-III) ont été chargés de petites quantités du médicament et immergés dans un fluide simulant le poumon contenant un lipide du surfactant pulmonaire. MSP-I a libéré le médicament très rapidement, générant une solution brièvement sursaturée — des niveaux élevés de médicament qui ont ensuite diminué à mesure que le médicament se cristallisait probablement. MSP-III, en revanche, a produit une libération initiale un peu plus lente mais une concentration de médicament plus stable sur de nombreuses heures. Dans les deux cas, les niveaux dissous de clofazimine dépassaient les concentrations connues pour tuer les bactéries de la tuberculose, mais la particule plus lente soutenait une exposition plus prolongée qui pourrait être mieux adaptée à des thérapies pulmonaires de longue durée.
Ce que cela signifie pour les futurs médicaments inhalés
Pour un lecteur non spécialiste, le message principal est que la vitesse à laquelle ces transporteurs de silice poreuse se dissolvent dans le fluide pulmonaire agit comme un cadran maître pour la sécurité et la performance. À une dose inférieure ou égale à 0,06 mg/mL, les particules ont causé peu de dommages mitochondriaux, un stress oxydatif modéré et aucune hausse inflammatoire nette dans des modèles de macrophages humains, en particulier lorsque l’environnement protéique pulmonaire réaliste était présent. Les particules à dissolution plus rapide ont délivré le médicament plus rapidement mais ont aussi engendré des signaux de stress plus marqués et précoces, tandis que les particules à dissolution plus lente ont offert une libération de médicament plus douce et prolongée. Ces connaissances suggèrent que le réglage fin de la porosité et du taux de dissolution des particules peut permettre de concevoir des traitements inhalés combinant une déposition efficace en profondeur, une délivrance intracellulaire du médicament et des marges de sécurité acceptables — une avancée prometteuse pour de meilleurs traitements des infections respiratoires comme la tuberculose.
Citation: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Mots-clés: administration pulmonaire de médicaments, particules de silice mésoporeuse, macrophages alvéolaires, dissolution des nanoparticules, clofazimine