Clear Sky Science · es
La velocidad de disolución de partículas controla la respuesta de los macrófagos y la liberación de fármaco desde transportadores de sílice mesoporosa para inhalación
Por qué importan los transportadores diminutos para el pulmón
Administrar medicamentos directamente en los pulmones es una vía atractiva para tratar enfermedades como la tuberculosis evitando muchos efectos secundarios sistémicos. Este estudio explora una nueva clase de pequeñas partículas porosas de sílice diseñadas para actuar como transportadores "de doble escala": ingresan a los pulmones como gránulos microscópicos y luego se disuelven en partículas mucho más pequeñas en el fluido pulmonar. Los investigadores plantearon dos preguntas prácticas: ¿qué tan seguras son estas partículas para las células inmunitarias clave del pulmón? y ¿cómo controla la velocidad de disolución tanto la respuesta celular como la forma en que se libera un fármaco contra la tuberculosis a lo largo del tiempo?
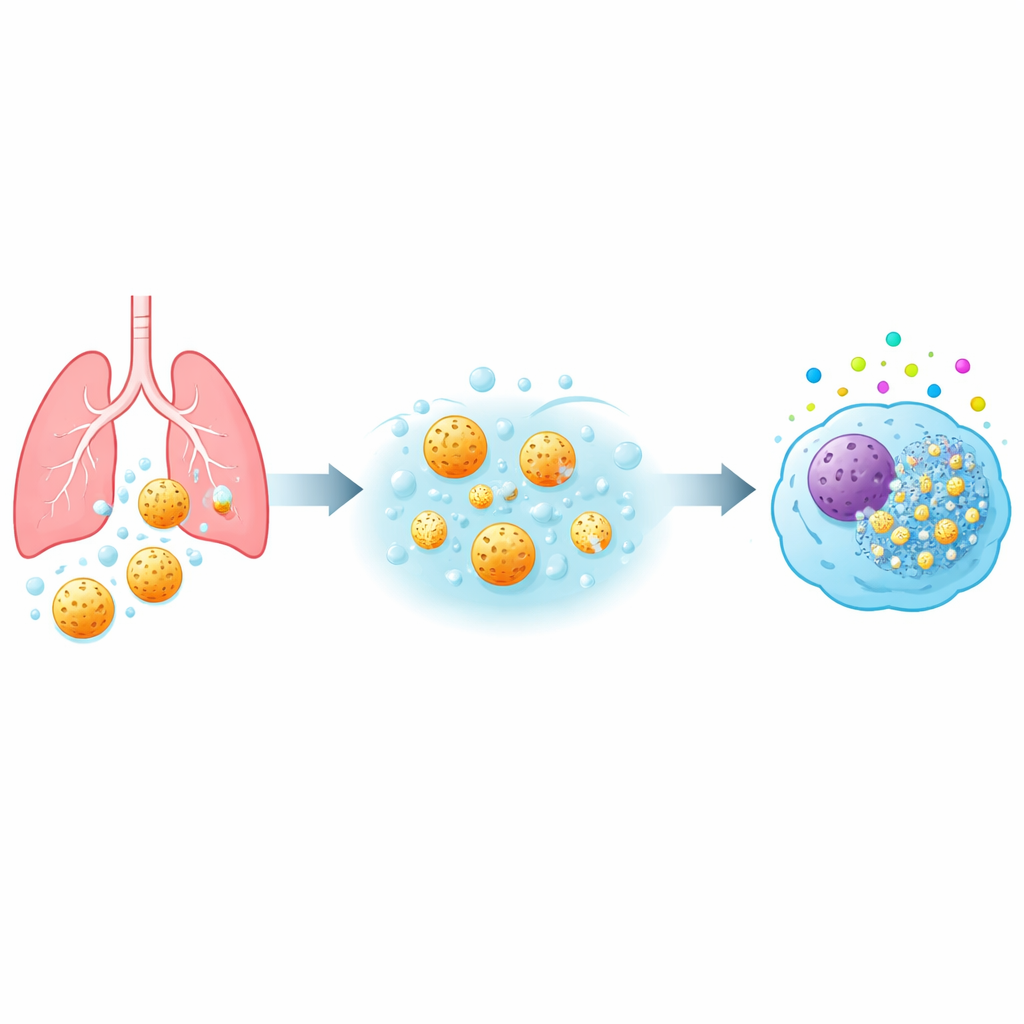
De las vías respiratorias a las células inmunes
Cuando cualquier polvo o medicamento alcanza la zona profunda del pulmón, se encuentra primero con los macrófagos alveolares: células inmunitarias que patrullan los alvéolos y fagocitan material extraño. El equipo estudió tres tipos de partículas de sílice mesoporosa (denominadas MSP-I, MSP-II y MSP-III) que tenían el mismo tamaño global pero diferentes estructuras internas de poros y, de forma crucial, distintas velocidades de disolución en un fluido similar al pulmonar. Expusieron varios modelos de macrófagos humanos, incluidas células primarias de donantes sanguíneos y una línea celular estándar de laboratorio, a una amplia gama de dosis de partículas y tiempos de contacto. Midiendo la actividad mitocondrial, el daño de membrana, señales inflamatorias y estrés oxidativo, construyeron un perfil de seguridad detallado para cada tipo de partícula.
Cómo las partículas de rápida disolución moldean la seguridad
En todos los tipos de macrófagos, exposiciones cortas de 4 horas a las partículas, incluso a dosis relativamente altas, mantuvieron la actividad mitocondrial por encima del umbral del 50% que a menudo se usa para señalar daño grave. Ninguna de las partículas indujo la liberación de la señal inflamatoria clave TNF-α, lo que sugiere que no provocaron una fuerte alarma inmune en estas condiciones. Sin embargo, cuando las partículas se colocaron en fluido simulado del pulmón que las hace degradarse lentamente, apareció un patrón importante: a medida que los micropartículas se erosionaban y generaban nubes de nanopartículas, la toxicidad aumentó. Las partículas de disolución más rápida fueron más dañinas en los primeros puntos temporales, pero tras 24 horas los tres tipos convergieron a niveles de toxicidad similares, siguiendo de cerca el tiempo necesario para que cada partícula se disolviera a la mitad. En otras palabras, la velocidad de disolución fijó efectivamente la sincronía del estrés celular máximo.
Recubrir las partículas con proteínas pulmonares
Los pulmones reales no son solo agua salina: están ricos en proteínas como la albúmina, la proteína más abundante en el fluido pulmonar. Los investigadores mimetizaron esto añadiendo proteínas séricas o albúmina purificada al fluido similar al pulmonar. Esta capa proteica, a menudo llamada "corona proteica", suavizó el impacto de los transportadores de sílice sobre los macrófagos, especialmente a dosis más bajas. En el nivel de efecto adverso más bajo observado de 0,06 mg/mL, la albúmina pudo elevar la actividad mitocondrial de nuevo a un rango considerado no perjudicial según guías estándar. A dosis más altas, la protección se desvaneció, pero los resultados muestran que el entorno proteico natural del pulmón puede mejorar significativamente la biocompatibilidad aparente de estos transportadores inhalados.
Relacionando la degradación de partículas con señales de estrés
Para profundizar en cómo el comportamiento de las partículas dentro de las células conduce al daño, el equipo midió especies reactivas de oxígeno (ROS), moléculas químicamente agresivas asociadas con vías de estrés, y comprobó si los lisosomas, los compartimentos ácidos de reciclaje dentro de las células, empezaban a fugas. En la dosis de referencia baja de 0,06 mg/mL, los niveles de ROS y la fuga lisosomal se mantuvieron cerca de lo normal. A dosis más altas, especialmente con la partícula de disolución más rápida (MSP-I), tanto las ROS como la permeabilización lisosomal aumentaron, coherente con un escenario en el que la rápida erosión de partículas y la acumulación de nanopartículas tensionan las defensas celulares. Aun así, incluso bajo estas condiciones más estresantes, las partículas no provocaron una liberación inflamatoria de citoquinas intensa, lo que apunta a una respuesta matizada, dependiente de la concentración y el tiempo, más que a una toxicidad simple de tipo "todo o nada".
Liberación sostenida de fármacos contra la tuberculosis
Además de la seguridad, el estudio examinó cómo las propiedades de las partículas controlan la liberación de clofazimina, un antibiótico usado contra la tuberculosis. Tanto un transportador de disolución rápida (MSP-I) como otro más lento (MSP-III) se cargaron con pequeñas cantidades del fármaco y se sumergieron en fluido similar al pulmonar que contenía un lípido surfactante pulmonar. MSP-I liberó el fármaco muy rápidamente, generando una solución sobresaturada de corta duración: niveles altos de fármaco que luego disminuyeron conforme el fármaco probablemente cristalizaba. MSP-III, por el contrario, produjo una liberación inicial algo más lenta pero una concentración de fármaco más estable durante muchas horas. En ambos casos, los niveles disueltos de clofazimina superaron las concentraciones conocidas por matar bacterias de tuberculosis, pero la partícula más lenta mantuvo una exposición más sostenida que podría ser más adecuada para terapias pulmonares de larga duración.
Qué significa esto para futuros medicamentos inhalados
Para un lector general, el mensaje principal es que la velocidad a la que estos transportadores porosos de sílice se disuelven en el fluido pulmonar actúa como un control maestro tanto para la seguridad como para el rendimiento. A una dosis igual o inferior a 0,06 mg/mL, las partículas causaron poco daño mitocondrial, un estrés oxidativo modesto y no provocaron un aumento inflamatorio claro en modelos de macrófagos humanos, especialmente cuando estaba presente un entorno proteico pulmonar realista. Las partículas de disolución más rápida liberaron el fármaco con mayor rapidez pero también generaron señales de estrés más agudas y tempranas, mientras que las de disolución más lenta ofrecieron una liberación del fármaco más suave y prolongada. Estos hallazgos sugieren que ajustar cuidadosamente la porosidad y la tasa de disolución de las partículas puede crear tratamientos inhalados que combinen una deposición eficiente en zona profunda del pulmón, entrega intracelular de fármaco y márgenes de seguridad aceptables —un paso prometedor hacia mejores terapias para infecciones respiratorias como la tuberculosis.
Cita: Yalovenko, T., Campos Pacheco, J.E., Sedelius, G. et al. Particle dissolution rate controls macrophage response and drug release from mesoporous silica inhalation carriers. Sci Rep 16, 11229 (2026). https://doi.org/10.1038/s41598-026-46033-8
Palabras clave: administración pulmonar de fármacos, partículas de sílice mesoporosa, macrófagos alveolares, disolución de nanopartículas, clofazimina