Clear Sky Science · sv
Kemokiners potentiella styrande roll för specifika metastasställen vid bröstcancer
Hur cancerceller väljer sitt nästa hem
När bröstcancer sprider sig sker det sällan helt slumpmässigt. Tumörceller dyker ofta upp i lungor, lever, skelett eller hjärna, och dessa nya tillväxter är det som i hög grad hotar patientens liv. Denna studie ställer en enkel men kraftfull fråga: vad händer om osynliga kemiska ”doftspår” i blodet hjälper till att styra vandrande cancerceller mot specifika organ? Genom att följa en liten grupp av dessa signalmolekyler i patienternas blod letade forskarna efter mönster som kan förklara — och en dag hjälpa till att förutsäga eller blockera — vart bröstcancer kommer att resa härnäst. 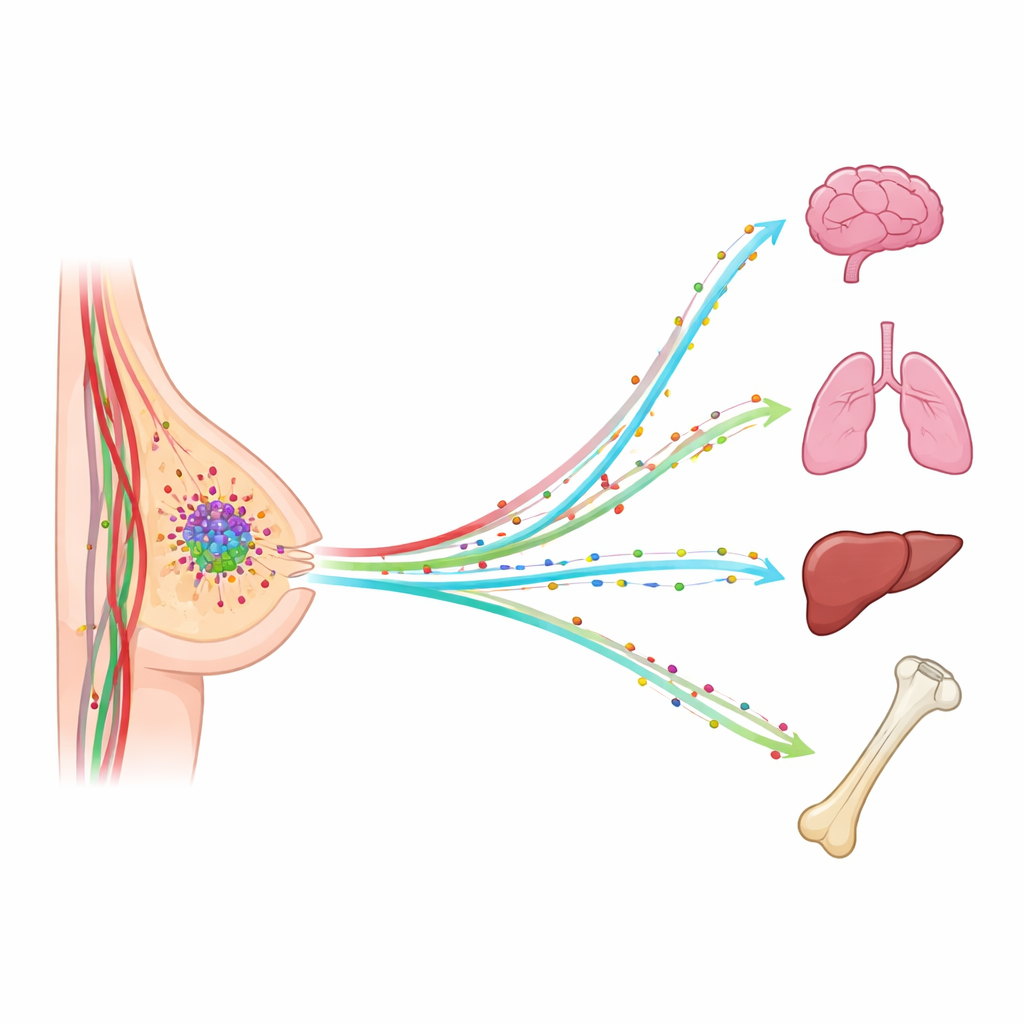
Osynliga signaler som styr cancerceller
Vårt immunsystem använder små proteiner kallade cytokiner och kemokiner som hemvisningsbeacons, för att tala om för celler vart de ska röra sig i kroppen. Tumörer kan kapa dessa signaler för att förbereda avlägsna organ och locka till sig cancerceller, lite som att skicka ut spejare för att anlägga läger. Denna forskargrupp fokuserade på fem sådana molekyler i blodet — IL-4, IL-11, CCL2, CCL4 och CXCL12 — eftersom de är kända för att påverka inflammation, immunrespons och cellrörelse. Idén var att vissa ”signalprofiler” skulle kunna kopplas till särskilda metastasställen och avslöja vilka organ som är mest välkomnande för inkommande cancerceller.
Vad forskarna mätte hos patienterna
Studien följde 175 kvinnor med bröstcancer och jämförde dem med 50 friska kvinnor. Vissa patienter hade sjukdom begränsad till bröstområdet, medan de flesta hade cancer som redan spridit sig till organ som skelett, lungor, lever eller hjärna. Med ett standardlaboratorietest på blodprover mätte forskarna hur mycket av var och en av de fem molekylerna som cirkulerade. De jämförde sedan nivåerna mellan patienter och friska frivilliga, samt mellan patienter med olika tumöregenskaper, behandlingssvar och metastasställen.
Olika signaler, olika destinationer
Blodet hos bröstcancerpatienterna visade högre nivåer av IL-4, CXCL12 och CCL4 än hos friska kvinnor, vilket antyder en övergripande ”pro-metastatisk” signalmiljö. Utöver det framträdde specifika mönster. Högre nivåer av IL-11 kopplades till metastaser i lungorna. Förhöjda IL-4- och CXCL12-nivåer var förknippade med cancer som nått hjärnan, särskilt i tumörer som saknade hormonreceptorer eller hade ett överskott av HER2, ett tillväxtfrämjande protein. Skelettmetastaser associerades med ökade CCL2- och CCL4-nivåer, medan förhöjt CCL2 också markerade leverengagemang. Statistiska tester visade att dessa markörer måttligt kunde skilja patienter med hjärn-, lung- eller levermetastaser från dem utan, vilket antyder en möjlig roll i diagnostik eller riskstratifiering. 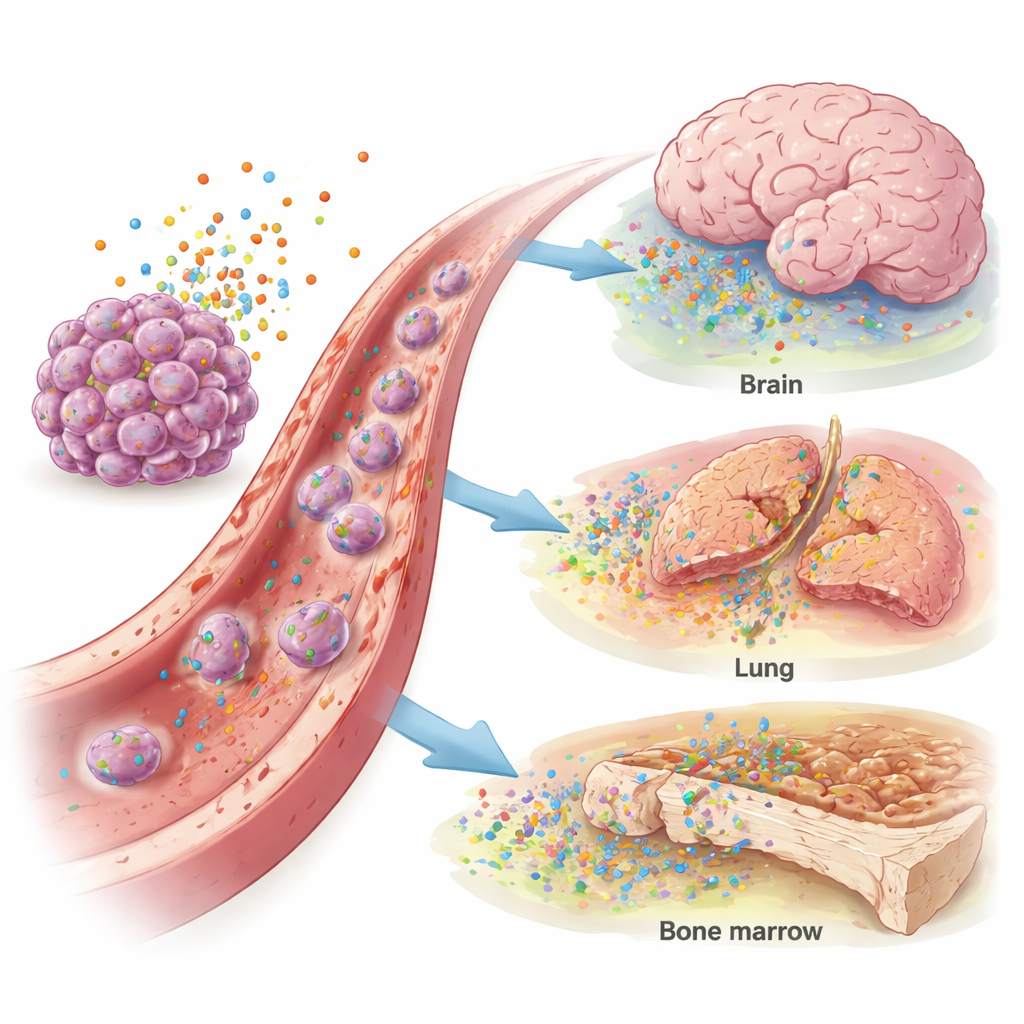
Ledtrådar om prognos och behandlingssvar
Patienter vars tumörer saknade östrogenreceptorer, och de med spridning till hjärna eller lever, tenderade att ha kortare perioder utan återfall, vilket understryker hur vissa biologiska drag och metastasställen hänger ihop med en sämre prognos. Överraskande nog förutsade de övergripande nivåerna av de fem mätta molekylerna inte tydligt hur länge patienterna förblev sjukdomsfria, men högre CCL2 och CXCL12 kopplades till mer avlägsen spridning och sämre behandlingssvar. Det tyder på att även om dessa signaler kanske inte fungerar som enkla fristående prognostiska tester, är de djupt engagerade i hur tumörer växer, utvecklar resistens mot behandling och koloniserar specifika organ.
Vad detta betyder för patienter och framtida vård
För personer som lever med bröstcancer är studiens budskap att metastasering delvis kan styras av igenkännbara kemiska mönster snarare än att vara helt slumpmässig. IL-4 och CXCL12 verkade markera en ökad risk för spridning till hjärnan, IL-11 till lungorna, och CCL2 och CCL4 till skelett och lever. Dessa fynd, även om de baseras på en enda, måttligt stor patientgrupp och en observationsdesign, ger en vägkarta för framtida forskning. Om de bekräftas och förfinas skulle sådana blodmarkörer kunna hjälpa läkare att uppskatta var metastaser sannolikt kommer att uppträda, övervaka högriskpatienter noggrannare och i slutändan utforma läkemedel som stör dessa ”styrsignaler” för att hindra cancer från att hitta nya hem.
Citering: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Nyckelord: bröstcancermetastas, kemokiner, cytokiner, biomarkörer, tumörmikromiljö