Clear Sky Science · nl
De mogelijke richtinggevende rol van chemokines voor specifieke metastaseplaatsen bij borstkanker
Hoe kankercellen hun volgende bestemming kiezen
Wanneer borstkanker zich verspreidt, gebeurt dat zelden willekeurig. Tumorcellen verschijnen vaak in de longen, de lever, botten of hersenen, en die nieuwe gezwellen vormen de grootste bedreiging voor het leven van de patiënt. Deze studie stelt een eenvoudige maar krachtige vraag: wat als onzichtbare chemische “geuren” in de bloedbaan rondzwervende kankercellen helpen leiden naar specifieke organen? Door een kleine groep van deze signaalmoleculen in het bloed van patiënten te volgen, zochten de onderzoekers naar patronen die zouden kunnen verklaren — en op den duur helpen voorspellen of blokkeren — waar borstkanker daarna naartoe zal reizen. 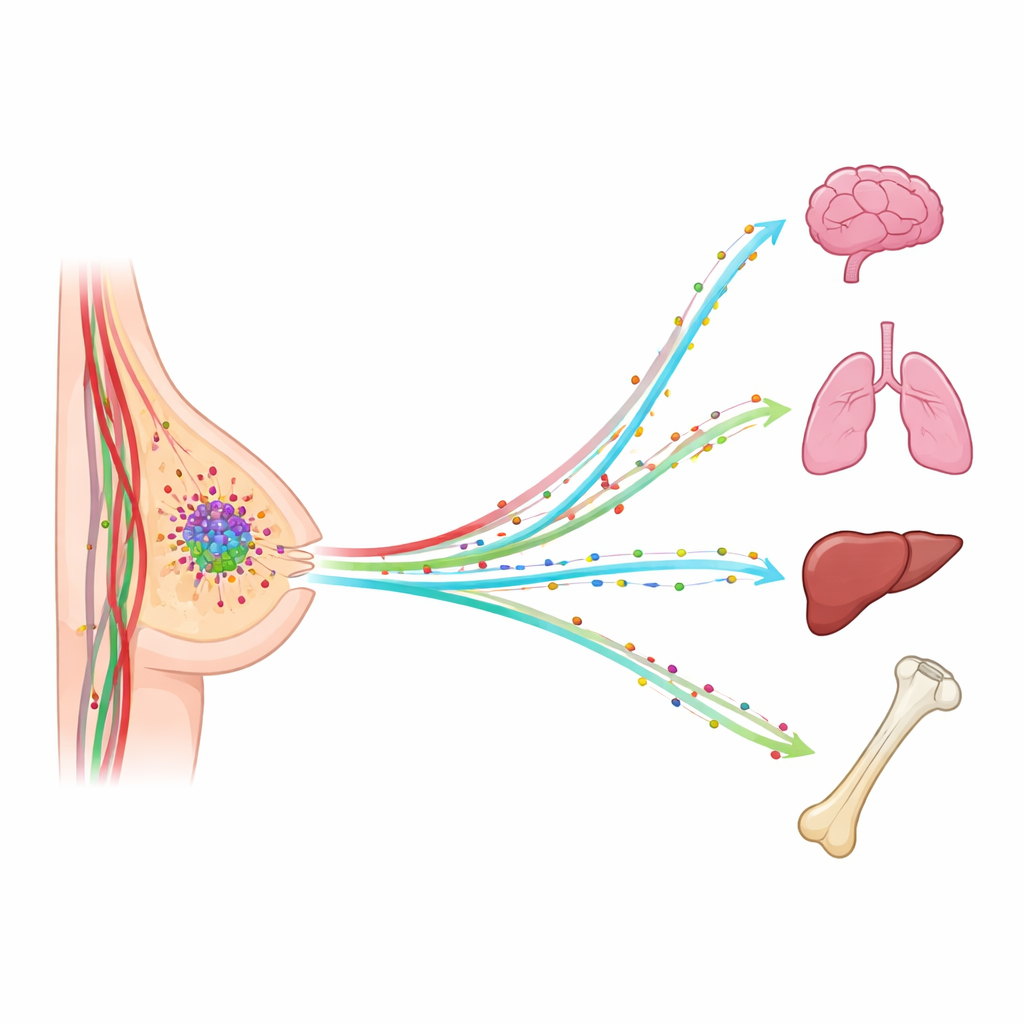
Onzichtbare signalen die kankercellen sturen
Ons immuunsysteem gebruikt kleine eiwitten, cytokines en chemokines genoemd, als navigatiebaken om cellen te vertellen waar ze naartoe moeten in het lichaam. Tumoren kunnen deze signalen kapen om verre organen voor te bereiden en kankercellen aan te trekken, een beetje alsof ze verkenners vooruit sturen om kamp op te bouwen. Dit team richtte zich op vijf van zulke moleculen in het bloed — IL-4, IL-11, CCL2, CCL4 en CXCL12 — omdat bekend is dat ze invloed hebben op ontsteking, immuunreacties en celbeweging. Het idee was dat bepaalde “signaalprofielen” zouden kunnen overeenkomen met specifieke metastaseplaatsen en zo onthullen welke organen het meest gastvrij zijn voor binnenkomende kankercellen.
Wat de onderzoekers bij patiënten maten
De studie volgde 175 vrouwen met borstkanker en vergeleek hen met 50 gezonde vrouwen. Sommige patiënten hadden ziekte beperkt tot het borstgebied, terwijl de meeste al uitzaaiingen naar organen zoals bot, long, lever of hersenen hadden. Met een standaard laboratoriumtest op bloedmonsters maten de onderzoekers hoeveel van elk van de vijf moleculen circuleerde. Daarna vergeleken ze de niveaus tussen patiënten en gezonde vrijwilligers, en tussen patiënten met verschillende tumorkenmerken, behandelreacties en metastaseplaatsen.
Verschillende signalen, verschillende bestemmingen
Het bloed van borstkankerpatiënten vertoonde hogere niveaus van IL-4, CXCL12 en CCL4 dan dat van gezonde vrouwen, wat wijst op een algemeen “pro-metastatisch” signaleringsmilieu. Daarbovenop verschenen specifieke patronen. Hogere IL-11-niveaus werden in verband gebracht met uitzaaiingen in de longen. Verhoogde IL-4 en CXCL12 waren gekoppeld aan kanker die de hersenen had bereikt, vooral bij tumoren zonder hormoonreceptoren of met een overmaat aan HER2, een groeibevorderend eiwit. Botmetastasen waren geassocieerd met verhoogde CCL2 en CCL4, terwijl verhoogd CCL2 ook leverbetrokkenheid aangaf. Statistische tests toonden aan dat deze markers patiënten met hersen-, long- of levermetastasen matig konden onderscheiden van degenen zonder, wat wijst op een mogelijke rol bij diagnose of risicostratificatie. 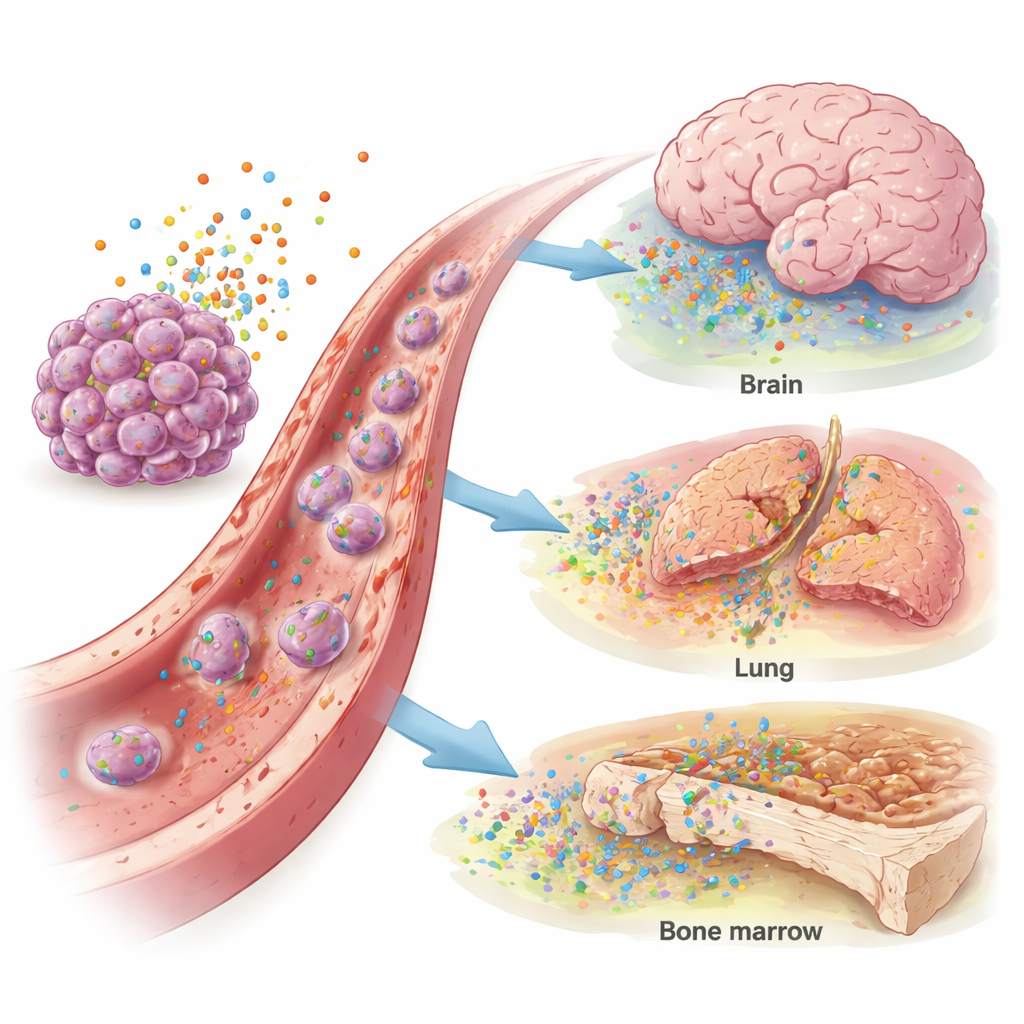
Aanwijzingen voor prognose en behandelrespons
Patiënten wiens tumoren geen oestrogeenreceptoren vertoonden, en degenen met uitzaaiingen naar de hersenen of lever, hadden doorgaans kortere perioden zonder terugkeer van de ziekte, wat benadrukt hoe bepaalde biologische kenmerken en metastaseplaatsen samenhangen met een slechtere prognose. Verrassend genoeg voorspelden de totale niveaus van de vijf gemeten moleculen op zichzelf niet duidelijk hoe lang patiënten ziektevrij bleven, maar hogere CCL2 en CXCL12 werden gekoppeld aan meer verre verspreiding en slechtere respons op therapie. Dit suggereert dat hoewel deze signalen geen eenvoudige, zelfstandige prognostische tests zijn, ze diep betrokken zijn bij hoe tumoren groeien, resistent worden tegen behandeling en specifieke organen koloniseren.
Wat dit betekent voor patiënten en toekomstige zorg
Voor mensen die leven met borstkanker is de boodschap van de studie dat metastasering deels geleid kan worden door herkenbare chemische patronen in plaats van puur willekeurig te zijn. IL-4 en CXCL12 leken een groter risico op uitzaaiingen naar de hersenen aan te geven, IL-11 naar de longen, en CCL2 en CCL4 naar bot en lever. Deze bevindingen, hoewel gebaseerd op één, matig grote patiëntengroep en een observationeel ontwerp, bieden een routekaart voor vervolgonderzoek. Indien bevestigd en verfijnd, zouden dergelijke bloedmarkers artsen kunnen helpen inschatten waar uitzaaiingen het meest waarschijnlijk zullen verschijnen, hoogrisicopatiënten nauwkeuriger volgen en uiteindelijk geneesmiddelen ontwerpen die deze “richtingssignalen” verstoren om te voorkomen dat kanker nieuwe thuisbases vindt.
Bronvermelding: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Trefwoorden: uitzaaiingen van borstkanker, chemokines, cytokines, biomarkers, tumor-micro-omgeving