Clear Sky Science · de
Die mögliche steuernde Rolle von Chemokinen für spezifische Metastasenorte bei Brustkrebs
Wie Krebszellen ihr nächstes Ziel wählen
Wenn sich Brustkrebs ausbreitet, geschieht das selten zufällig. Tumorzellen treten häufig in Lunge, Leber, Knochen oder Gehirn auf, und genau diese neuen Herde sind es, die das Leben der Patientinnen am stärksten bedrohen. Die Studie stellt eine einfache, aber wirkungsvolle Frage: Was, wenn unsichtbare chemische "Duftspuren" im Blutstrom wandernde Krebszellen zu bestimmten Organen lenken? Indem die Forschenden eine kleine Gruppe dieser Signalstoffe im Blut von Patientinnen verfolgten, suchten sie nach Mustern, die erklären — und eines Tages vorhersagen oder blockieren — könnten, wohin sich der Brustkrebs als Nächstes ausbreitet. 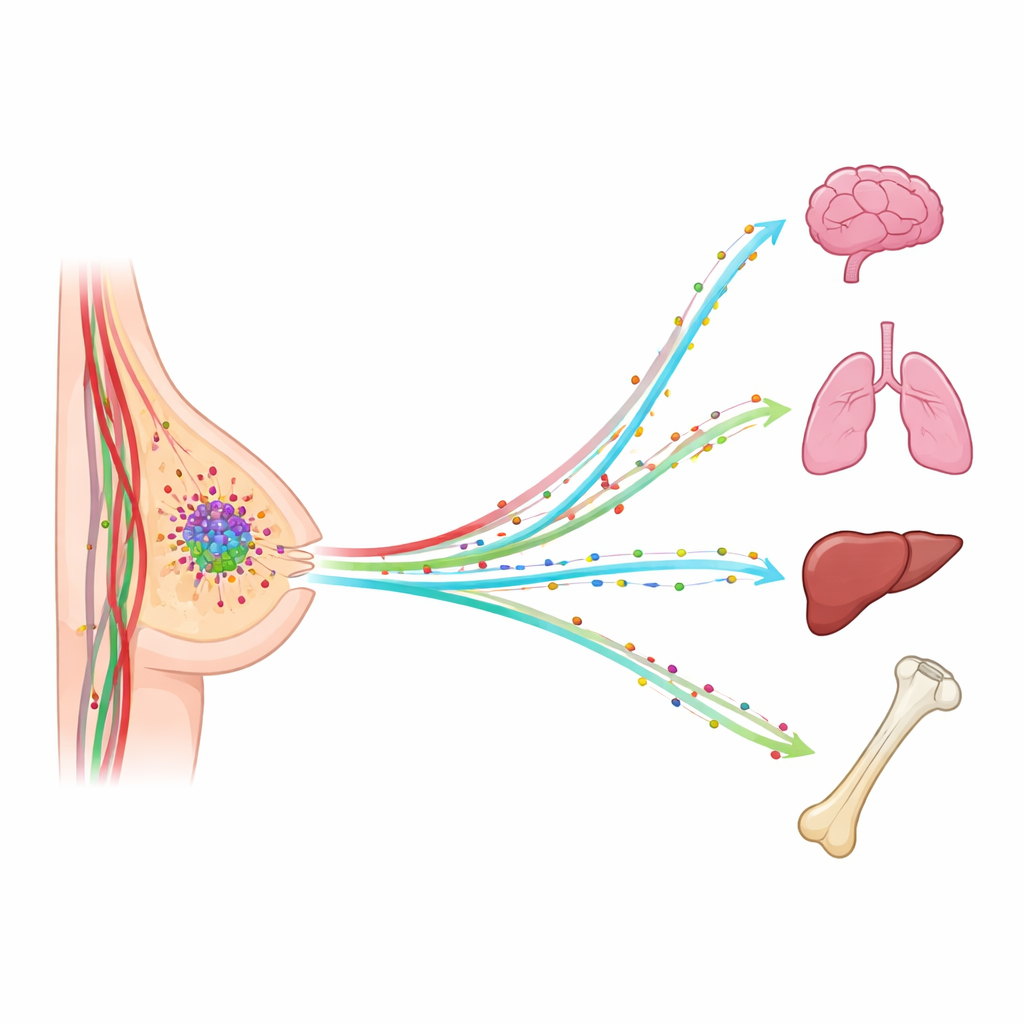
Unsichtbare Signale, die Krebszellen steuern
Unser Immunsystem nutzt kleine Proteine, sogenannte Zytokine und Chemokine, als Wegweiser, die Zellen sagen, wohin sie im Körper wandern sollen. Tumore können diese Signale kapern, um entfernte Organe vorzubereiten und Krebszellen anzulocken — ähnlich wie Kundschafter, die vorausgeschickt werden, um ein Lager zu errichten. Das Team konzentrierte sich auf fünf solcher Moleküle im Blut — IL-4, IL-11, CCL2, CCL4 und CXCL12 — weil bekannt ist, dass sie Entzündungen, Immunantworten und Zellbewegung beeinflussen. Die Idee war, dass bestimmte "Signaturprofile" zu bestimmten Metastasenorten passen könnten und damit offenbaren, welche Organe für eintreffende Krebszellen besonders empfänglich sind.
Was die Forschenden bei Patientinnen gemessen haben
Die Studie begleitete 175 Frauen mit Brustkrebs und verglich sie mit 50 gesunden Frauen. Einige Patientinnen hatten auf die Brustregion beschränkte Erkrankung, während die meisten bereits Metastasen in Organen wie Knochen, Lunge, Leber oder Gehirn aufwiesen. Mit einem standardisierten Labortest an Blutproben bestimmten die Forschenden die zirkulierenden Mengen der fünf Moleküle. Anschließend verglichen sie die Werte zwischen Patientinnen und gesunden Freiwilligen sowie zwischen Patientinnen mit verschiedenen Tumoreigenschaften, Ansprechen auf Therapien und Metastasenorten.
Unterschiedliche Signale, unterschiedliche Ziele
Das Blut von Brustkrebspatientinnen wies höhere Konzentrationen von IL-4, CXCL12 und CCL4 auf als das von gesunden Frauen, was auf ein insgesamt "pro-metastatisches" Signalumfeld hindeutet. Darüber hinaus zeigten sich spezifische Muster. Höhere IL-11-Werte standen im Zusammenhang mit Lungenmetastasen. Erhöhte IL-4- und CXCL12-Spiegel waren mit Tumoren assoziiert, die das Gehirn erreicht hatten, insbesondere bei Tumoren ohne Hormonrezeptoren oder mit Überexpression von HER2, einem wachstumsfördernden Protein. Knochenmetastasen korrelierten mit erhöhten CCL2- und CCL4-Werten, während erhöhte CCL2-Werte auch auf Leberbeteiligung hinwiesen. Statistische Tests zeigten, dass diese Marker Patientinnen mit Hirn-, Lungen- oder Lebermetastasen moderat von denen ohne unterscheiden konnten, was auf eine mögliche Rolle bei Diagnose oder Risikostratifizierung hinweist. 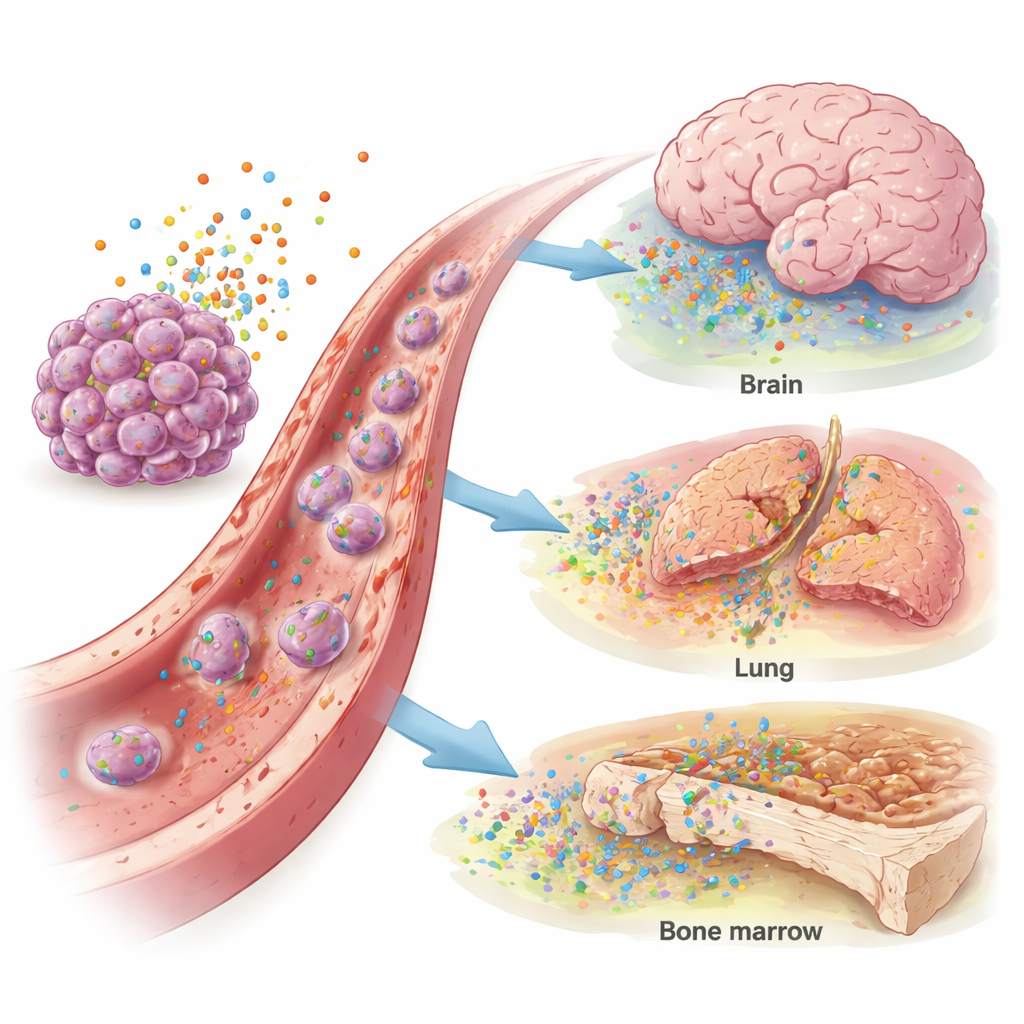
Anhaltspunkte für Prognose und Therapieansprechen
Patientinnen mit ER-negativen Tumoren (ohne Östrogenrezeptoren) sowie solche mit Metastasen in Gehirn oder Leber hatten tendenziell kürzere krankheitsfreie Intervalle, was unterstreicht, wie bestimmte biologische Merkmale und Metastasenorte mit einer ungünstigeren Prognose einhergehen. Überraschenderweise sagten die Gesamtwerte der fünf gemessenen Moleküle allein nicht klar voraus, wie lange Patientinnen ohne Krankheitsrückfall blieben; jedoch waren höhere CCL2- und CXCL12-Spiegel mit vermehrter Fernmetastasierung und schlechterem Therapieansprechen verbunden. Das deutet darauf hin, dass diese Signale zwar keine einfachen Einzelprognosetests sind, aber tief in die Prozesse eingebunden sind, wie Tumoren wachsen, Therapien widerstehen und spezifische Organe besiedeln.
Was das für Patientinnen und die künftige Versorgung bedeutet
Für Menschen mit Brustkrebs lautet die Botschaft der Studie, dass Metastasierung teilweise von erkennbaren chemischen Mustern gelenkt werden könnte und nicht rein zufällig abläuft. IL-4 und CXCL12 schienen ein erhöhtes Risiko für Hirnmetastasen anzuzeigen, IL-11 für Lungenmetastasen und CCL2 sowie CCL4 für Knochen und Leber. Diese Ergebnisse, obwohl sie auf einer einzelnen, mäßig großen Patientengruppe und einem beobachtenden Studiendesign beruhen, liefern eine Landkarte für künftige Forschung. Werden sie bestätigt und verfeinert, könnten solche Blutmarker Ärzten helfen abzuschätzen, wo Metastasen wahrscheinlich auftreten, Hochrisikopatientinnen intensiver zu überwachen und letztlich Medikamente zu entwickeln, die diese "Orientierungssignale" stören, damit sich Krebs keine neuen Nischen schafft.
Zitation: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Schlüsselwörter: Brustkrebsmetastasen, Chemokine, Zytokine, Biomarker, Tumormikroumgebung