Clear Sky Science · it
Il possibile ruolo direttivo delle chemokine per siti metastatici specifici nel cancro al seno
Come le cellule tumorali scelgono la loro prossima destinazione
Quando il cancro al seno si diffonde, raramente lo fa in modo casuale. Le cellule tumorali spesso compaiono nei polmoni, nel fegato, nelle ossa o nel cervello, e queste nuove lesioni sono ciò che più mette a rischio la vita del paziente. Questo studio pone una domanda semplice ma potente: e se degli “odoretti” chimici invisibili nel flusso sanguigno aiutassero a guidare le cellule tumorali erranti verso organi specifici? Tracciando un piccolo gruppo di queste molecole segnale nel sangue dei pazienti, i ricercatori hanno cercato schemi che potessero spiegare — e un giorno aiutare a prevedere o bloccare — dove il cancro al seno si sposterà dopo.
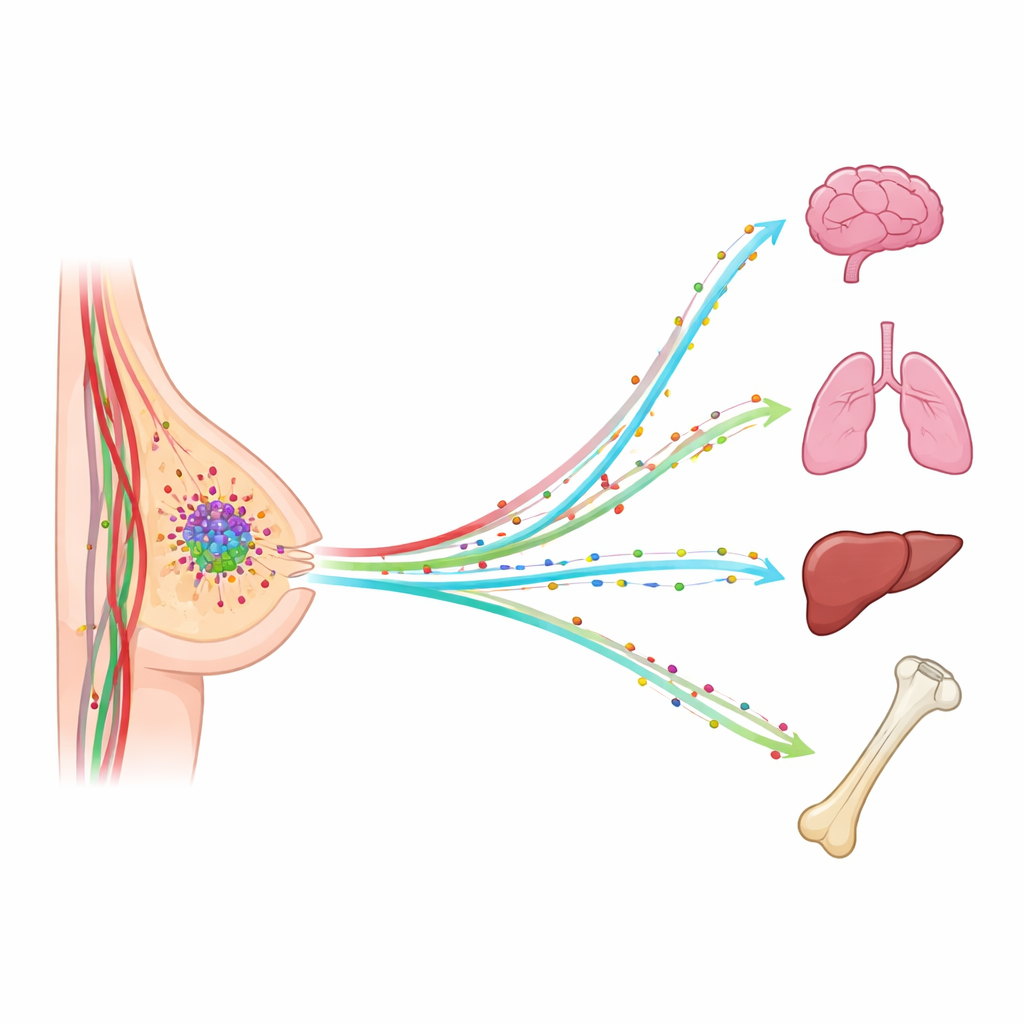
Segnali invisibili che indirizzano le cellule tumorali
Il nostro sistema immunitario utilizza piccole proteine chiamate citochine e chemokine come segnali di richiamo, indicando alle cellule dove muoversi nel corpo. I tumori possono dirottare questi segnali per preparare organi distanti e attirare cellule tumorali, un po’ come inviare esploratori in anticipo per stabilire un accampamento. Il gruppo di lavoro si è concentrato su cinque di queste molecole nel sangue — IL-4, IL-11, CCL2, CCL4 e CXCL12 — perché sono note per influenzare l’infiammazione, le risposte immunitarie e il movimento cellulare. L’idea era che certi “profili di segnale” potessero corrispondere a siti metastatici particolari, rivelando quali organi siano più ospitali per le cellule tumorali in arrivo.
Cosa hanno misurato i ricercatori nei pazienti
Lo studio ha seguito 175 donne con cancro al seno e le ha confrontate con 50 donne sane. Alcune pazienti avevano la malattia confinata alla mammella, mentre la maggior parte aveva un cancro già diffuso in organi come ossa, polmone, fegato o cervello. Utilizzando un test di laboratorio standard sui campioni di sangue, i ricercatori hanno misurato la quantità di ciascuna delle cinque molecole circolanti. Hanno poi confrontato i livelli tra pazienti e volontarie sane e tra pazienti con diverse caratteristiche tumorali, risposte ai trattamenti e sedi di metastasi.
Segnali diversi, destinazioni diverse
Il sangue delle pazienti con cancro al seno mostrava livelli più alti di IL-4, CXCL12 e CCL4 rispetto a quello delle donne sane, suggerendo un ambiente segnale complessivo “pro-metastatico”. Oltre a questo, sono emersi schemi specifici. Livelli più elevati di IL-11 sono stati associati a metastasi polmonari. IL-4 e CXCL12 aumentati sono risultati legati al cancro che aveva raggiunto il cervello, in particolare in tumori privi di recettori ormonali o con eccesso di HER2, una proteina che promuove la crescita. Le metastasi ossee sono state associate a un incremento di CCL2 e CCL4, mentre un aumento di CCL2 ha anche segnalato interessamento epatico. I test statistici hanno mostrato che questi marcatori potevano distinguere moderatamente i pazienti con metastasi cerebrali, polmonari o epatiche da quelli senza, suggerendo un ruolo nella diagnosi o nella stratificazione del rischio.
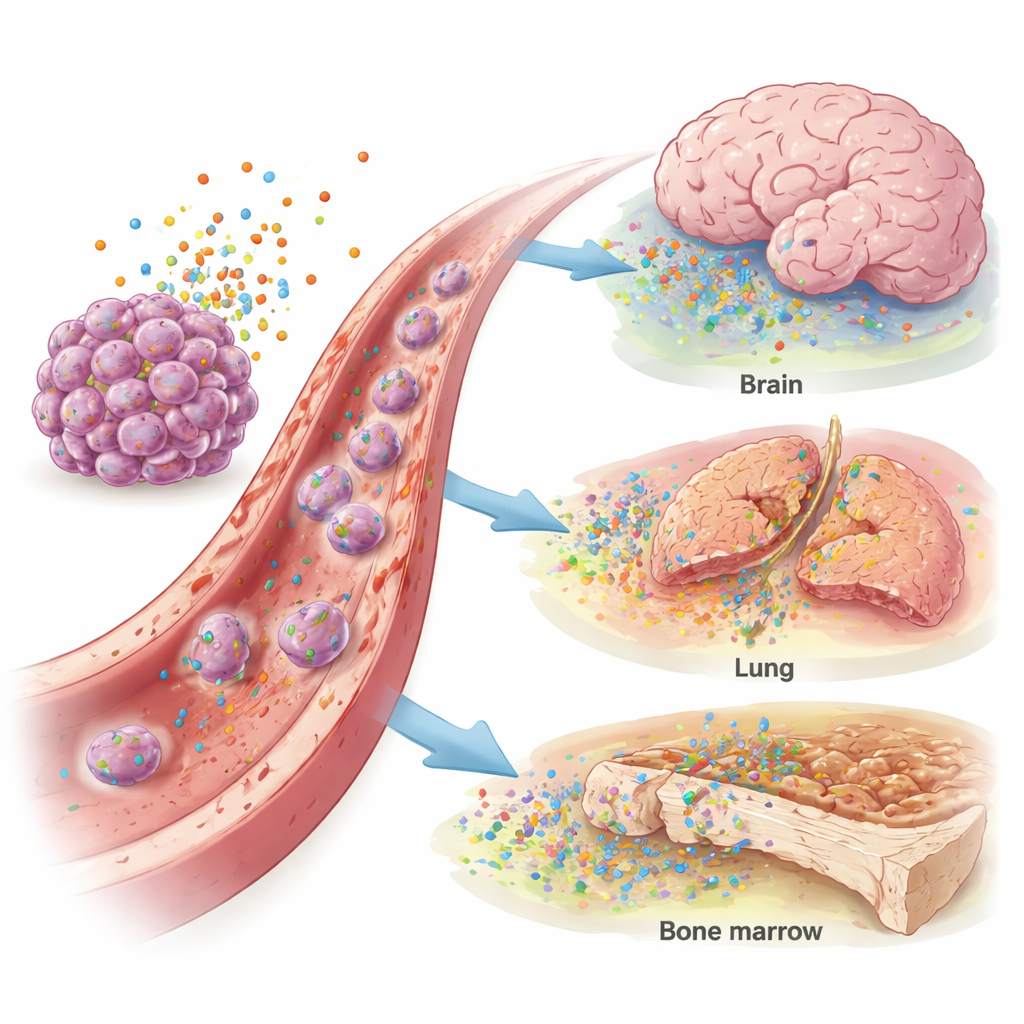
Indizi per prognosi e risposta al trattamento
Le pazienti i cui tumori erano privi di recettori estrogenici, e quelle con diffusione al cervello o al fegato, tendevano ad avere periodi più brevi senza recidiva della malattia, evidenziando come certe caratteristiche biologiche e sedi metastatiche vadano di pari passo con una prognosi peggiore. Sorprendentemente, i livelli complessivi delle cinque molecole misurate da soli non hanno predetto in modo chiaro per quanto tempo le pazienti sono rimaste libere da malattia, ma livelli più alti di CCL2 e CXCL12 sono stati collegati a una maggiore diffusione a distanza e a una risposta peggiore alla terapia. Questo suggerisce che, pur non essendo semplici test prognostici autonomi, questi segnali sono profondamente coinvolti nel modo in cui i tumori crescono, resistono ai trattamenti e colonizzano organi specifici.
Cosa significa questo per i pazienti e per le cure future
Per le persone che vivono con il cancro al seno, il messaggio dello studio è che la metastasi può essere in parte guidata da schemi chimici riconoscibili piuttosto che essere puramente casuale. IL-4 e CXCL12 sembrano segnalare un rischio maggiore di diffusione al cervello, IL-11 ai polmoni, e CCL2 e CCL4 alle ossa e al fegato. Questi risultati, sebbene basati su un singolo gruppo di pazienti di dimensioni moderate e su uno studio osservazionale, forniscono una mappa per ricerche future. Se confermati e raffinati, tali marcatori ematici potrebbero aiutare i medici a stimare dove è più probabile che compaiano metastasi, monitorare più attentamente i pazienti ad alto rischio e, in ultima analisi, progettare farmaci che interrompano questi “segnali guida” per impedire al cancro di trovare nuove dimore.
Citazione: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Parole chiave: metastasi del cancro al seno, chemokine, citochine, biomarcatori, microambiente tumorale