Clear Sky Science · fr
Le rôle directeur potentiel des chimiokines pour des sites métastatiques spécifiques dans le cancer du sein
Comment les cellules cancéreuses choisissent leur prochaine résidence
Lorsque le cancer du sein se propage, ce n’est rarement au hasard. Les cellules tumorales se retrouvent souvent dans les poumons, le foie, les os ou le cerveau, et ce sont ces nouvelles poussées qui menacent le plus la vie du patient. Cette étude pose une question simple mais puissante : et si des « parfums » chimiques invisibles dans le sang aidaient à guider les cellules cancéreuses errantes vers des organes spécifiques ? En suivant un petit groupe de ces molécules signal dans le sang des patientes, les chercheurs ont cherché des motifs susceptibles d’expliquer — et un jour d’aider à prédire ou bloquer — où le cancer du sein migrera ensuite. 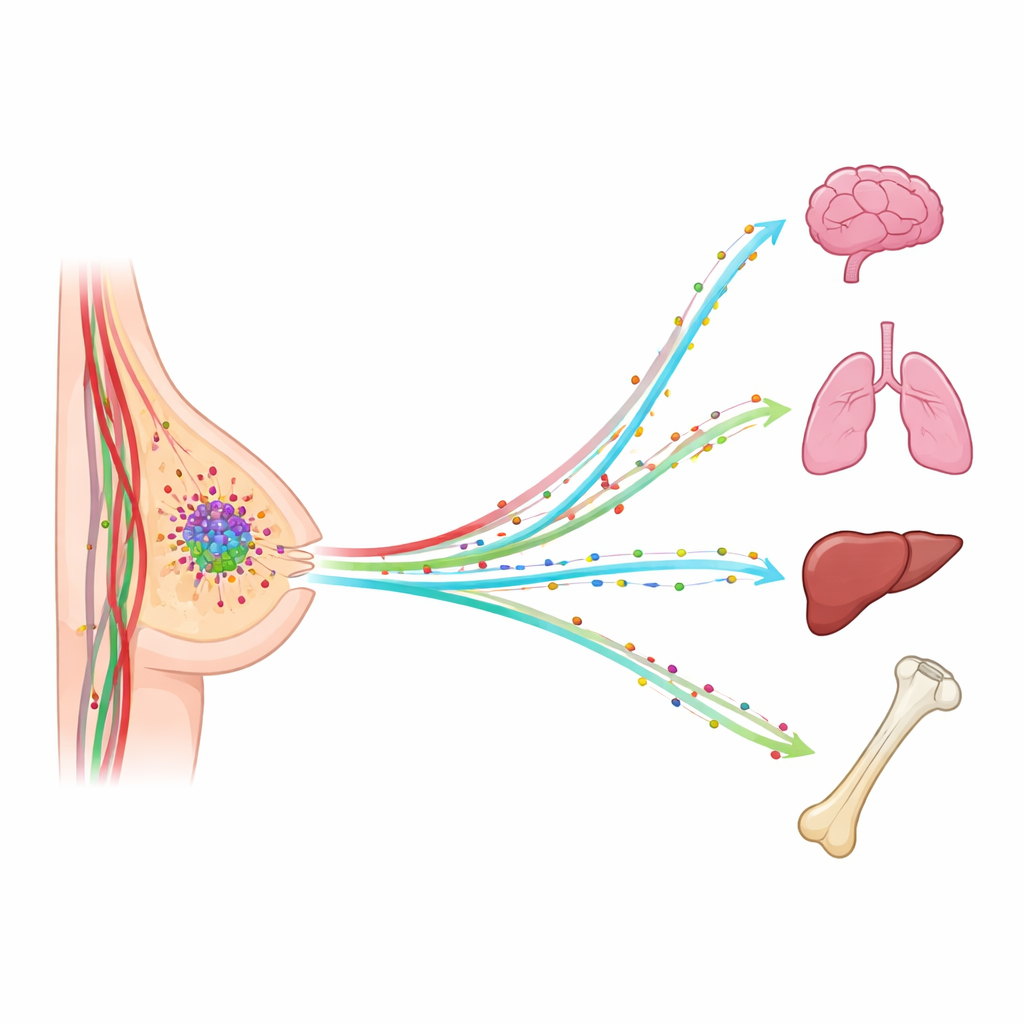
Des signaux invisibles qui orientent les cellules cancéreuses
Notre système immunitaire utilise de petites protéines appelées cytokines et chimiokines comme balises d’orientation, indiquant aux cellules où se déplacer dans le corps. Les tumeurs peuvent détourner ces signaux pour préparer des organes distants et attirer les cellules cancéreuses, un peu comme envoyer des éclaireurs pour installer un camp. L’équipe s’est concentrée sur cinq de ces molécules dans le sang — IL-4, IL-11, CCL2, CCL4 et CXCL12 — car elles influent sur l’inflammation, les réponses immunitaires et la mobilité cellulaire. L’idée était que certains « profils de signaux » pourraient correspondre à des sites métastatiques particuliers, révélant quels organes sont les plus accueillants pour les cellules cancéreuses entrantes.
Ce que les chercheurs ont mesuré chez les patientes
L’étude a suivi 175 femmes atteintes d’un cancer du sein et les a comparées à 50 femmes en bonne santé. Certaines patientes avaient une maladie confinée à la région mammaire, tandis que la plupart avaient un cancer déjà disséminé dans des organes tels que les os, les poumons, le foie ou le cerveau. À l’aide d’un test de laboratoire standard sur des échantillons de sang, les chercheurs ont mesuré la quantité de chacune des cinq molécules en circulation. Ils ont ensuite comparé les niveaux entre patientes et volontaires saines, et entre patientes présentant différentes caractéristiques tumorales, réponses au traitement et sites de métastases.
Des signaux différents, des destinations différentes
Le sang des patientes atteintes d’un cancer du sein montrait des niveaux plus élevés d’IL-4, de CXCL12 et de CCL4 que celui des femmes en bonne santé, suggérant un environnement de signalisation globalement « pro-métastatique ». Au-delà de cela, des schémas spécifiques sont apparus. Des taux plus élevés d’IL-11 étaient associés à des métastases pulmonaires. Des niveaux accrus d’IL-4 et de CXCL12 étaient liés au cancer ayant atteint le cerveau, en particulier dans les tumeurs dépourvues de récepteurs hormonaux ou présentant un excès de HER2, une protéine favorisant la croissance. Les métastases osseuses étaient associées à une augmentation de CCL2 et CCL4, tandis qu’un CCL2 élevé marquait également l’atteinte hépatique. Des tests statistiques ont montré que ces marqueurs pouvaient modérément distinguer les patientes avec métastases cérébrales, pulmonaires ou hépatiques de celles sans, suggérant un rôle potentiel en diagnostic ou en stratification du risque. 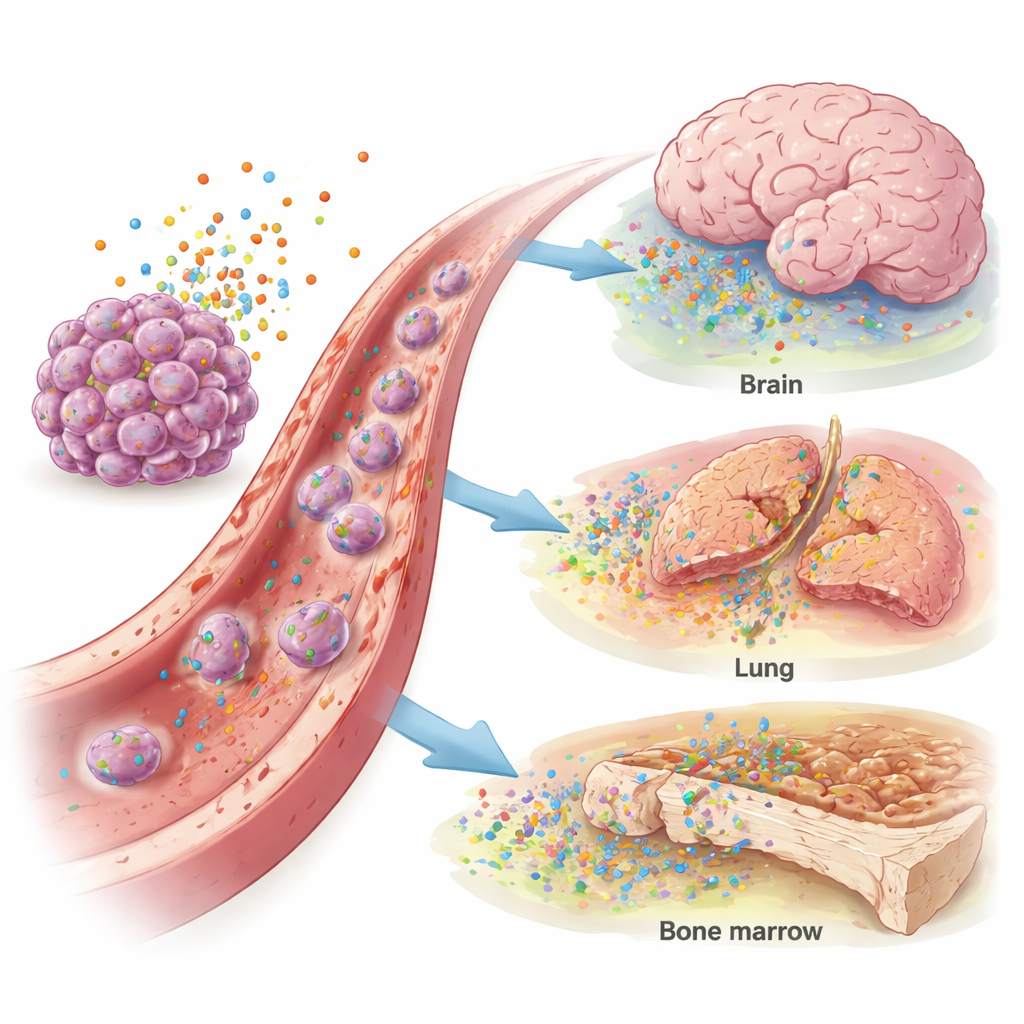
Indices sur le pronostic et la réponse au traitement
Les patientes dont les tumeurs étaient dépourvues de récepteurs aux œstrogènes, ainsi que celles présentant des métastases au cerveau ou au foie, avaient tendance à présenter des périodes sans récidive plus courtes, soulignant comment certains traits biologiques et sites métastatiques s’accompagnent d’un pronostic plus défavorable. De manière surprenante, les niveaux globaux des cinq molécules mesurées n’ont pas clairement prédit la durée de survie sans maladie, mais des taux plus élevés de CCL2 et de CXCL12 étaient liés à une dissémination plus lointaine et à une moins bonne réponse au traitement. Cela suggère que, bien que ces signaux ne soient pas des tests pronostiques simples et autonomes, ils participent profondément aux mécanismes de croissance tumorale, de résistance thérapeutique et de colonisation d’organes spécifiques.
Ce que cela signifie pour les patientes et les soins futurs
Pour les personnes vivant avec un cancer du sein, le message de l’étude est que la métastase peut être en partie guidée par des motifs chimiques reconnaissables plutôt que purement aléatoire. L’IL-4 et le CXCL12 semblaient signaler un risque accru de dissémination au cerveau, l’IL-11 aux poumons, et CCL2 et CCL4 aux os et au foie. Ces résultats, bien qu’établis sur un groupe de patientes unique de taille modérée et dans le cadre d’une étude observationnelle, fournissent une feuille de route pour la recherche future. Si ces observations sont confirmées et affinées, de tels marqueurs sanguins pourraient aider les médecins à estimer où les métastases sont le plus susceptibles d’apparaître, surveiller de plus près les patientes à haut risque et, en dernière instance, concevoir des médicaments qui perturbent ces « indices d’orientation » pour empêcher le cancer de trouver de nouveaux refuges.
Citation: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Mots-clés: métastases du cancer du sein, chimiokines, cytokines, biomarqueurs, microenvironnement tumoral