Clear Sky Science · es
El posible papel directivo de las quimiocinas en la elección de sitios metastásicos específicos en el cáncer de mama
Cómo las células cancerosas eligen su próximo hogar
Cuando el cáncer de mama se disemina, rara vez lo hace al azar. Las células tumorales con frecuencia aparecen en los pulmones, el hígado, los huesos o el cerebro, y esos nuevos crecimientos son los que más amenazan la vida de la paciente. Este estudio plantea una pregunta simple pero potente: ¿y si «aromas» químicos invisibles en el torrente sanguíneo ayudan a guiar a las células cancerosas errantes hacia órganos concretos? Al seguir un pequeño grupo de estas moléculas señalizadoras en la sangre de pacientes, los investigadores buscaron patrones que pudieran explicar —y que algún día pudieran ayudar a predecir o bloquear— adónde viajará el cáncer de mama a continuación. 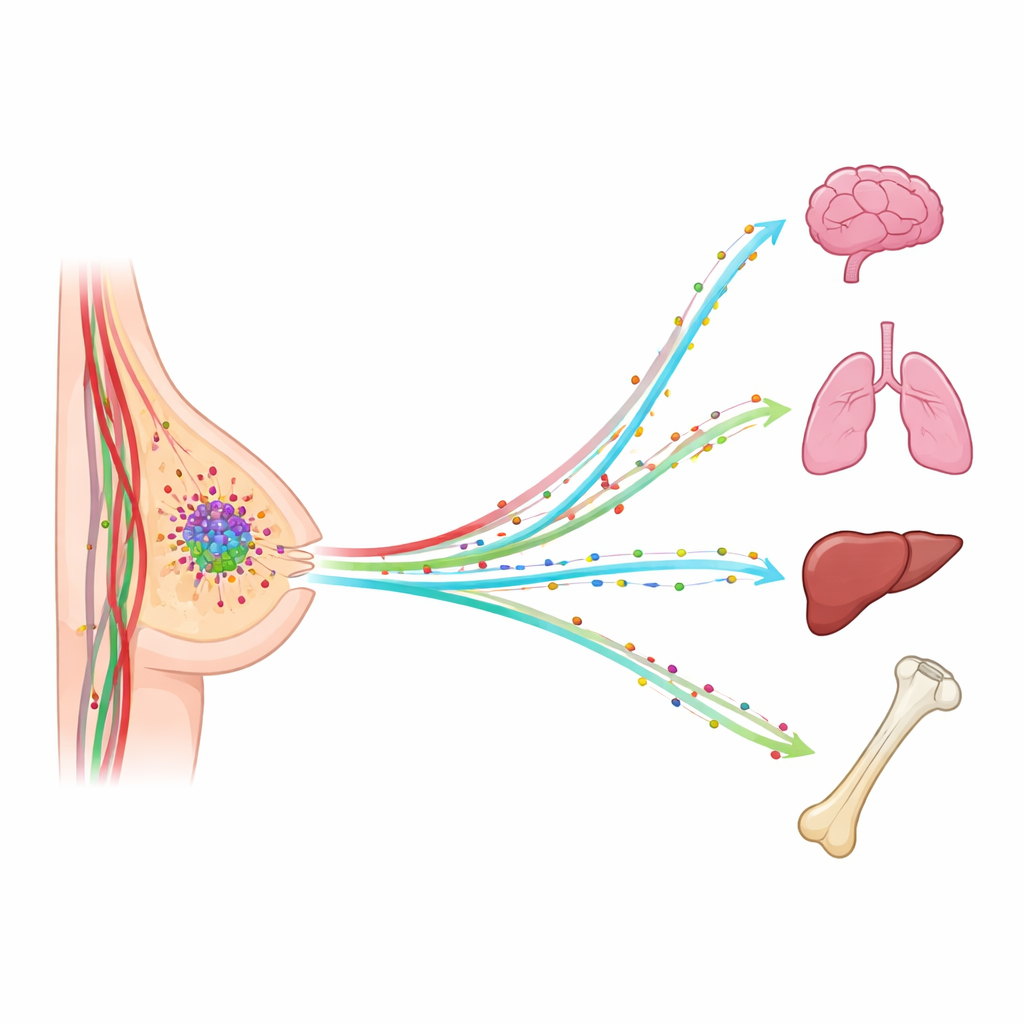
Señales invisibles que orientan a las células cancerosas
Nuestro sistema inmunitario utiliza pequeñas proteínas llamadas citoquinas y quimiocinas como balizas de localización, indicando a las células hacia dónde moverse en el cuerpo. Los tumores pueden secuestrar estas señales para preparar órganos distantes y atraer células cancerosas, como si enviaran exploradores para preparar el terreno. Este equipo se centró en cinco de esas moléculas en la sangre —IL-4, IL-11, CCL2, CCL4 y CXCL12— porque se sabe que influyen en la inflamación, las respuestas inmunitarias y el movimiento celular. La idea era que ciertos «perfiles de señalización» pudieran corresponder a sitios metastásicos particulares, revelando qué órganos son más acogedores para las células cancerosas entrantes.
Qué midieron los investigadores en las pacientes
El estudio siguió a 175 mujeres con cáncer de mama y las comparó con 50 mujeres sanas. Algunas pacientes tenían la enfermedad confinada a la mama, mientras que la mayoría tenía cáncer que ya se había diseminado a órganos como hueso, pulmón, hígado o cerebro. Mediante una prueba de laboratorio estándar en muestras de sangre, los investigadores midieron cuánto de cada una de las cinco moléculas circulaba. Luego compararon los niveles entre pacientes y voluntarias sanas, y entre pacientes con diferentes características tumorales, respuestas al tratamiento y sitios de metástasis.
Diferentes señales, diferentes destinos
La sangre de las pacientes con cáncer de mama mostró niveles más altos de IL-4, CXCL12 y CCL4 que la de las mujeres sanas, lo que sugiere un entorno señalizador global «prometastásico». Además, surgieron patrones específicos. Niveles más altos de IL-11 se asociaron con metástasis en los pulmones. IL-4 elevado y CXCL12 se relacionaron con cáncer que había alcanzado el cerebro, sobre todo en tumores que carecían de receptores hormonales o que tenían exceso de HER2, una proteína promotora del crecimiento. Las metástasis óseas se asociaron con un aumento de CCL2 y CCL4, mientras que CCL2 elevada también marcó afectación hepática. Las pruebas estadísticas mostraron que estos marcadores podían diferenciar de forma moderada a las pacientes con metástasis en cerebro, pulmón o hígado de aquellas sin ellas, lo que apunta a un papel potencial en el diagnóstico o la estratificación del riesgo. 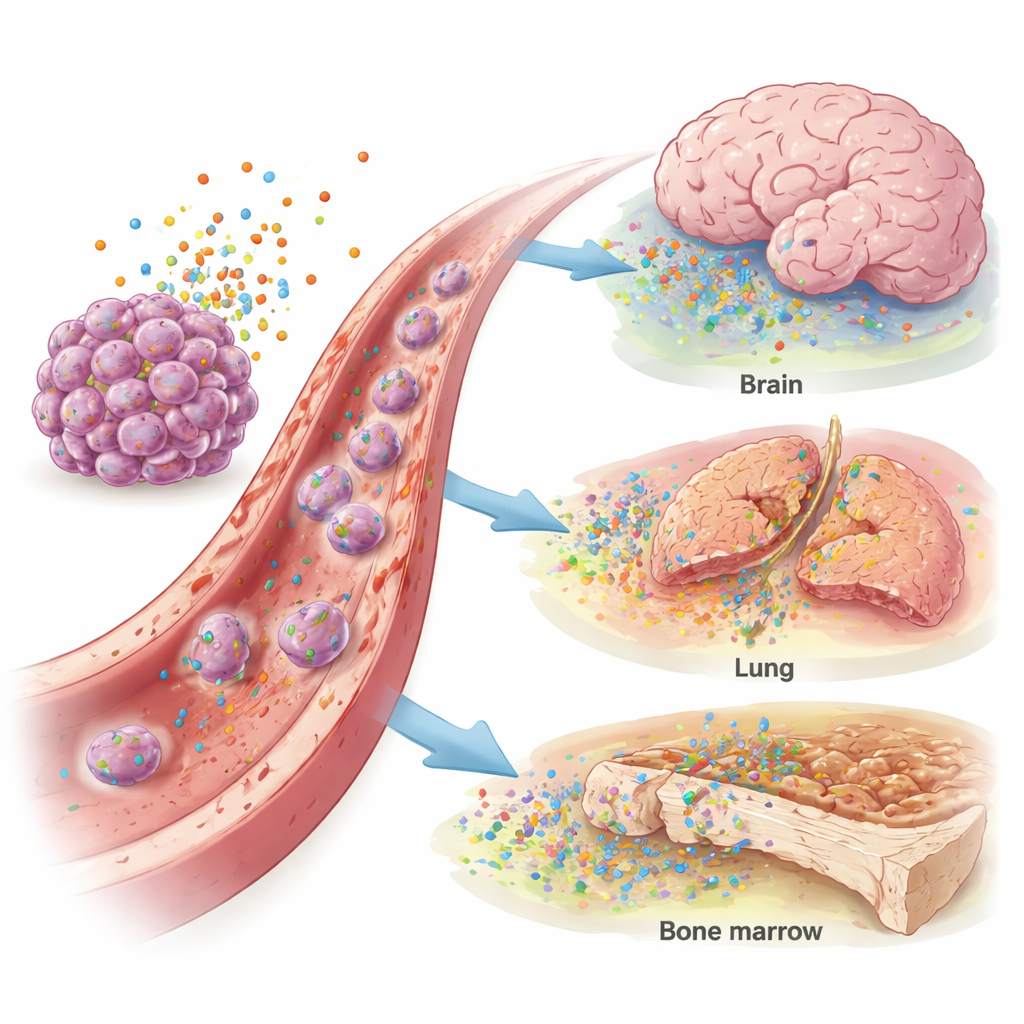
Pistas sobre pronóstico y respuesta al tratamiento
Las pacientes cuyos tumores carecían de receptores de estrógeno, y aquellas con diseminación al cerebro o al hígado, tendieron a tener períodos más cortos sin recurrencia de la enfermedad, lo que destaca cómo ciertos rasgos biológicos y sitios metastásicos van de la mano con un peor pronóstico. Sorprendentemente, los niveles globales de las cinco moléculas medidas por sí solos no predijeron con claridad cuánto tiempo permanecieron libres de enfermedad las pacientes, pero CCL2 y CXCL12 más altos se asociaron con mayor diseminación a distancia y peor respuesta a la terapia. Esto sugiere que, aunque estas señales no sean pruebas pronósticas simples e independientes, participan de forma profunda en cómo los tumores crecen, resisten al tratamiento y colonizan órganos específicos.
Qué significa esto para las pacientes y la atención futura
Para las personas que conviven con cáncer de mama, el mensaje del estudio es que la metástasis puede estar parcialmente guiada por patrones químicos reconocibles en lugar de ser puramente aleatoria. IL-4 y CXCL12 parecieron señalar un mayor riesgo de diseminación al cerebro, IL-11 a los pulmones, y CCL2 y CCL4 a hueso e hígado. Estos hallazgos, aunque se basan en un único grupo de pacientes de tamaño moderado y en un diseño observacional, proporcionan una hoja de ruta para investigaciones futuras. Si se confirman y afinan, tales marcadores en sangre podrían ayudar a los médicos a estimar dónde es más probable que aparezcan metástasis, monitorizar más de cerca a pacientes de alto riesgo y, en última instancia, diseñar fármacos que interrumpan estas «señales de guía» para evitar que el cáncer encuentre nuevos hogares.
Cita: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Palabras clave: metástasis de cáncer de mama, quimiocinas, citoquinas, biomarcadores, microambiente tumoral