Clear Sky Science · pl
Potencjalna rola kierunkowa chemokin dla specyficznych miejsc przerzutów w raku piersi
Jak komórki nowotworowe wybierają swoje kolejne miejsce
Gdy rak piersi się rozprzestrzenia, rzadko bywa to przypadkowe. Komórki nowotworowe często pojawiają się w płucach, wątrobie, kościach lub mózgu, a to właśnie te nowe ogniska najbardziej zagrażają życiu pacjentki. Badanie stawia proste, lecz istotne pytanie: co jeśli niewidzialne chemiczne „zapachy” we krwi pomagają kierować wędrującymi komórkami nowotworowymi do konkretnych narządów? Śledząc niewielką grupę tych molekuł sygnałowych we krwi pacjentek, badacze szukali wzorców, które mogłyby wyjaśnić — i być może w przyszłości pomóc przewidzieć lub zablokować — dokąd rak piersi uda się następnie. 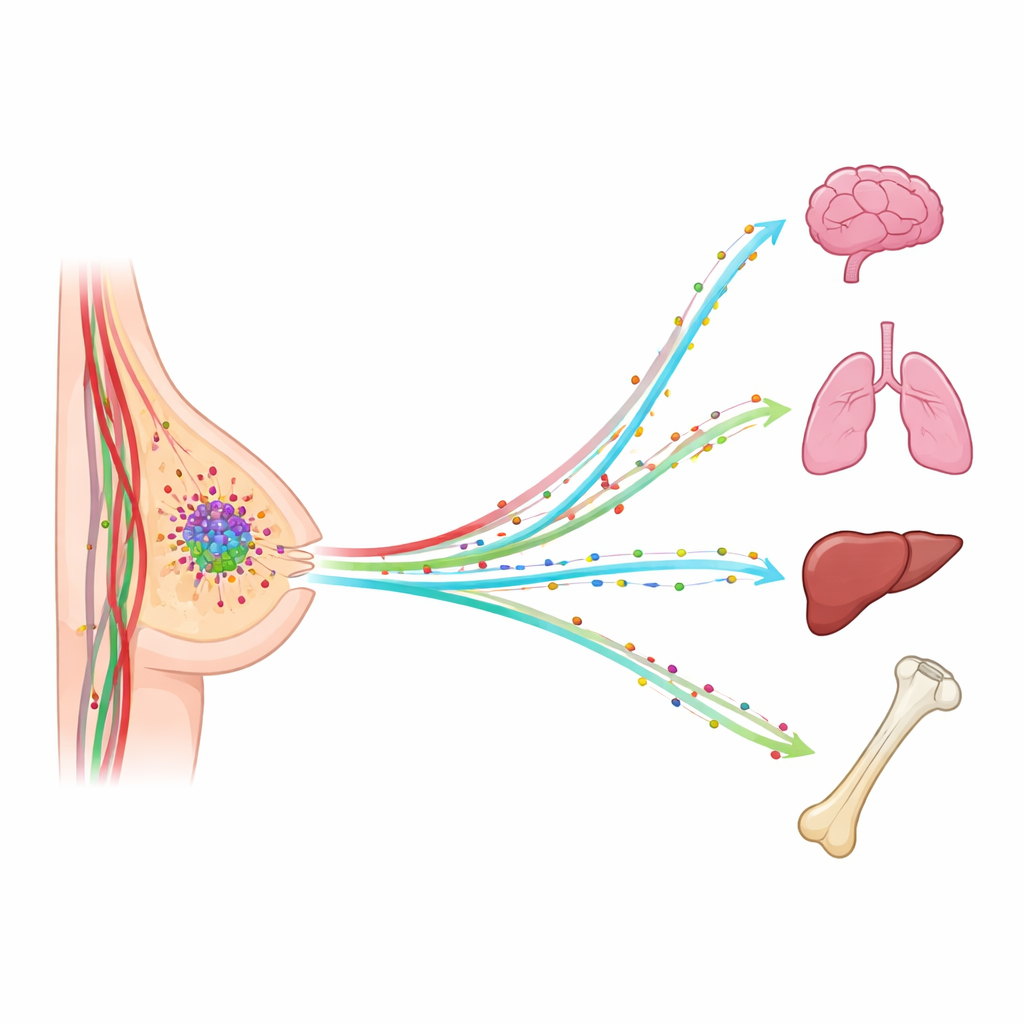
Niewidzialne sygnały kierujące komórkami raka
Nasz układ odpornościowy wykorzystuje małe białka zwane cytokinami i chemokinami jako sygnały nawigacyjne, wskazujące komórkom, gdzie mają się przemieszczać w organizmie. Guzy potrafią przejąć te sygnały, przygotowując odległe narządy i przyciągając komórki nowotworowe — trochę jak wysyłanie zwiadowców, którzy wcześniej zajmują teren. Zespół skupił się na pięciu takich molekułach we krwi — IL-4, IL-11, CCL2, CCL4 i CXCL12 — ponieważ wiadomo, że wpływają na zapalenie, odpowiedzi immunologiczne i ruch komórek. Zakładano, że pewne „profile sygnałowe” mogą odpowiadać konkretnym miejscom przerzutów, ujawniając, które narządy są bardziej gościnne dla napływających komórek raka.
Co mierzyli badacze u pacjentek
Badanie objęło 175 kobiet z rakiem piersi i porównało je z 50 zdrowymi kobietami. Część pacjentek miała chorobę ograniczoną do piersi, podczas gdy u większości rak już rozprzestrzenił się do narządów takich jak kości, płuca, wątroba lub mózg. Za pomocą standardowego testu laboratoryjnego na próbkach krwi zmierzono poziomy każdej z pięciu molekuł we krwiobiegu. Następnie porównano ich stężenia między pacjentkami a zdrowymi ochotniczkami oraz wśród pacjentek o różnych cechach guza, odpowiedzi na leczenie i miejscach przerzutów.
Różne sygnały, różne cele
Krew pacjentek z rakiem piersi wykazywała wyższe poziomy IL-4, CXCL12 i CCL4 niż krew zdrowych kobiet, co sugeruje ogólnie „pro-przerzutowe” środowisko sygnałowe. Pojawiły się też bardziej specyficzne wzorce. Wyższe stężenia IL-11 wiązały się z przerzutami do płuc. Podwyższony IL-4 i CXCL12 korelowały z przerzutami do mózgu, zwłaszcza w guzach pozbawionych receptorów hormonalnych lub z nadmiarem HER2 — białka wspomagającego wzrost. Przerzuty do kości powiązano ze zwiększonymi CCL2 i CCL4, natomiast podwyższony CCL2 oznaczał także zajęcie wątroby. Testy statystyczne wykazały, że te markery mogły ze średnią dokładnością odróżniać pacjentki z przerzutami do mózgu, płuc lub wątroby od tych bez nich, co sugeruje ich potencjalną rolę w diagnostyce lub stratifikacji ryzyka. 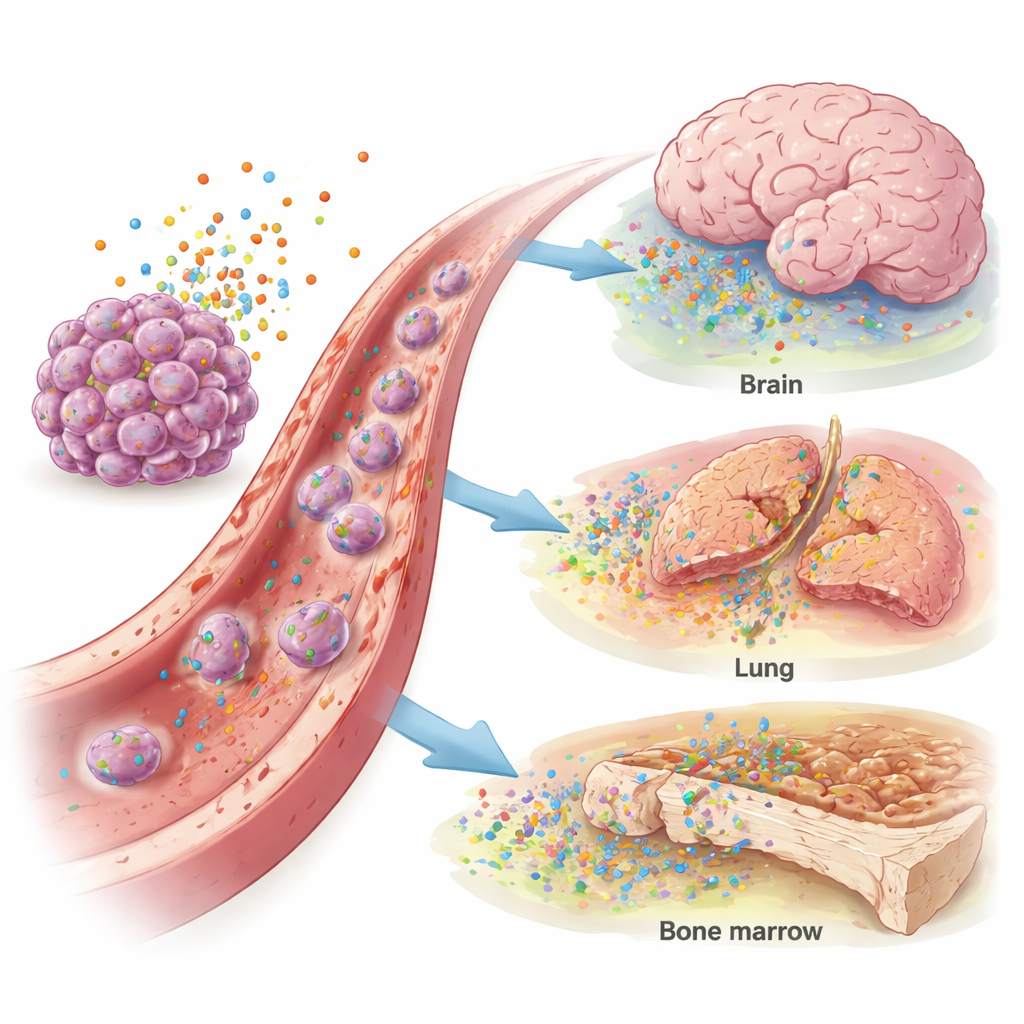
Wskazówki dotyczące rokowania i odpowiedzi na leczenie
Pacjentki, których guzy nie miały receptorów estrogenowych, oraz te z przerzutami do mózgu lub wątroby, miały zwykle krótsze okresy wolne od nawrotu choroby, co podkreśla, że niektóre cechy biologiczne i miejsca przerzutów idą w parze z gorszym rokowaniem. Zaskakująco, same ogólne poziomy pięciu mierzonych molekuł nie przewidywały wyraźnie czasu pozostawania bez choroby, ale wyższe CCL2 i CXCL12 wiązały się z większym odległym rozsiewem i gorszą odpowiedzią na terapię. To sugeruje, że choć te sygnały nie są prostymi, pojedynczymi testami prognostycznymi, są głęboko zaangażowane w to, jak guzy rosną, opierają się leczeniu i kolonizują określone narządy.
Co to oznacza dla pacjentek i przyszłej opieki
Dla osób żyjących z rakiem piersi przesłanie badania jest takie, że przerzuty mogą być częściowo kierowane rozpoznawalnymi wzorcami chemicznymi, a nie być całkowicie losowe. IL-4 i CXCL12 wydawały się wskazywać na większe ryzyko rozprzestrzenienia do mózgu, IL-11 do płuc, a CCL2 i CCL4 do kości i wątroby. Wyniki te, choć oparte na jednej, umiarkowanie licnej grupie pacjentek i badaniu obserwacyjnym, dostarczają mapy drogowej dla przyszłych badań. Jeśli zostaną potwierdzone i dopracowane, takie markery we krwi mogłyby pomóc lekarzom oszacować, gdzie przerzuty najprawdopodobniej się pojawią, baczniej monitorować pacjentki o wysokim ryzyku i ostatecznie projektować leki zakłócające te „wskazówki nawigacyjne”, by uniemożliwić rakowi znalezienie nowych domów.
Cytowanie: Ayoub, A.M., EL-Houseini, M.E., Tharwat, E. et al. The potential directing role of chemokines for specific metastatic sites in breast cancer. Sci Rep 16, 12015 (2026). https://doi.org/10.1038/s41598-026-45036-9
Słowa kluczowe: przerzuty raka piersi, chemokiny, cytokiny, biomarkery, mikrośrodowisko guza