Clear Sky Science · sv
En parallell UNet som integrerar KAN och mamba för medicinsk bildsegmentering
Varför detta är viktigt för patienter och läkare
Bakom varje cancerscreening eller ultraljudsbild finns ett avgörande steg: att lära datorer att markera var en förändring eller ett organ faktiskt ligger. Denna process, kallad segmentering, hjälper läkare att mäta tumörer, följa sjukdomsförlopp och planera behandling. Artikeln presenterar KMP‑UNet, ett nytt, kompakt bildanalysnätverk som lovar att spåra dessa gränser mer noggrant och effektivt, och som därigenom kan göra automatiserad medicinsk bildavläsning mer tillförlitlig och lättare att implementera i verklig klinisk miljö.
Att se helheten i en medicinsk bild
Moderna medicinska bilder är stora och komplexa: viktiga ledtrådar kan vara utspridda över stora områden, samtidigt som själva förändringen kan ha otydliga eller oregelbundna kanter. Traditionella konvolutionella neurala nätverk, inklusive den populära UNet-familjen, är bra på att upptäcka lokala mönster men har svårigheter att koppla ihop avlägsna regioner i en bild. Transformermodeller kan betrakta hela bilden samtidigt men tenderar att vara tunga och långsamma, vilket är problematiskt för högupplöst kliniskt material och begränsad hårdvara på sjukhus. Författarna bygger vidare på en nyare familj sekvensmodeller, så kallade state space-modeller, och en ny nätverksstil känd som Kolmogorov–Arnold-nätverk, för att fånga både bred kontext och subtila detaljer utan att beräkningskostnaden exploderar.
Två hjärnsmarta specialister som arbetar sida vid sida
KMP‑UNet behåller den välkända U-formade encoder–decoder-strukturen hos UNet men ändrar vad som händer inuti. I stället för att förlita sig på en enda bearbetningstyp kör den två parallella grenar genom nätverket. Den ena grenen bygger på en modell kallad Mamba, som är utmärkt på att hantera långa sekvenser och här anpassas för att svepa över bilden. Denna gren samlar effektivt långtäckande kontext och hjälper nätverket att förstå hur avlägsna regioner relaterar till varandra. Den andra grenen använder Kolmogorov–Arnold-nätverk, som ersätter fasta aktiveringsfunktioner med flexibla, lärbara kurvor. Det ger modellen extra kapacitet att representera svåra, icke‑linjära mönster, såsom subtila intensitetsförändringar vid kanten av en hudförändring eller en polyp.
Intelligenta sammanslagningar av egenskaper och klarare gränser
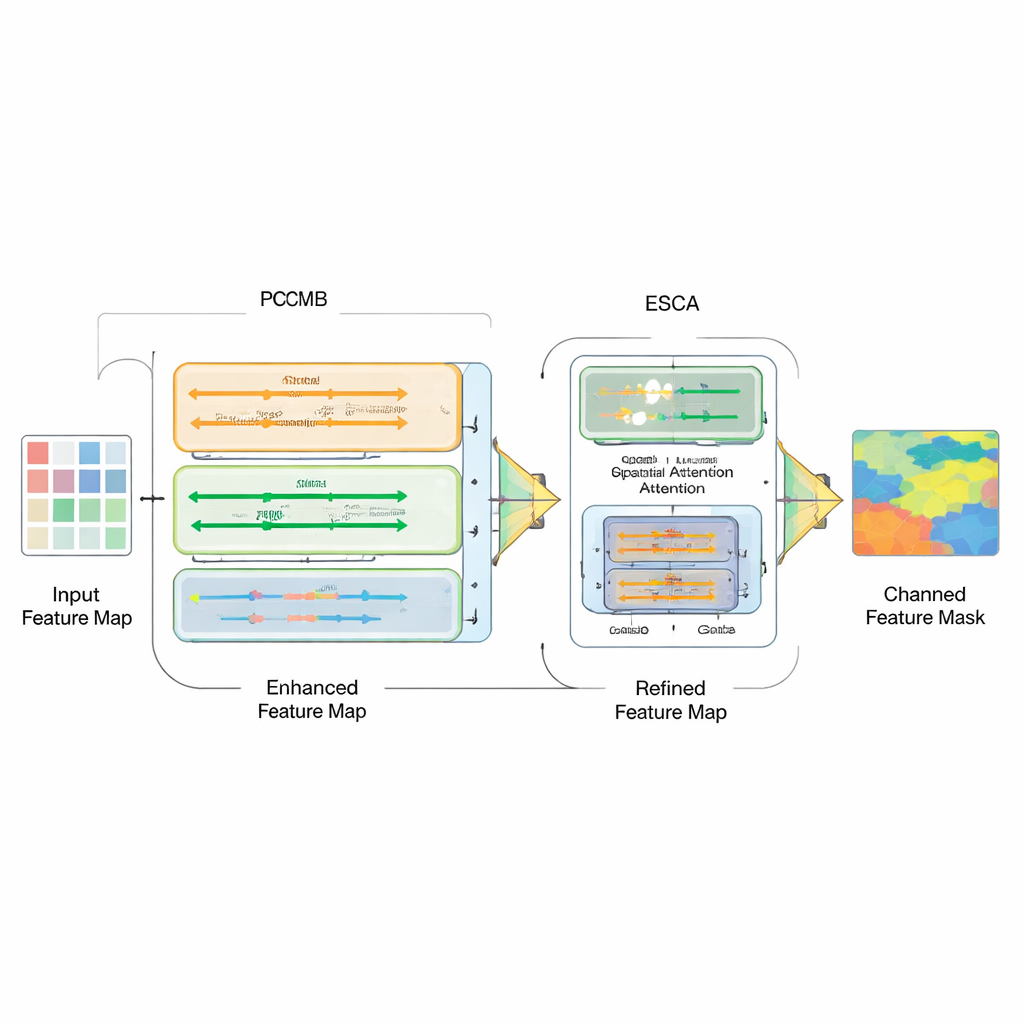
Att bara sätta ihop olika modeltyper räcker inte; den verkliga utmaningen är hur man kombinerar deras styrkor. För detta introducerar författarna en Parallel Convolution Mamba Block (PCMB), som delar upp funktioner i grupper och bearbetar dem genom flera lätta Mamba‑baserade och konvolutionella vägar innan de slås ihop igen. Denna design balanserar global kontext och fina detaljer samtidigt som beräkningskostnaden hålls låg. De omarbetar också skip‑kopplingarna som förbinder encoder och decoder. En ny Enhanced Spatial‑Channel Attention (ESCA)-modul betonar selektivt viktiga positioner och feature‑kanaler, samtidigt som användbar information bevaras via residualkopplingar. Detta gör nätverket mindre benäget att bli förvirrat av distraktioner som hår, reflexer eller brusiga texturer runt en förändring.
Hur bra fungerar den nya metoden?
Teamet utvärderar KMP‑UNet på fyra publika dataset som täcker hudförändringar, kolonpolyper och bröstultraljudsbilder, och testar också överföring till ett annat huddataset. Över dessa benchmarkresultat matchar eller överträffar modellen konsekvent en rad starka baslinjer, inklusive klassiska UNet-varianter, transformerbaserade konstruktioner och andra nyare nätverk förstärkta med Mamba och KAN. Till exempel når KMP‑UNet på det välanvända huddatasetet ISIC2018 hög Dice‑score och noggrannhet samtidigt som den använder ungefär en miljon parametrar—betydligt färre än många konkurrenter. Detaljerade experiment visar att varje komponent—Mamba‑baserad kontextmodellering, KAN‑baserad icke‑linjär förfining och ESCA‑baserad skip‑förfining—ger mätbara förbättringar, särskilt vad gäller kantkvalitet och minskning av falska positiva regioner.
Vad detta betyder för framtida medicinska AI‑verktyg
För icke‑specialister är huvudpoängen att KMP‑UNet erbjuder ett mer kompakt men kapabelt sätt att lära datorer att markera förändringar och organ i bilder, genom att låta två kompletterande ”experter” arbeta parallellt och sedan noggrant förena deras insikter. Även om metoden fortfarande har svårigheter med de mest utmanande fallen—mycket oregelbundna former, extremt suddiga gränser eller kraftiga artefakter—utgör den en stark grund för noggrann och effektiv segmentering. Med vidare arbete för att hantera brusiga bakgrunder och för anpassning mellan olika bildcenter kan metoder som KMP‑UNet bidra till att föra pålitlig, snabb bildanalys närmare vardaglig klinisk användning.
Citering: Liu, J., Wu, J., Xu, L. et al. A parallel UNet integrating KAN and mamba for medical image segmentation. Sci Rep 16, 13579 (2026). https://doi.org/10.1038/s41598-026-43127-1
Nyckelord: medicinsk bildsegmentering, deep learning, UNet, state space-modeller, Kolmogorov–Arnold-nätverk