Clear Sky Science · fr
Un UNet parallèle intégrant KAN et mamba pour la segmentation d’images médicales
Pourquoi cela compte pour les patients et les médecins
Derrière chaque examen de dépistage du cancer ou chaque image d’échographie, une étape cruciale consiste à apprendre aux ordinateurs à délimiter où se trouve réellement une lésion ou un organe. Ce processus, appelé segmentation, aide les médecins à mesurer les tumeurs, suivre l’évolution de la maladie et planifier les traitements. L’article présente KMP-UNet, un nouveau type de réseau d’analyse d’images compact qui promet de tracer ces frontières de manière plus précise et efficace, rendant potentiellement la lecture automatisée des images médicales plus fiable et plus facile à déployer en milieu clinique.
Voir l’ensemble d’un examen médical
Les images médicales modernes sont grandes et complexes : des indices importants peuvent être répartis sur une vaste zone, tandis que la lésion elle‑même peut présenter des bords flous ou irréguliers. Les réseaux de neurones convolutifs traditionnels, y compris la famille UNet populaire, sont bons pour repérer des motifs locaux mais ont du mal à relier des régions distantes d’un examen. Les modèles basés sur les Transformers peuvent analyser l’image dans son ensemble mais tendent à être lourds et lents, ce qui pose problème pour des données cliniques à haute résolution et des matériels hospitaliers limités. Les auteurs s’appuient sur une famille plus récente de modèles séquentiels, appelés modèles d’état, et sur un style nouveau de réseau neuronal connu sous le nom de Kolmogorov–Arnold Networks, pour capturer à la fois le contexte global et les détails subtils sans faire exploser le coût de calcul.
Deux spécialistes intelligents travaillant côte à côte
KMP-UNet conserve la disposition en U familière de l’encodeur‑décodeur du UNet mais modifie ce qui se passe à l’intérieur. Au lieu de s’appuyer sur un seul type de traitement, il fait fonctionner deux branches parallèles dans le réseau. Une branche est basée sur un modèle appelé Mamba, qui excelle dans le traitement de longues séquences et est ici adapté pour balayer l’image. Cette branche rassemble efficacement le contexte à longue portée, aidant le réseau à comprendre comment des régions éloignées sont liées entre elles. La seconde branche utilise les Kolmogorov–Arnold Networks, qui remplacent les fonctions d’activation fixes par des courbes flexibles et apprenables. Cela donne au modèle une puissance supplémentaire pour représenter des motifs non linéaires difficiles, tels que des variations subtiles d’intensité le long du bord d’une lésion cutanée ou d’un polype.
Une fusion plus intelligente des caractéristiques et des contours plus nets
Assembler simplement différents types de modèles ne suffit pas ; le vrai défi est de combiner leurs forces. À cette fin, les auteurs introduisent un bloc Parallel Convolution Mamba (PCMB), qui sépare les caractéristiques en groupes et les traite via plusieurs voies légères basées sur Mamba et la convolution avant de les fusionner à nouveau. Cette conception équilibre le contexte global et les détails fins tout en maintenant un coût computationnel faible. Ils revisitent également les connexions de saut qui relient l’encodeur et le décodeur. Un nouveau module Enhanced Spatial-Channel Attention (ESCA) met sélectivement en évidence les emplacements et canaux de caractéristiques importants, tout en préservant l’information utile grâce à des connexions résiduelles. Cela rend le réseau moins susceptible d’être perturbé par des distractions telles que des cheveux, des reflets ou des textures bruyantes autour d’une lésion.
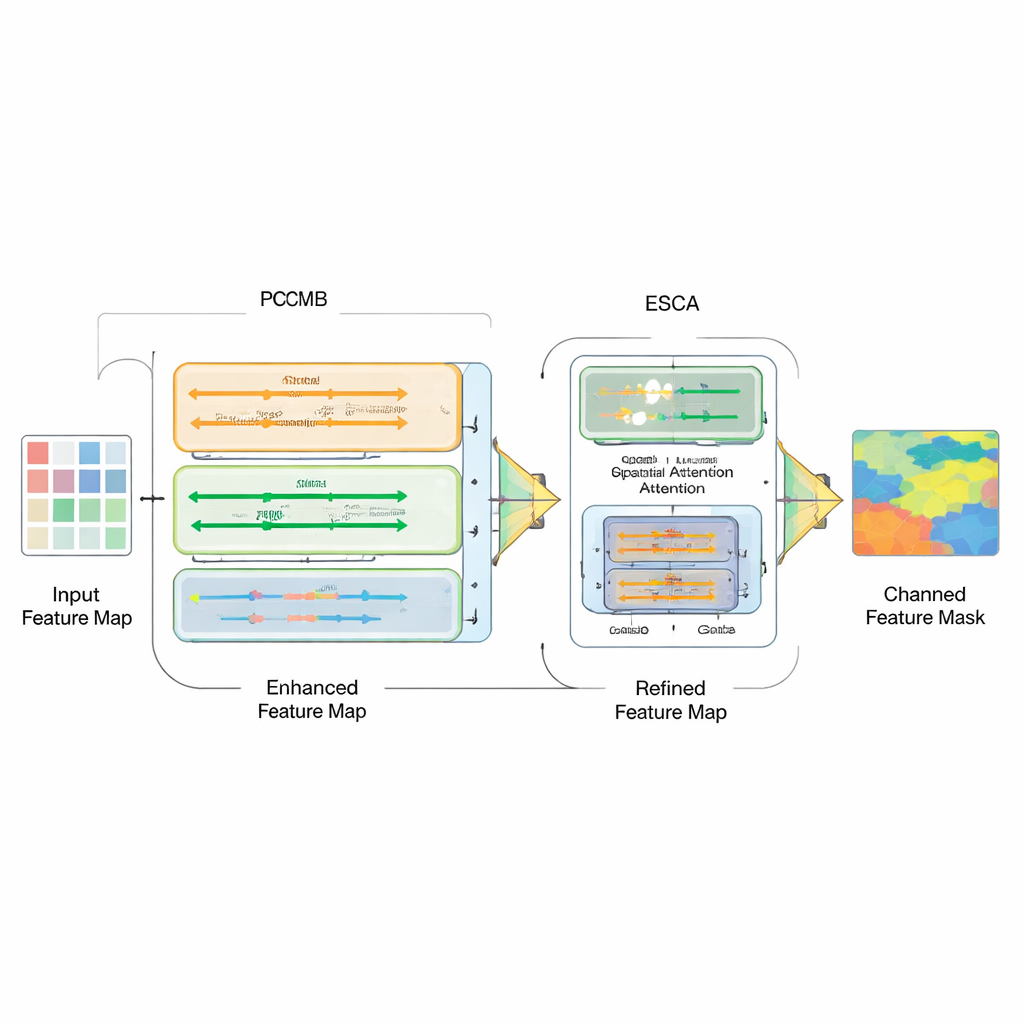
Quelle est l’efficacité de la nouvelle approche ?
L’équipe évalue KMP-UNet sur quatre jeux de données publics couvrant les lésions cutanées, les polypes du côlon et les images d’échographie mammaire, et teste également le transfert vers un autre jeu de données cutané. Sur ces benchmarks, le modèle égalise ou dépasse systématiquement une gamme de solides méthodes de référence, y compris des variantes classiques de UNet, des architectures basées sur Transformer et d’autres réseaux récents enrichis en Mamba et KAN. Par exemple, sur un jeu de données de lésions cutanées largement utilisé (ISIC2018), KMP-UNet atteint un score Dice et une précision élevés tout en utilisant environ un million de paramètres — bien moins que beaucoup de concurrents. Des expériences détaillées montrent que chaque composant — la modélisation du contexte basée sur Mamba, le raffinement non linéaire basé sur KAN et l’amélioration des sauts via ESCA — apporte des gains mesurables, en particulier sur la qualité des contours et la réduction des fausses régions positives.
Ce que cela signifie pour les futurs outils d'IA médicale
Pour les non-spécialistes, la principale conclusion est que KMP-UNet offre une manière plus compacte mais performante d’apprendre aux ordinateurs à délimiter lésions et organes dans les images, en laissant deux « experts » complémentaires travailler en parallèle puis en fusionnant soigneusement leurs apports. Bien que la méthode peine encore sur les cas les plus difficiles — formes très irrégulières, bords extrêmement flous ou artefacts importants — elle constitue une base solide pour une segmentation précise et efficace. Avec des travaux supplémentaires sur la gestion des arrière-plans bruyants et l’adaptation entre centres d’imagerie, des approches comme KMP-UNet pourraient aider à rapprocher une analyse d’images fiable et rapide de la pratique clinique quotidienne.
Citation: Liu, J., Wu, J., Xu, L. et al. A parallel UNet integrating KAN and mamba for medical image segmentation. Sci Rep 16, 13579 (2026). https://doi.org/10.1038/s41598-026-43127-1
Mots-clés: segmentation d'images médicales, apprentissage profond, UNet, modèles d'état, réseaux de Kolmogorov–Arnold