Clear Sky Science · de
Ein paralleler UNet, der KAN und Mamba für die medizinische Bildsegmentierung integriert
Warum das für Patientinnen, Patienten und Ärztinnen sowie Ärzte wichtig ist
Hinter jedem Screening-Scan oder Ultraschallbild steht ein entscheidender Schritt: Computern beizubringen, wo genau eine Läsion oder ein Organ liegt. Dieser Vorgang, Segmentierung genannt, hilft Ärzten, Tumore zu vermessen, den Krankheitsverlauf zu verfolgen und Behandlungen zu planen. Die Arbeit stellt KMP-UNet vor, ein neues, kompaktes Bildanalyse-Netzwerk, das verspricht, diese Grenzen genauer und effizienter nachzuzeichnen und damit automatisierte Auswertungen medizinischer Bilder zuverlässiger und leichter in der Praxis einsetzbar zu machen.
Das Gesamtbild in einem medizinischen Scan erfassen
Moderne medizinische Bilder sind groß und komplex: Wichtige Hinweise können über weite Bereiche verteilt sein, während die Läsion selbst unscharfe oder unregelmäßige Ränder haben kann. Traditionelle Faltungsnetzwerke, einschließlich der beliebten UNet-Familie, sind gut darin, lokale Muster zu erkennen, tun sich aber schwer damit, weit entfernte Regionen eines Scans zu verknüpfen. Transformer-basierte Modelle können das ganze Bild auf einmal erfassen, sind jedoch oft rechenintensiv und langsam — problematisch für hochauflösende klinische Daten und begrenzte Krankenhaus-Hardware. Die Autoren bauen auf einer neueren Familie von Sequenzmodellen auf, den Zustandsraummodellen, sowie auf einem frischen Netzwerkkonzept, den Kolmogorov–Arnold-Netzwerken, um sowohl breiten Kontext als auch feine Details zu erfassen, ohne die Rechenkosten stark anwachsen zu lassen.
Zwei kluge Spezialisten, die nebeneinander arbeiten
KMP-UNet behält die vertraute U-förmige Encoder–Decoder-Anordnung des UNet bei, verändert aber die internen Verarbeitungsschritte. Statt sich auf einen einzigen Verarbeitungstyp zu stützen, laufen zwei parallele Zweige durch das Netzwerk. Ein Zweig basiert auf einem Modell namens Mamba, das besonders gut mit langen Sequenzen umgehen kann und hier so angepasst wurde, dass es das Bild durchscannt. Dieser Zweig sammelt effizient langreichweitigen Kontext und hilft dem Netzwerk zu verstehen, wie weit auseinanderliegende Bereiche zueinander in Beziehung stehen. Der zweite Zweig nutzt Kolmogorov–Arnold-Netzwerke, die feste Aktivierungsfunktionen durch flexible, lernbare Kurven ersetzen. Das verleiht dem Modell zusätzliche Kapazität, schwierige nichtlineare Muster abzubilden, etwa subtile Intensitätsänderungen entlang der Kante einer Hautläsion oder eines Polypen.
Intelligentere Fusion von Merkmalen und klarere Ränder
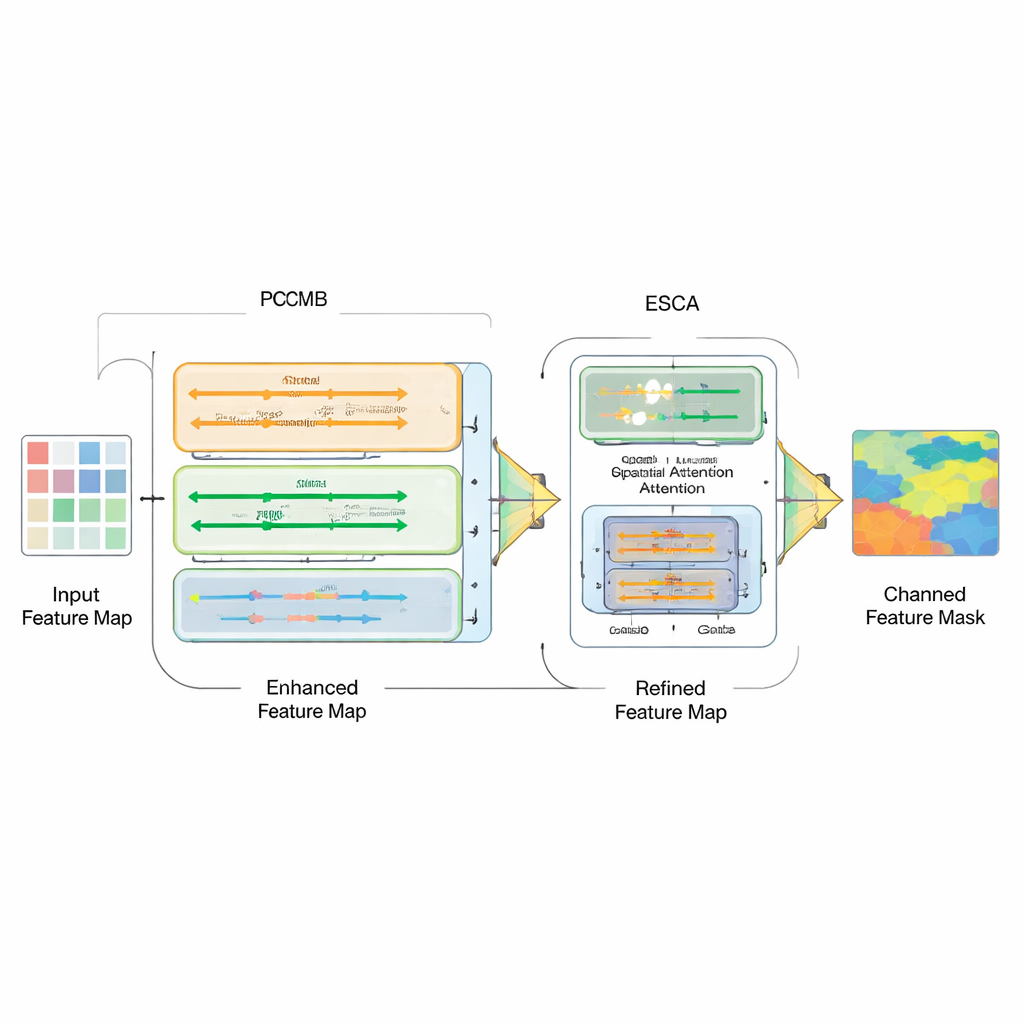
Verschiedene Modelltypen einfach zusammenzuschalten reicht nicht aus; die eigentliche Herausforderung besteht darin, ihre Stärken sinnvoll zu kombinieren. Dazu führen die Autoren einen Parallel Convolution Mamba Block (PCMB) ein, der Merkmale in Gruppen aufteilt und sie durch mehrere leichte, auf Mamba basierende und konvolutionale Pfade verarbeitet, bevor er sie wieder zusammenführt. Dieses Design balanciert globalen Kontext und feine Details aus, bei geringem Rechenaufwand. Zudem überarbeiten sie die Skip-Verbindungen, die Encoder und Decoder koppeln. Ein neues Enhanced Spatial-Channel Attention (ESCA)-Modul betont selektiv wichtige Orte und Merkmal-Kanäle, während nützliche Informationen über Residualverbindungen erhalten bleiben. Dadurch wird das Netzwerk weniger anfällig für Störfaktoren wie Haare, Reflexionen oder verrauschte Texturen rund um eine Läsion.
Wie gut funktioniert der neue Ansatz?
Das Team bewertet KMP-UNet auf vier öffentlichen Datensätzen zu Hautläsionen, Darmpolypen und Brustultraschallbildern und prüft zudem die Übertragbarkeit auf einen weiteren Hautdatensatz. Über diese Benchmarks hinweg erreicht das Modell durchgehend Ergebnisse, die mit einer Reihe starker Baselines mithalten oder diese übertreffen — darunter klassische UNet-Varianten, Transformer-basierte Entwürfe und andere kürzlich vorgestellte Mamba- und KAN-verstärkte Netzwerke. Beispielsweise erzielt KMP-UNet auf einem weit verbreiteten Hautläsionsdatensatz (ISIC2018) eine hohe Dice-Kennzahl und Genauigkeit bei nur etwa einer Million Parametern — deutlich weniger als viele Konkurrenten. Detaillierte Experimente zeigen, dass jede Komponente — Mamba-basierte Kontextmodellierung, KAN-basierte nichtlineare Verfeinerung und ESCA-basierte Skip-Verfeinerung — messbare Verbesserungen beiträgt, insbesondere bei der Randqualität und der Verringerung falsch positiver Regionen.
Was das für zukünftige medizinische KI‑Werkzeuge bedeutet
Für Nicht‑Spezialisten lautet die zentrale Erkenntnis: KMP-UNet bietet einen kompakteren, dennoch leistungsfähigen Weg, Computern beizubringen, Läsionen und Organe in Bildern zu umreißen, indem zwei komplementäre „Expertinnen/Experten“ parallel arbeiten und ihre Einsichten sorgfältig fusioniert werden. Zwar hat die Methode weiterhin Schwierigkeiten mit den extremsten Fällen — sehr unregelmäßigen Formen, stark verschwommenen Grenzen oder schweren Artefakten —, doch sie bietet eine solide Grundlage für genaue, effiziente Segmentierung. Mit weiterer Arbeit an der Behandlung verrauschter Hintergründe und der Anpassung zwischen Bildgebungszentren könnten Ansätze wie KMP-UNet zuverlässige, schnelle Bildanalysen näher an den klinischen Alltag bringen.
Zitation: Liu, J., Wu, J., Xu, L. et al. A parallel UNet integrating KAN and mamba for medical image segmentation. Sci Rep 16, 13579 (2026). https://doi.org/10.1038/s41598-026-43127-1
Schlüsselwörter: medizinische Bildsegmentierung, deep learning, UNet, Zustandsraummodelle, Kolmogorov–Arnold-Netzwerke