Clear Sky Science · nl
Een parallelle UNet die KAN en mamba integreert voor medisch beeldsegmentatie
Waarom dit belangrijk is voor patiënten en artsen
Achter elke kanker-screeningsscan of echografische afbeelding gaat een cruciale stap schuil: het leren van computers om precies aan te geven waar een laesie of orgaan zich bevindt. Dit proces, segmentatie genoemd, helpt artsen bij het meten van tumoren, het volgen van ziekte en het plannen van behandelingen. Het artikel introduceert KMP-UNet, een nieuw soort compact beeldanalyse-netwerk dat belooft deze grenzen nauwkeuriger en efficiënter te bepalen, wat geautomatiseerde interpretatie van medische beelden betrouwbaarder en eenvoudiger inzetbaar in echte klinische omgevingen kan maken.
Het hele beeld zien in een medische scan
Moderne medische beelden zijn groot en complex: belangrijke aanwijzingen kunnen zich over een breed gebied verspreiden, terwijl de laesie zelf vage of onregelmatige randen kan hebben. Traditionele convolutionele neurale netwerken, waaronder de populaire UNet-familie, zijn goed in het herkennen van lokale patronen maar hebben moeite om verre regio’s in een scan met elkaar te verbinden. Transformer-gebaseerde modellen kunnen het hele beeld tegelijk bekijken, maar zijn vaak zwaar en traag, wat problematisch is voor hoge-resolutie klinische data en beperkte ziekenhuishardware. De auteurs bouwen voort op een nieuwere familie sequentiemodellen, genaamd statusruimte-modellen, en een frisse stijl van neurale netwerken bekend als Kolmogorov–Arnold-netwerken, om zowel ruime context als subtiele details vast te leggen zonder dat de rekenkosten exploderen.
Twee slimme specialisten werken zij aan zij
KMP-UNet behoudt de vertrouwde U-vormige encoder–decoder-indeling van UNet maar verandert wat er binnenin gebeurt. In plaats van te vertrouwen op één type verwerking, laat het twee parallelle takken door het netwerk lopen. De ene tak is gebaseerd op een model genaamd Mamba, dat uitstekend is in het verwerken van lange reeksen en hier wordt aangepast om over het beeld te scannen. Deze tak verzamelt efficiënt context op lange afstand, wat het netwerk helpt te begrijpen hoe ver uit elkaar liggende regio’s zich tot elkaar verhouden. De tweede tak gebruikt Kolmogorov–Arnold-netwerken, die vaste activatiefuncties vervangen door flexibele, leerbare krommen. Dat geeft het model extra vermogen om lastige, niet-lineaire patronen te modelleren, zoals subtiele intensiteitsveranderingen langs de rand van een huidlaesie of poliep.
Slimmere fusie van kenmerken en duidelijkere randen
Het is niet genoeg om simpelweg verschillende modeltypen aan elkaar te koppelen; de echte uitdaging is hoe je hun krachten combineert. Daarom introduceren de auteurs een Parallel Convolution Mamba Block (PCMB), dat kenmerken in groepen splitst en deze via meerdere lichte Mamba-gebaseerde en convolutionele paden verwerkt voordat ze weer samengevoegd worden. Dit ontwerp balanceert globale context en fijne details terwijl de rekenkosten laag blijven. Ze herzien ook de skip-verbindingen die encoder en decoder koppelen. Een nieuw Enhanced Spatial-Channel Attention (ESCA) module benadrukt selectief belangrijke locaties en feature-kanalen, terwijl nuttige informatie behouden blijft via residuele verbindingen. Dit maakt het netwerk minder vatbaar voor verwarring door afleidingen zoals haar, schittering of ruisige texturen rond een laesie.
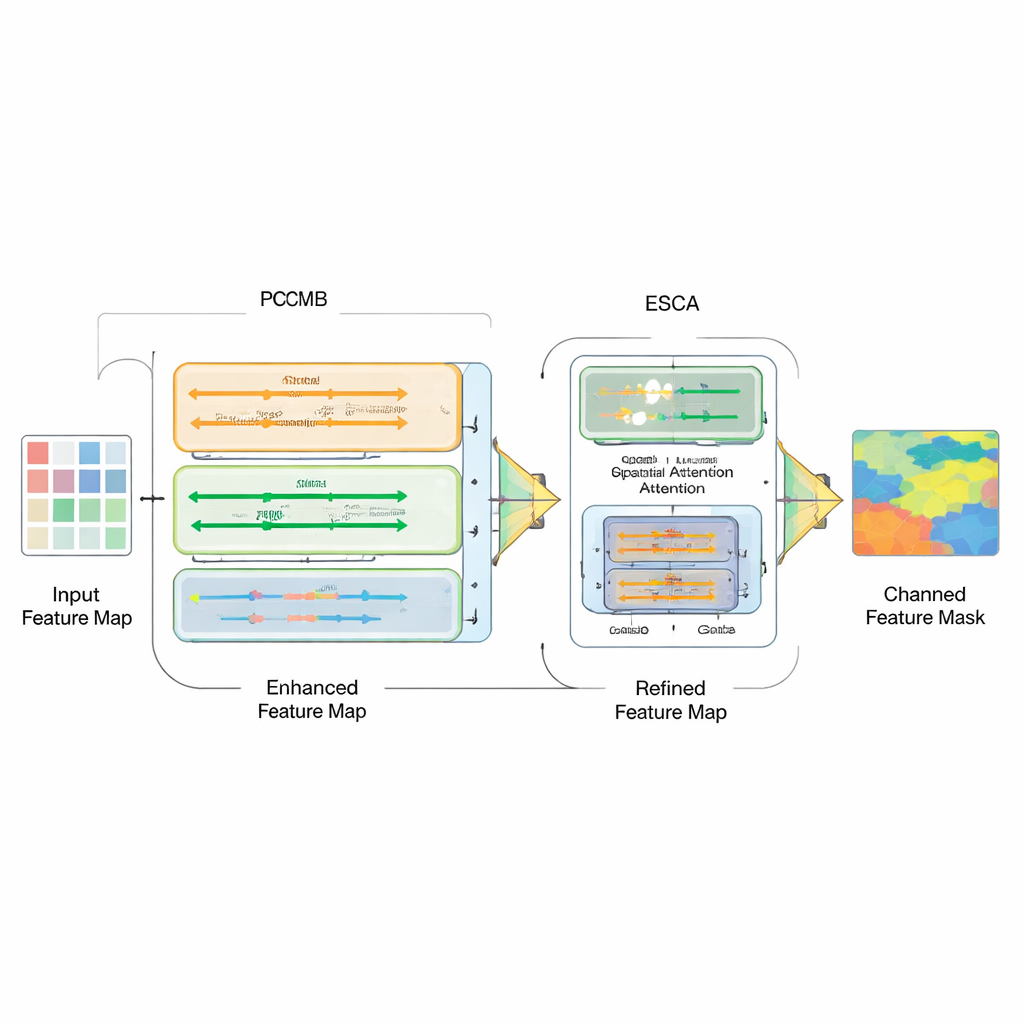
Hoe goed werkt de nieuwe aanpak?
Het team evalueert KMP-UNet op vier openbare datasets met huidlaesies, colonpoliepen en borst-echobeelden, en test ook overdracht naar een andere huiddataset. Over deze benchmarks heen evenaart of overtreft het model consequent een reeks sterke basismodellen, waaronder klassieke UNet-varianten, transformer-gebaseerde ontwerpen en andere recentere Mamba- en KAN-versterkte netwerken. Bijvoorbeeld, op een veelgebruikte huidlaesie-dataset (ISIC2018) bereikt KMP-UNet een hoge Dice-score en nauwkeurigheid terwijl het ongeveer één miljoen parameters gebruikt—veel minder dan veel concurrenten. Gedetailleerde experimenten tonen aan dat elk component—Mamba-gebaseerde contextmodellering, KAN-gebaseerde niet-lineaire verfijning en ESCA-gebaseerde skip-verfijning—meetbare verbeteringen bijdraagt, vooral in randkwaliteit en vermindering van fout-positieve regio’s.
Wat dit betekent voor toekomstige medische AI-tools
Voor niet-specialisten is de belangrijkste conclusie dat KMP-UNet een compacter maar capabeler middel biedt om computers te leren laesies en organen in beelden af te bakenen, door twee complementaire “experts” parallel te laten werken en hun inzichten zorgvuldig te fusioneren. Hoewel de methode nog worstelt met de meest uitdagende gevallen—zeer onregelmatige vormen, extreem vage randen of zware artefacten—biedt het een sterke basis voor nauwkeurige, efficiënte segmentatie. Met verder werk aan het omgaan met rumoerige achtergronden en aanpassing tussen beeldvormingscentra, zouden benaderingen zoals KMP-UNet kunnen bijdragen aan sneller en betrouwbaarder beeldanalysegebruik in de dagelijkse klinische praktijk.
Bronvermelding: Liu, J., Wu, J., Xu, L. et al. A parallel UNet integrating KAN and mamba for medical image segmentation. Sci Rep 16, 13579 (2026). https://doi.org/10.1038/s41598-026-43127-1
Trefwoorden: segmentatie van medische beelden, deep learning, UNet, statusruimte-modellen, Kolmogorov–Arnold-netwerken