Clear Sky Science · sv
Intrakraniell LPS‑injektion framkallar motoriska och beteendemässiga brister liknande cerebral pares hos immunbristmöss
Varför denna forskning är viktig
Cerebral pares är en av de vanligaste orsakerna till livslånga rörlighetsproblem hos barn, men läkare saknar fortfarande behandlingar som verkligen kan reparera den skadade hjärnan. Många lovande angreppssätt, som stamcellsterapier, måste först testas i djur. Standardlaboratoriedjur avvisar dock ofta mänskliga celler, vilket försvårar bedömningen om en behandling kommer att fungera hos barn. Denna studie introducerar en ny musmodell som noggrant efterliknar centrala rörlighetsproblem vid cerebral pares samtidigt som den är kompatibel med mänskliga celler, vilket öppnar för mer realistiska tester av framtida behandlingar.
Att bygga en särskild musmodell
Forskargruppen arbetade med nyfödda immunbristmöss som saknar viktiga delar av immunsystemet som normalt angriper främmande celler. När ungarna var sex dagar gamla injicerade forskarna försiktigt en mycket liten mängd lipopolysackarid, eller LPS — en molekyl som finns hos vissa bakterier — direkt i en vit substans‑region i hjärnan. LPS används ofta i forskning eftersom den pålitligt framkallar inflammation, liknande det som kan ske vid en allvarlig infektion före eller strax efter födseln, en känd riskfaktor för cerebral pares. En andra grupp ungar genomgick samma operation men fick endast saltlösning och fungerade som friska kontroller. Mössen tilläts därefter växa i sex veckor, vilket ungefär motsvarar en juvenilstadium, innan deras hälsa och beteende undersöktes i detalj. 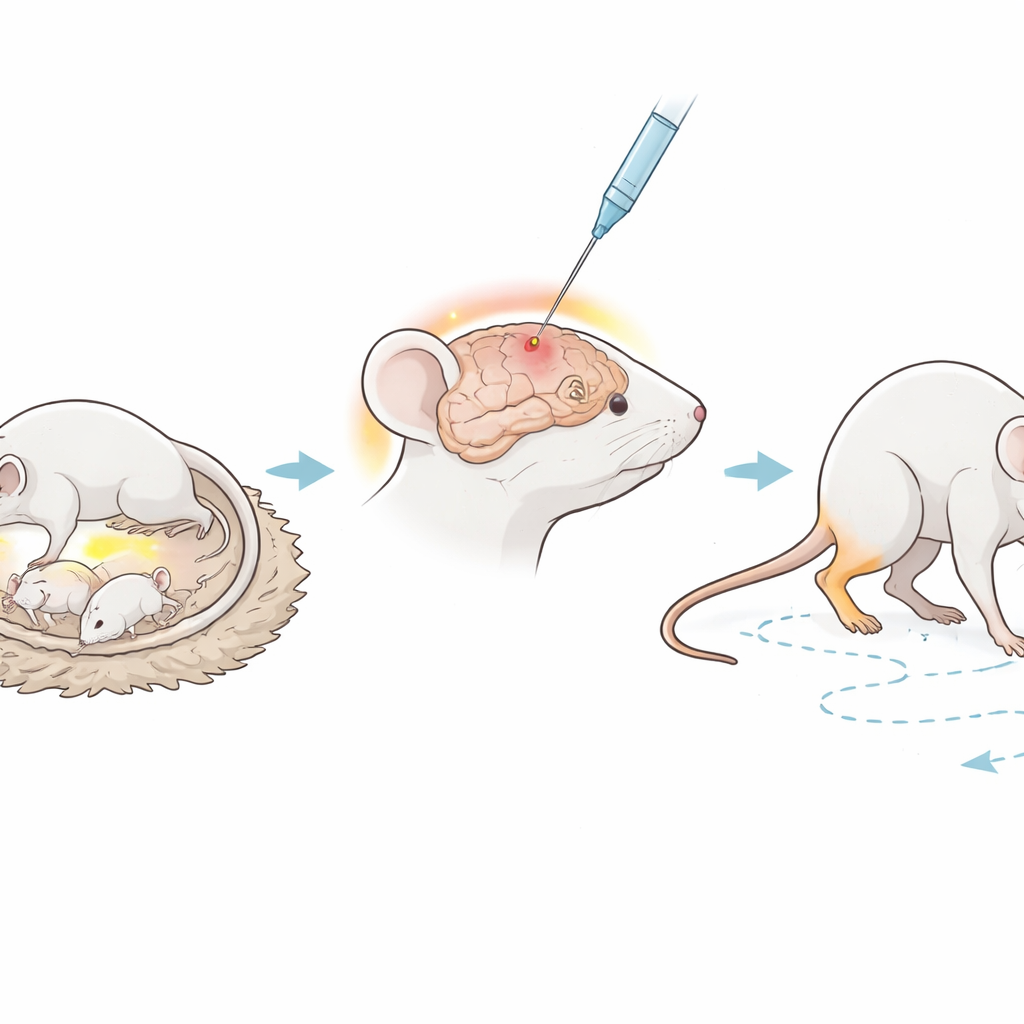
Tecken på sämre tillväxt och ojämn rörelse
Jämfört med kontrollgruppen överlevde färre LPS‑behandlade möss till slutet av studien, och de som överlevde vägde mindre, vilket tyder på att den tidiga hjärnskadan påverkade den övergripande utvecklingen. När forskarna testade grundläggande rörelser fann de att LPS‑behandlade möss uppvisade en tydlig obalans: när de hölls försiktigt i svansen svängde kroppen oftare åt ena sidan, och på en roterande stång föll de av tidigare, vilket indikerar nedsatt balans och uthållighet. I en öppen arena gick dessa möss långsammare och täckte mindre sträcka totalt, ett mönster känt som hypolokomotion. Intressant nog, även om de inte tillbringade mer tid i mitten av arenan, skedde en större andel av deras begränsade rörelse där, vilket antyder förändrade utforskningsmönster snarare än enbart förändringar i ångest.
Gångförändringar som speglar barns gångproblem
De mest iögonfallande fynden kom från datoriserad gånganalys, som mäter hur varje tass rör sig när musen går på ett transparent löpband. LPS‑behandlade möss gick långsammare, med längre stegscykler och färre steg per sekund. Deras bakben var särskilt påverkade: de var mer i kontakt med bandet och tryckte ifrån under längre tid, men deras stödlinje blev smalare. Vinkeln på baktassarna ökade, vilket liknar de inåtvända, saxliknande fotpositioner som ofta ses hos barn med spastisk diplegi‑cerebral pares. Samtidigt visade frambenen andra förändringar, vilket understryker en komplex omformning av koordineringen mellan fram‑ och bakben. Tillsammans indikerar dessa mönster en mångfacetterad rörelserubbning dominerad av bakbensavvikelser, som starkt parallellerar de underkropps‑inriktade problemen hos många barn med cerebral pares. 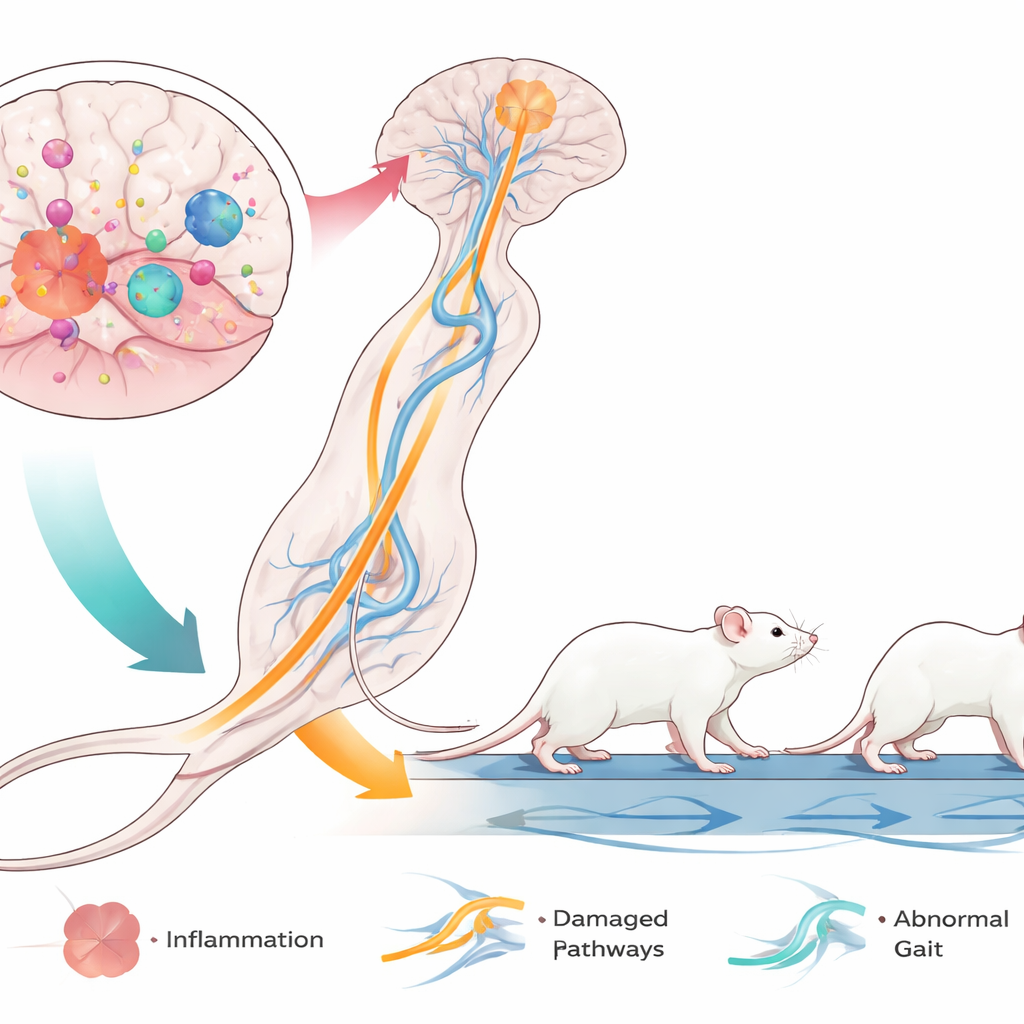
Vad som kan pågå inne i hjärnan
Även om denna studie inte mätte hjärnceller direkt bygger den på tidigare arbete som tyder på att LPS utlöser en aggressiv inflammatorisk respons i hjärnans egna immunceller, så kallade mikroglia. Dessa aktiverade celler kan skada isoleringen runt nervfibrer — särskilt i vit substans som förmedlar signaler från hjärnans rörelsecentra till ryggmärgen och benen. Eftersom mössen saknar adaptiva immunceller men fortfarande har medfödda immunreaktioner isolerar modellen hur tidig inflammation i sig kan störa motoriska banor samtidigt som den förblir kompatibel med transplantation av mänskliga celler. De bakbensfokuserade bristerna antyder att specifika hjärnregioner och kopplingsbanor för bakbenen är särskilt sårbara för denna typ av tidiga skador.
Vad detta betyder för framtida terapier
Enkelt uttryckt skapade forskarna unga möss vars rörlighetsproblem liknar en form av cerebral pares hos barn, med särskild påverkan på benen, och gjorde det i djur som säkert kan hysa mänskliga celler. Denna nya modell fångar inte alla aspekter av det mänskliga tillståndet, men den erbjuder en realistisk och etiskt förfinad plattform för att undersöka hur tidig inflammation skadar den utvecklande hjärnan och för att testa om experimentella behandlingar — särskilt mänskliga stamcells‑ och andra cellbaserade terapier — kan återställa mer normal rörlighet. Om framgångsrika behandlingar framkommer i detta sammanhang är det mer sannolikt att de översätts till verkliga förbättringar för barn som lever med cerebral pares.
Citering: Yang, J., Li, Y., Shi, C. et al. Intracranial LPS injection induces cerebral palsy-like motor and behavioral deficits in immunodeficient mice. Sci Rep 16, 10105 (2026). https://doi.org/10.1038/s41598-026-40909-5
Nyckelord: cerebral pares, neuroinflammation, djurmodeller, gångavvikelser, cellterapi