Clear Sky Science · nl
Intracraniële LPS-injectie veroorzaakt motorische en gedragsstoornissen vergelijkbaar met cerebrale parese bij immuundeficiënte muizen
Waarom dit onderzoek belangrijk is
Cerebrale parese is één van de meest voorkomende oorzaken van levenslange bewegingsproblemen bij kinderen, maar artsen hebben nog steeds geen behandelingen die het beschadigde brein echt kunnen herstellen. Veel veelbelovende benaderingen, zoals stamceltherapieën, moeten eerst in dieren worden getest. Standaard laboratoriumdieren verwerpen echter vaak menselijke cellen, waardoor het moeilijk is te voorspellen of een therapie bij kinderen zal werken. Deze studie introduceert een nieuw muismodel dat nauw aansluit bij de belangrijkste bewegingsproblemen gezien bij cerebrale parese en tegelijkertijd compatibel is met menselijke cellen, wat realistischer testen van toekomstige behandelingen mogelijk maakt.
Het opbouwen van een speciaal muismodel
Het team werkte met pasgeboren immuundeficiënte muizen die belangrijke onderdelen van het immuunsysteem missen die normaal vreemde cellen aanvallen. Toen de pups zes dagen oud waren, injecteerden de onderzoekers voorzichtig een kleine hoeveelheid lipopolysaccharide, of LPS—een molecule die op bepaalde bacteriën voorkomt—direct in een witte-stofgebied van de hersenen. LPS wordt veel gebruikt in onderzoek omdat het betrouwbaar ontsteking opwekt, vergelijkbaar met wat kan optreden tijdens een ernstige infectie voor of kort na de geboorte, een bekende risicofactor voor cerebrale parese. Een tweede groep pups onderging dezelfde operatie maar kreeg alleen zoutoplossing, en diende als gezonde controlegroep. De muizen mochten vervolgens zes weken opgroeien, wat grofweg overeenkomt met een juveniele fase, voordat hun gezondheid en gedrag in detail werden onderzocht. 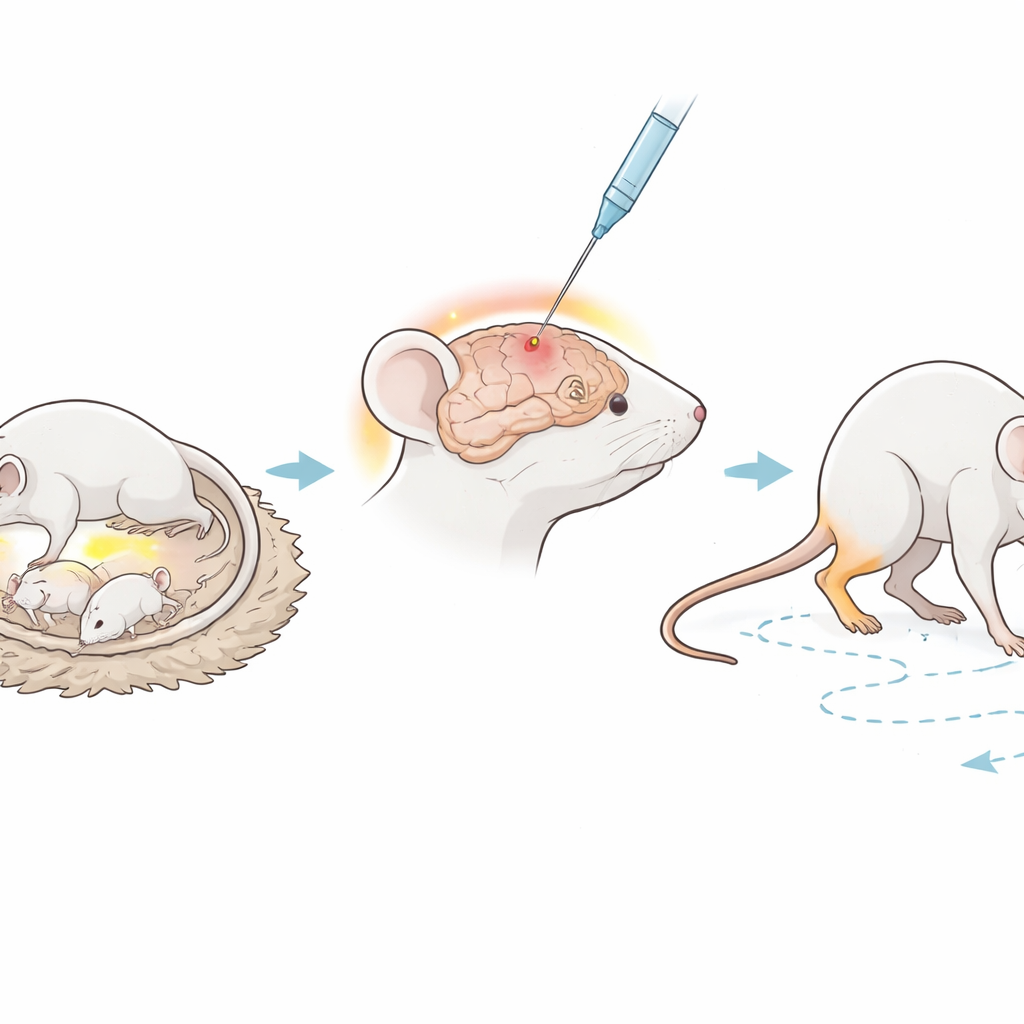
Tekenen van slechtere groei en oneven beweging
Vergeleken met controledieren overleefden minder LPS-behandelde muizen de volledige studie, en degenen die dat wel deden wogen minder, wat suggereert dat de vroege hersenbeschadiging de algemene ontwikkeling aantastte. Toen de onderzoekers basale beweging testten, vonden ze dat LPS-behandelde muizen een duidelijke onevenwichtigheid vertoonden: wanneer ze voorzichtig aan hun staart werden opgetild, zwaaiden hun lichamen vaker naar één kant, en op een roterende stok vielen ze eerder van de stok af, wat wijst op verminderde balans en uithoudingsvermogen. In een open arena liepen deze muizen langzamer en legden ze in totaal minder afstand af, een patroon dat bekend staat als hypolocomotie. Interessant genoeg brachten ze niet meer tijd door in het midden van de arena, maar een groter aandeel van de beperkte beweging die ze maakten vond daar plaats, wat duidt op veranderde verkenningspatronen in plaats van eenvoudige veranderingen in angst.
Loopveranderingen die echoën van wandelproblemen bij kinderen
De meest opvallende bevindingen kwamen uit gecomputeriseerde ganganalyse, die meet hoe elke poot beweegt terwijl de muis op een transparante loopband loopt. LPS-behandelde muizen liepen langzamer, met langere stapcycli en minder stappen per seconde. Hun achterpoten waren bijzonder aangetast: ze brachten meer tijd in contact met de band door en duwden langer af, maar hun steunbasis werd smaller. De hoek van de achterpoten nam toe, wat leek op de naar binnen gedraaide, schaarachtige voetposities die vaak worden gezien bij kinderen met spastische diplegie. Tegelijkertijd lieten de voorpoten andere veranderingen zien, wat wijst op een complexe herschikking van de coördinatie tussen voor- en achterpoten. Gezamenlijk wijzen deze patronen op een veelzijdige bewegingsstoornis die wordt gedomineerd door afwijkingen in de achterpoten, nauw vergelijkbaar met de problemen die bij veel kinderen met cerebrale parese in de onderste ledematen voorkomen. 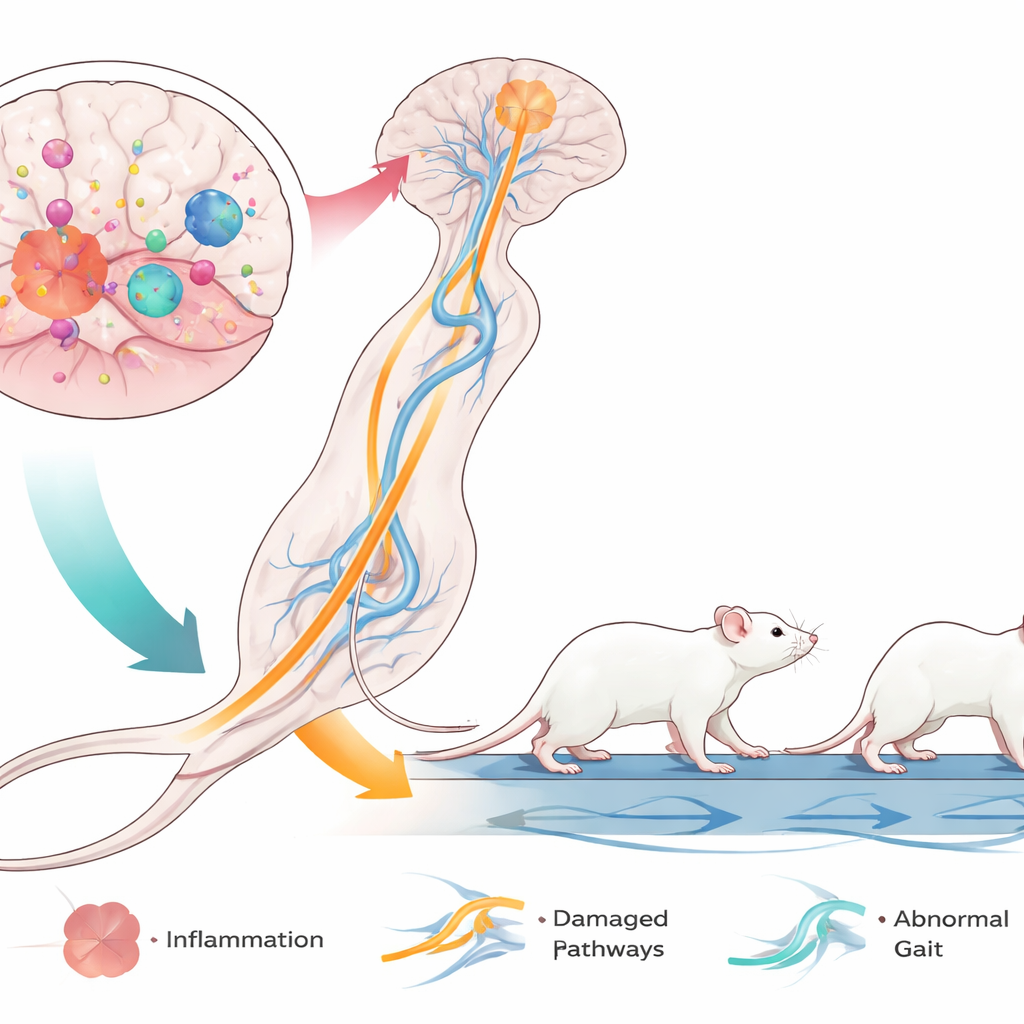
Wat er mogelijk in de hersenen gebeurt
Hoewel deze studie de hersencellen niet rechtstreeks mat, put zij uit eerder werk dat suggereert dat LPS een agressieve ontstekingsreactie opwekt in de residentiële immuuncellen van de hersenen, de microglia. Deze geactiveerde cellen kunnen de isolatie rond zenuwvezels beschadigen—vooral in witte-stofgebieden die signalen van de bewegingscentra van de hersenen naar het ruggenmerg en de benen geleiden. Omdat de muizen adaptieve immuuncellen missen maar nog wel aangeboren immuunreacties hebben, is het model geschikt om te laten zien hoe vroeg ontsteking op zichzelf motorische banen kan verstoren terwijl het compatibel blijft met menselijke celtransplantaties. De op de achterpoten gerichte tekorten suggereren dat specifieke hersengebieden en de bedrading voor de achterpoten bijzonder kwetsbaar zijn voor dit soort vroegtijdige schade.
Wat dit betekent voor toekomstige therapieën
In eenvoudige bewoordingen creëerden de onderzoekers jonge muizen waarvan de bewegingsproblemen sterk lijken op een vorm van cerebrale parese bij kinderen, met name met een effect op de benen, en deden dat in dieren die veilig menselijke cellen kunnen herbergen. Dit nieuwe model vat niet elk aspect van de menselijke aandoening samen, maar het biedt een realistisch en ethisch verfijnd platform om te onderzoeken hoe vroege ontsteking het zich ontwikkelende brein beschadigt en om te testen of experimentele behandelingen—vooral menselijke stamcel- en andere celgebaseerde therapieën—meer normaal bewegen kunnen herstellen. Als er in deze setting succesvolle therapieën ontstaan, is de kans groter dat ze zich vertalen naar zinvolle verbeteringen voor kinderen die leven met cerebrale parese.
Bronvermelding: Yang, J., Li, Y., Shi, C. et al. Intracranial LPS injection induces cerebral palsy-like motor and behavioral deficits in immunodeficient mice. Sci Rep 16, 10105 (2026). https://doi.org/10.1038/s41598-026-40909-5
Trefwoorden: cerebrale parese, neuro-inflammatie, diermodellen, loopafwijkingen, celtherapie