Clear Sky Science · fr
L’injection intracrânienne de LPS induit des déficits moteurs et comportementaux de type paralysie cérébrale chez des souris immunodéficientes
Pourquoi cette recherche est importante
La paralysie cérébrale est l’une des causes les plus fréquentes de difficultés motrices durables chez l’enfant, et pourtant les médecins disposent encore de peu de traitements capables de réparer réellement le cerveau lésé. De nombreuses approches prometteuses, comme les thérapies par cellules souches, doivent d’abord être testées chez l’animal. Or, les animaux de laboratoire usuels rejettent souvent les cellules humaines, ce qui complique la prédiction de l’efficacité d’un traitement chez l’enfant. Cette étude présente un nouveau modèle murin qui reproduit fidèlement des troubles moteurs clés observés dans la paralysie cérébrale tout en étant compatible avec des cellules humaines, ouvrant la voie à des évaluations plus réalistes des futurs traitements.
Construire un modèle murin particulier
L’équipe a travaillé avec des souris nouveau‑nées immunodéficientes qui sont dépourvues d’éléments essentiels du système immunitaire qui attaquent normalement les cellules étrangères. À six jours après la naissance, les chercheurs ont injecté avec précaution une très petite quantité de lipopolysaccharide, ou LPS — une molécule présente chez certaines bactéries — directement dans une région de matière blanche du cerveau. Le LPS est largement utilisé en recherche parce qu’il provoque de façon fiable une inflammation, semblable à ce qui peut survenir lors d’une infection sévère avant ou peu après la naissance, un facteur de risque connu de la paralysie cérébrale. Un second groupe de petits a subi la même chirurgie mais n’a reçu que de l’eau salée, servant de témoins sains. Les souris ont ensuite été élevées pendant six semaines, correspondant approximativement à un stade juvénile, avant que leur santé et leur comportement ne soient examinés en détail. 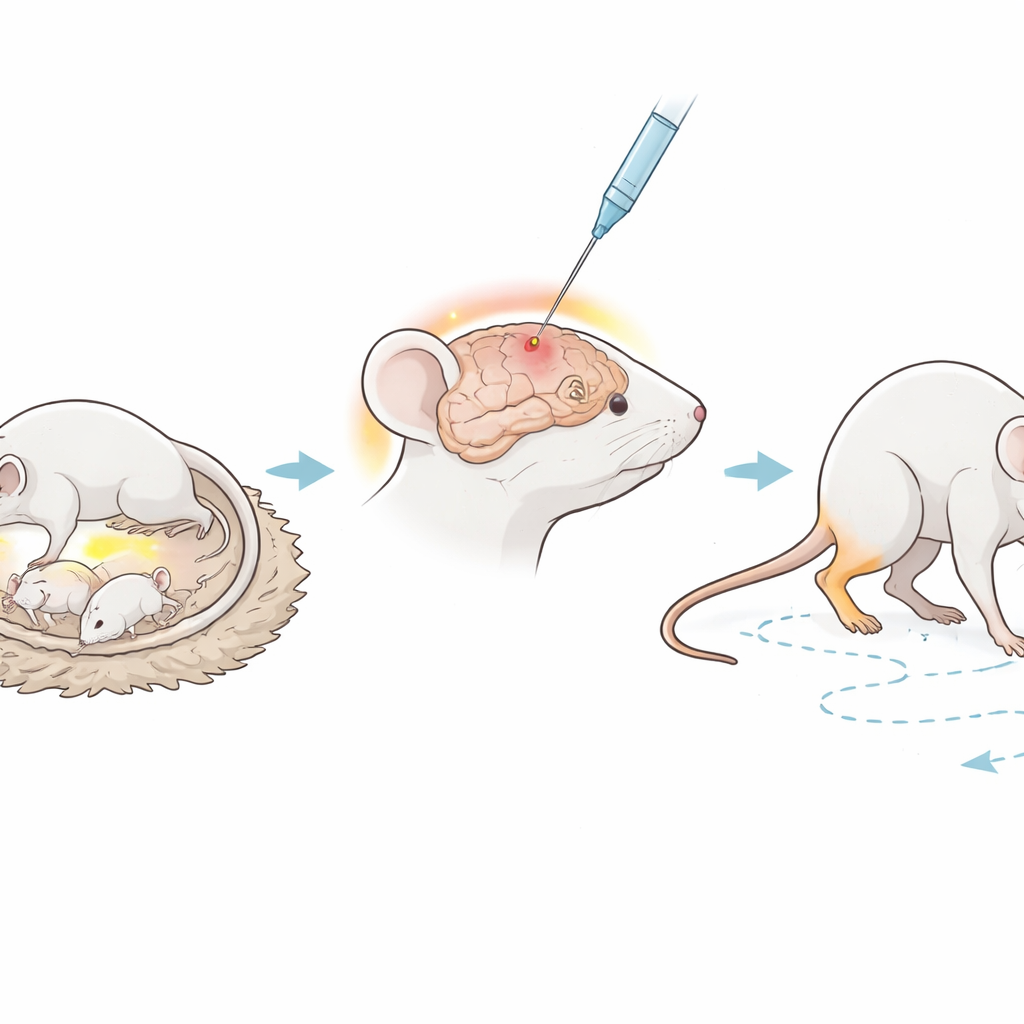
Signes de croissance ralentie et de mouvements inégaux
Par rapport aux animaux témoins, moins de souris traitées au LPS ont survécu jusqu’à la fin de l’étude, et celles qui ont survécu pesaient moins, suggérant que l’agression cérébrale précoce a affecté le développement global. Lors des tests de motricité de base, les chercheurs ont observé un déséquilibre net chez les souris traitées au LPS : tenues délicatement par la queue, leur corps basculait plus souvent d’un côté, et sur une barre rotative elles tombaient plus rapidement, indiquant une réduction de l’équilibre et de l’endurance. Dans une arène ouverte, ces souris se déplaçaient plus lentement et parcouraient moins de distance au total, un schéma connu sous le nom d’hypolocomotion. Fait intéressant, bien qu’elles ne passent pas plus de temps au centre de l’arène, une plus grande part de leurs rares déplacements avait lieu là‑bas, suggérant des modifications du mode d’exploration plutôt qu’un simple changement d’anxiété.
Modifications de la démarche rappelant les troubles de la marche chez l’enfant
Les résultats les plus frappants proviennent de l’analyse informatisée de la démarche, qui mesure le mouvement de chaque patte lorsque la souris marche sur un tapis roulant transparent. Les souris traitées au LPS marchaient plus lentement, avec des cycles de pas plus longs et moins de pas par seconde. Leurs membres postérieurs étaient particulièrement affectés : ils restaient plus longtemps en contact avec la bande et poussaient plus longtemps, mais leur base de sustentation devenait plus étroite. L’angle des pattes arrière augmentait, ressemblant aux positions convergentes et en « cisaillement » souvent observées chez les enfants atteints de paralysie cérébrale spastique diplegique. Dans le même temps, les pattes avant montraient des modifications différentes, soulignant une reconfiguration complexe de la coordination entre membres antérieurs et postérieurs. Ensemble, ces profils indiquent un trouble moteur multifacette dominé par des anomalies des membres postérieurs, parallèle aux problèmes centrés sur les membres inférieurs chez de nombreux enfants atteints de paralysie cérébrale. 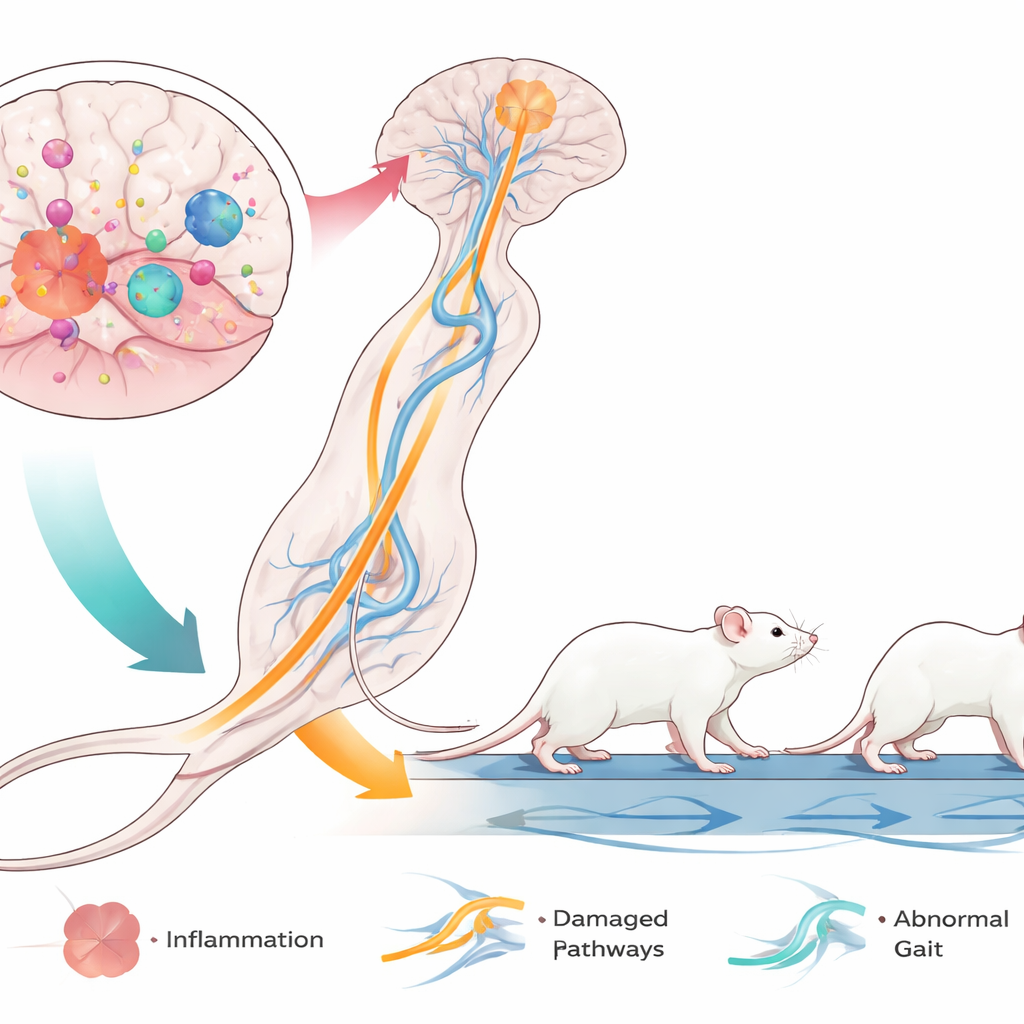
Ce qui pourrait se passer à l’intérieur du cerveau
Bien que cette étude n’ait pas mesuré directement les cellules cérébrales, elle s’appuie sur des travaux antérieurs suggérant que le LPS déclenche une réponse inflammatoire agressive des cellules immunitaires résidentes du cerveau, appelées microglies. Ces cellules activées peuvent endommager l’isolant entourant les fibres nerveuses — en particulier dans les régions de matière blanche qui véhiculent les signaux des centres moteurs du cerveau vers la moelle épinière et les pattes. Parce que les souris manquent de cellules immunitaires adaptatives mais conservent des réponses immunitaires innées, le modèle isole l’effet d’une inflammation précoce seule sur les voies motrices tout en restant compatible avec des greffes de cellules humaines. Les déficits centrés sur les membres postérieurs laissent entendre que des régions et des circuits spécifiques responsables des pattes arrière sont particulièrement vulnérables à ce type d’agression en début de vie.
Ce que cela signifie pour les thérapies futures
En termes simples, les chercheurs ont créé de jeunes souris dont les troubles moteurs ressemblent et se comportent comme une forme de paralysie cérébrale chez l’enfant, affectant particulièrement les jambes, et ce dans des animaux capables d’héberger des cellules humaines en toute sécurité. Ce nouveau modèle ne capture pas tous les aspects de la condition humaine, mais il offre une plateforme réaliste et éthiquement améliorée pour explorer comment l’inflammation précoce blesse le cerveau en développement et pour tester si des traitements expérimentaux — en particulier les thérapies cellulaires humaines et autres approches à base de cellules — peuvent restaurer une motricité plus normale. Si des thérapies s’avèrent efficaces dans ce contexte, elles auront plus de chances de se traduire par des améliorations significatives pour les enfants vivant avec une paralysie cérébrale.
Citation: Yang, J., Li, Y., Shi, C. et al. Intracranial LPS injection induces cerebral palsy-like motor and behavioral deficits in immunodeficient mice. Sci Rep 16, 10105 (2026). https://doi.org/10.1038/s41598-026-40909-5
Mots-clés: paralysie cérébrale, neuroinflammation, modèles animaux, anomalies de la démarche, thérapie cellulaire