Clear Sky Science · ar
حقن LPS داخل القحف يسبب عجزًا حركيًا وسلوكيًا شبيهًا بالشلل الدماغي في فئران ناقصة المناعة
لماذا يهم هذا البحث
الشلل الدماغي هو أحد أكثر أسباب الصعوبات الحركية المستمرة مدى الحياة شيوعًا لدى الأطفال، ومع ذلك يفتقر الأطباء إلى علاجات قادرة فعليًا على إصلاح الدماغ المصاب. يجب اختبار العديد من النهج الواعدة، مثل علاجات الخلايا الجذعية، أولًا على الحيوانات. إلا أن الحيوانات المخبرية القياسية غالبًا ما ترفض الخلايا البشرية، مما يصعب التنبؤ بما إذا كان العلاج سينجح لدى الأطفال. تُقدم هذه الدراسة نموذج فئران جديدًا يُحاكي عن كثب مشاكل الحركة الرئيسية في الشلل الدماغي وفي الوقت ذاته مناسبًا لاستقبال خلايا بشرية، مما يفتح المجال لاختبارات أكثر واقعية للعلاجات المستقبلية.
بناء نموذج فأري خاص
عمل الفريق مع فئران حديثة الولادة ناقصة المناعة تفتقر إلى أجزاء رئيسية من الجهاز المناعي التي تهاجم عادة الخلايا الأجنبية. عندما كان الصغار في عمر ستة أيام، حقن الباحثون بعناية كمية صغيرة من الليبوبوليسكرايد، أو LPS — وهو جزيء موجود على بعض البكتيريا — مباشرة في منطقة المادة البيضاء في الدماغ. يُستخدم LPS على نطاق واسع في الأبحاث لأنه يثير الالتهاب بشكل موثوق، مشابهًا لما قد يحدث خلال عدوى شديدة قبل الولادة أو بعدها بفترة وجيزة، وهو عامل خطر معروف للشلل الدماغي. خضعت مجموعة ثانية من الصغار لنفس العملية الجراحية لكنها تلقت ماءً مالحًا فقط، لتكون مجموعة ضابطة سليمة. تُركت الفئران لتنمو لمدة ستة أسابيع، تقابل مرحلة شبابية تقريبًا، قبل أن تُفحص صحتها وسلوكها بالتفصيل. 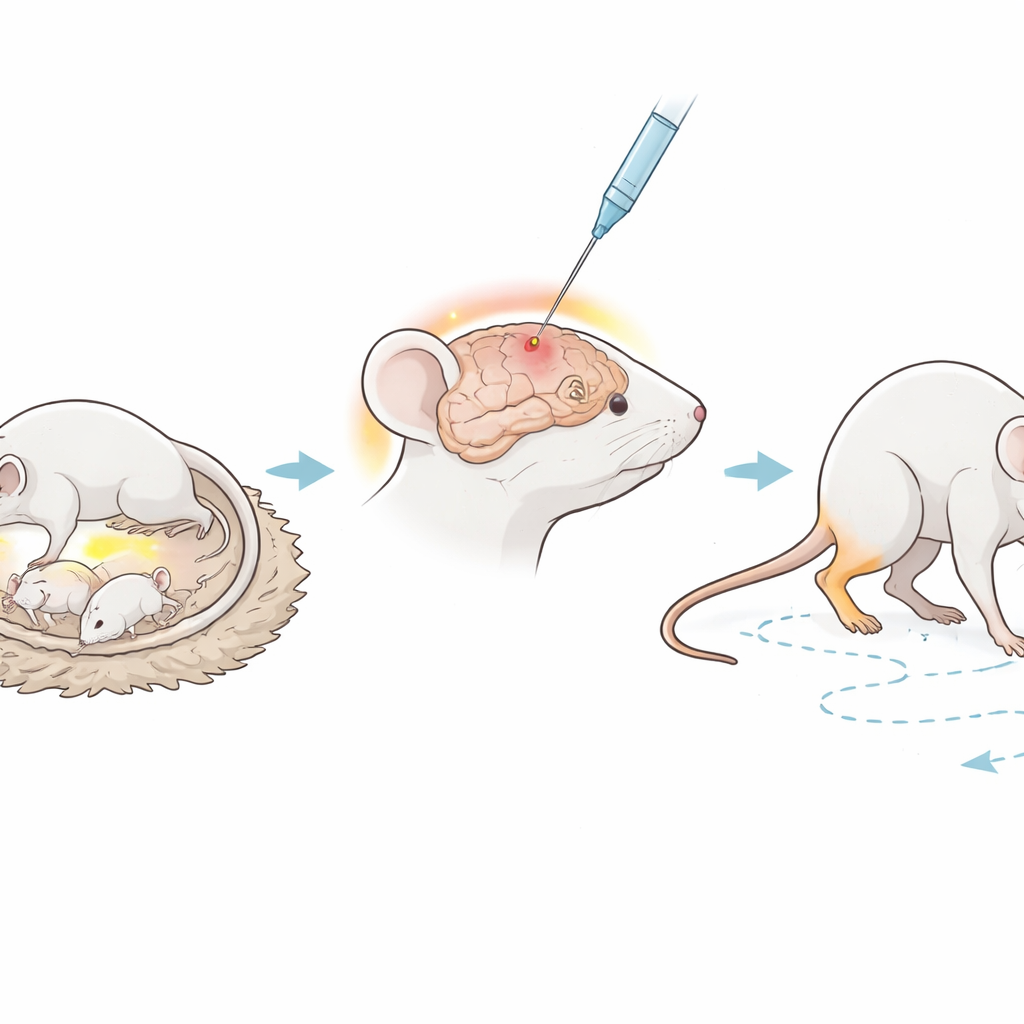
علامات تباطؤ النمو وحركة غير متوازنة
بالمقارنة مع الحيوانات الضابطة، نجت فئران الـLPS بنسبة أقل حتى نهاية الدراسة، وكان وزن الناجين أقل، مما يشير إلى أن الإصابة المبكرة في الدماغ أثرت على التطور العام. عند اختبار الحركة الأساسية، وجد الباحثون أن فئران الـLPS أظهرت خللًا واضحًا في التوازن: عند حملها برفق من الذيل، كانت أجسادها تتأرجح أكثر إلى أحد الجانبين، وعلى قضيب دوار كانت تسقط أسرع، مما يدل على ضعف التوازن والقدرة على التحمل. في ساحة مفتوحة، مشت هذه الفئران أبطأ وقطعت مسافة إجمالية أقل، وهو نمط يُعرف بنقص الحركة. ومن المثير أن هذه الفئران لم تقضِ وقتًا أطول في مركز الساحة، لكن نسبة أكبر من الحركة القليلة التي قامت بها حدثت هناك، مما يوحي بتغيّر في أنماط الاستكشاف بدل تغيير بسيط في مستوى القلق.
تغيرات في المشي تشبه مشاكل المشي لدى الأطفال
أكثر النتائج بروزًا جاءت من تحليل المشية المحوسب، الذي يقيس كيفية حركة كل كف أثناء سير الفأر على سير شفاف. مشت فئران الـLPS أبطأ، مع دورات خطوات أطول وعدد خطوات أقل في الثانية. كانت الأطراف الخلفية متأثرة بشكل خاص: قضت وقتًا أطول على الحزام ودفعَت لمسافة أطول، لكن قاعدة دعمها أصبحت أضيق. ازداد زاوية الأقدام الخلفية، مشابهة لوضعية الانعطاف الداخلي للأقدام أو ما يشبه مقصًا التي تُرى غالبًا لدى الأطفال المصابين بالشلل الدماغي المشدود ثنائي الشلل. في الوقت نفسه، أظهرت الأقدام الأمامية تغيرات مختلفة، مما يبرز إعادة تشكيل معقدة للتنسيق بين الأطراف الأمامية والخلفية. مجتمعة، تشير هذه الأنماط إلى اضطراب حركي متعدد الأوجه يهيمن عليه شذوذات الأطراف الخلفية، بما يقارب مشاكل الأطراف السفلية لدى كثير من الأطفال المصابين بالشلل الدماغي.
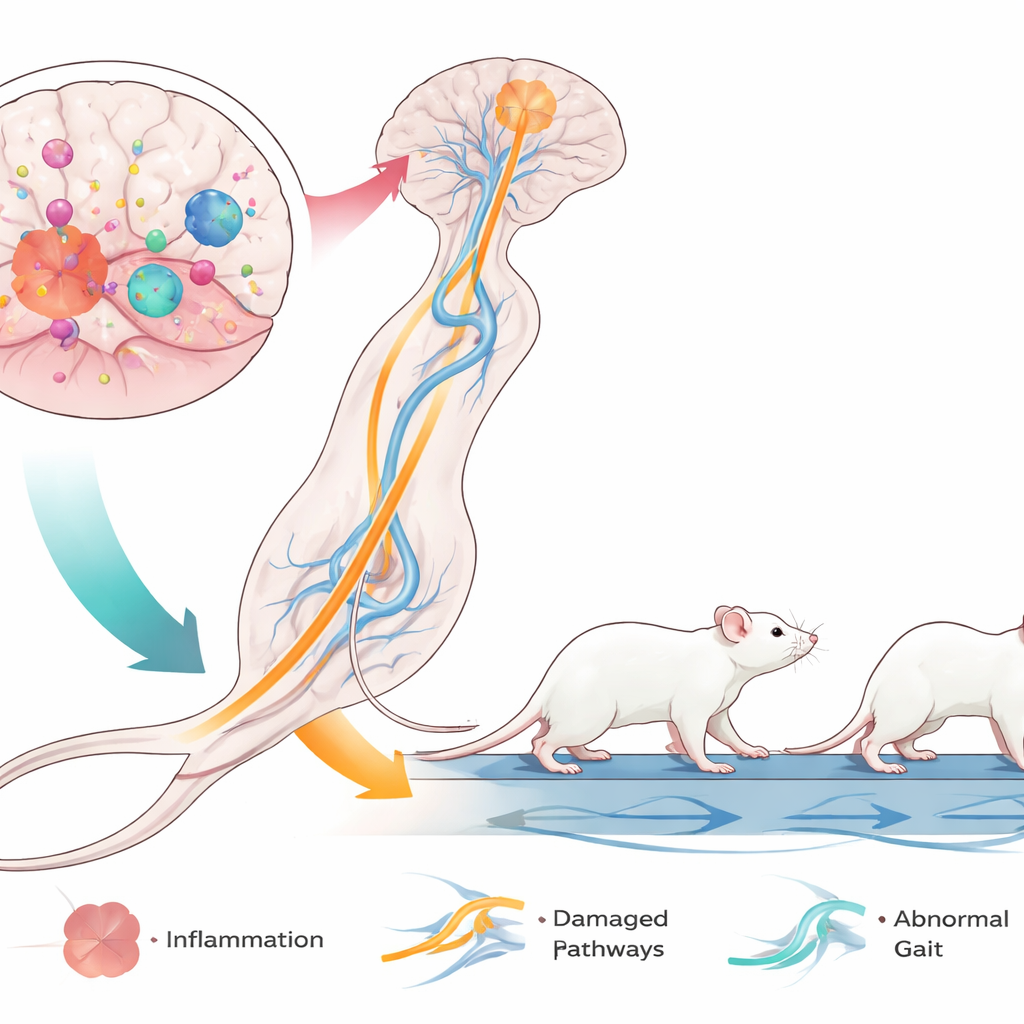
ما الذي قد يحدث داخل الدماغ
رغم أن هذه الدراسة لم تقِس الخلايا الدماغية مباشرة، فإنها تستند إلى أعمال سابقة تشير إلى أن LPS يثير استجابة التهابية عنيفة في الخلايا المناعية المقيمة في الدماغ، المسماة الميكروغليا. يمكن لهذه الخلايا المنشطة أن تتلف غلاف العصب — خاصة في مناطق المادة البيضاء التي تنقل الإشارات من مراكز الحركة في الدماغ إلى النخاع الشوكي والأرجل. وبما أن الفئران تفتقر للخلايا المناعية التكيفية لكنها لا تزال تمتلك استجابات مناعية فطرية، فإن النموذج يعزل تأثير الالتهاب المبكر بمفرده على مسارات الحركة مع بقائه متوافقًا مع زرع الخلايا البشرية. وتشير العيوب المركزة في الأطراف الخلفية إلى أن مناطق محددة من الدماغ والدوائر العصبية المسؤولة عن الأرجل الخلفية أكثر عرضة لهذا النوع من الإصابة في فترة الحياة المبكرة.
ماذا يعني هذا للعلاجات المستقبلية
ببساطة، أنشأ الباحثون فئرانًا صغيرة تبدو مشاكل حركتها وتصرفاتها مشابهة لشكل من أشكال الشلل الدماغي لدى الأطفال، مع تأثير واضح على الساقين، وفعلوا ذلك في حيوانات قادرة على استضافة خلايا بشرية بأمان. لا يلتقط هذا النموذج كل جوانب الحالة البشرية، لكنه يوفر منصة واقعية ومُحسنة أخلاقيًا لاستكشاف كيف يضر الالتهاب المبكر الدماغ النامي وللاختبار ما إذا كانت العلاجات التجريبية — وخصوصًا علاجات الخلايا البشرية وغيرها من العلاجات الخلوية — قادرة على استعادة حركة أكثر طبيعية. إذا برزت علاجات ناجحة في هذا الإعداد، فمن المحتمل أن تُترجَم إلى تحسينات ذات مغزى للأطفال المصابين بالشلل الدماغي.
الاستشهاد: Yang, J., Li, Y., Shi, C. et al. Intracranial LPS injection induces cerebral palsy-like motor and behavioral deficits in immunodeficient mice. Sci Rep 16, 10105 (2026). https://doi.org/10.1038/s41598-026-40909-5
الكلمات المفتاحية: الشلل الدماغي, الالتهاب العصبي, نماذج حيوانية, اضطرابات المشي, علاج بالخلايا