Clear Sky Science · es
La inyección intracraneal de LPS induce déficits motores y conductuales similares a parálisis cerebral en ratones inmunodeficientes
Por qué importa esta investigación
La parálisis cerebral es una de las causas más comunes de dificultades de movimiento a lo largo de la vida en la infancia, y sin embargo los médicos aún carecen de tratamientos que puedan reparar verdaderamente el cerebro lesionado. Muchos enfoques prometedores, como las terapias con células madre, deben probarse primero en animales. Sin embargo, los animales de laboratorio estándar a menudo rechazan células humanas, lo que dificulta predecir si una terapia funcionará en niños. Este estudio presenta un nuevo modelo de ratón que imita de forma ajustada problemas de movimiento clave observados en la parálisis cerebral y que además es compatible con células humanas, abriendo la puerta a ensayos más realistas de futuros tratamientos.
Construyendo un tipo especial de modelo de ratón
El equipo trabajó con ratones inmunodeficientes recién nacidos que carecen de partes clave del sistema inmune que normalmente atacan células extrañas. Cuando las crías tenían seis días, los investigadores inyectaron cuidadosamente una pequeña cantidad de lipopolisacárido, o LPS—una molécula presente en ciertas bacterias—directamente en una región de materia blanca del cerebro. El LPS se utiliza ampliamente en investigación porque desencadena de forma fiable inflamación, similar a la que podría ocurrir durante una infección grave antes o poco después del nacimiento, un factor de riesgo conocido para la parálisis cerebral. Un segundo grupo de crías se sometió a la misma cirugía pero recibió solo solución salina, sirviendo como controles sanos. A continuación, permitieron que los ratones crecieran durante seis semanas, un periodo aproximadamente equivalente a una etapa juvenil, antes de examinar detalladamente su salud y comportamiento. 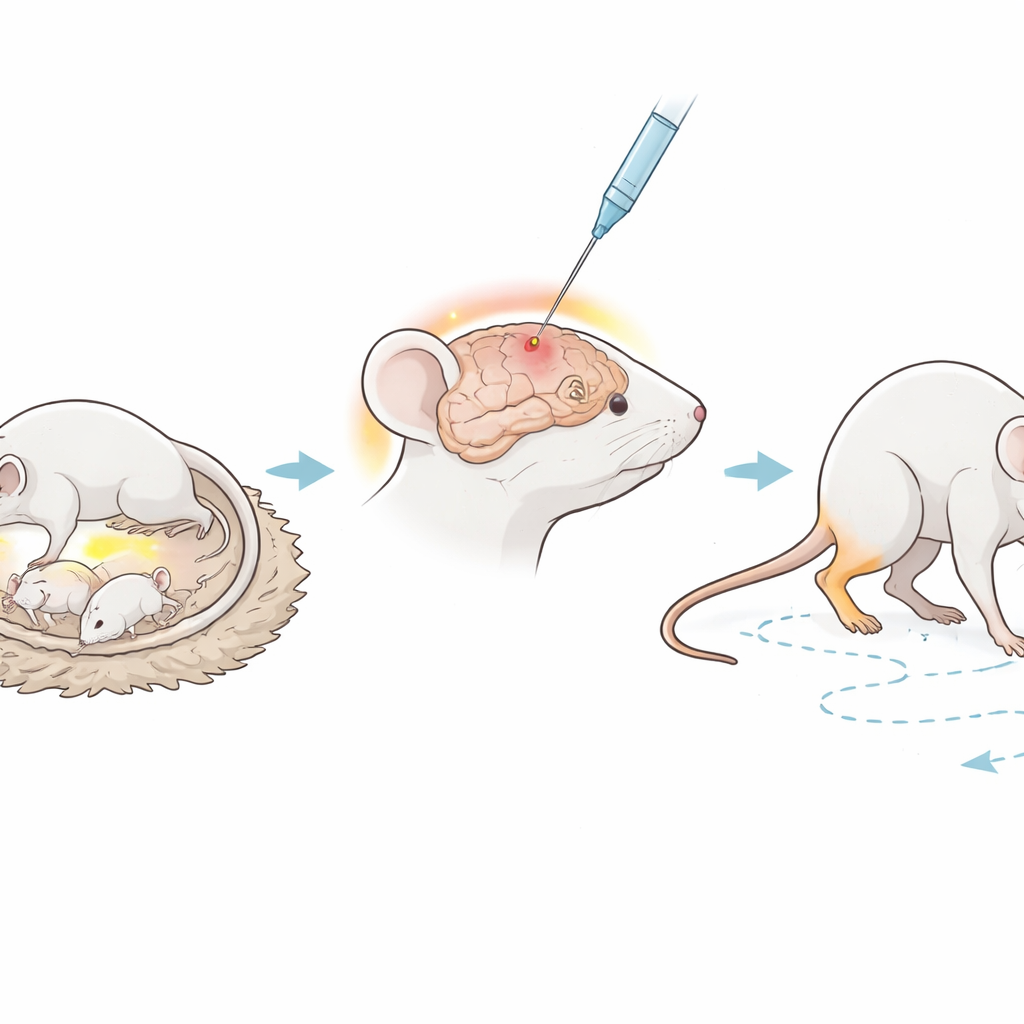
Signos de crecimiento deficiente y movimiento desigual
En comparación con los animales control, menos ratones tratados con LPS sobrevivieron hasta el final del estudio, y los que sobrevivieron pesaron menos, lo que sugiere que la lesión cerebral temprana afectó el desarrollo general. Cuando los investigadores evaluaron movimientos básicos, encontraron que los ratones tratados con LPS mostraron un claro desequilibrio: al sujetarlos suavemente por la cola, sus cuerpos se inclinaban más a un lado, y en una barra giratoria se caían antes, lo que indica una reducción del equilibrio y la resistencia. En un campo abierto, estos ratones caminaban más despacio y recorrieron menos distancia en conjunto, un patrón conocido como hipolocomoción. Curiosamente, aunque no pasaron más tiempo en el centro del recinto, una mayor proporción del poco movimiento que realizaron tuvo lugar allí, lo que sugiere cambios en los patrones de exploración más que simples variaciones en la ansiedad.
Cambios en la marcha que evocan los problemas de la deambulación en niños
Los hallazgos más llamativos provinieron del análisis de la marcha por computadora, que mide cómo se mueve cada pata mientras el ratón camina sobre una cinta transparente. Los ratones tratados con LPS caminaron más despacio, con ciclos de paso más largos y menos pasos por segundo. Sus extremidades traseras se vieron especialmente afectadas: pasaban más tiempo en contacto con la cinta y empujaban durante más tiempo, pero su base de apoyo se volvió más estrecha. El ángulo de las patas traseras aumentó, asemejándose a las posiciones hacia dentro y tipo tijera que suelen observarse en niños con parálisis cerebral espástica dipléjica. Al mismo tiempo, las patas delanteras mostraron cambios diferentes, subrayando una reorganización compleja de la coordinación entre las extremidades delanteras y traseras. En conjunto, estos patrones indican un trastorno del movimiento multifacético dominado por anomalías en las patas traseras, que paralelamente reflejan los problemas centrados en las extremidades inferiores en muchos niños con parálisis cerebral. 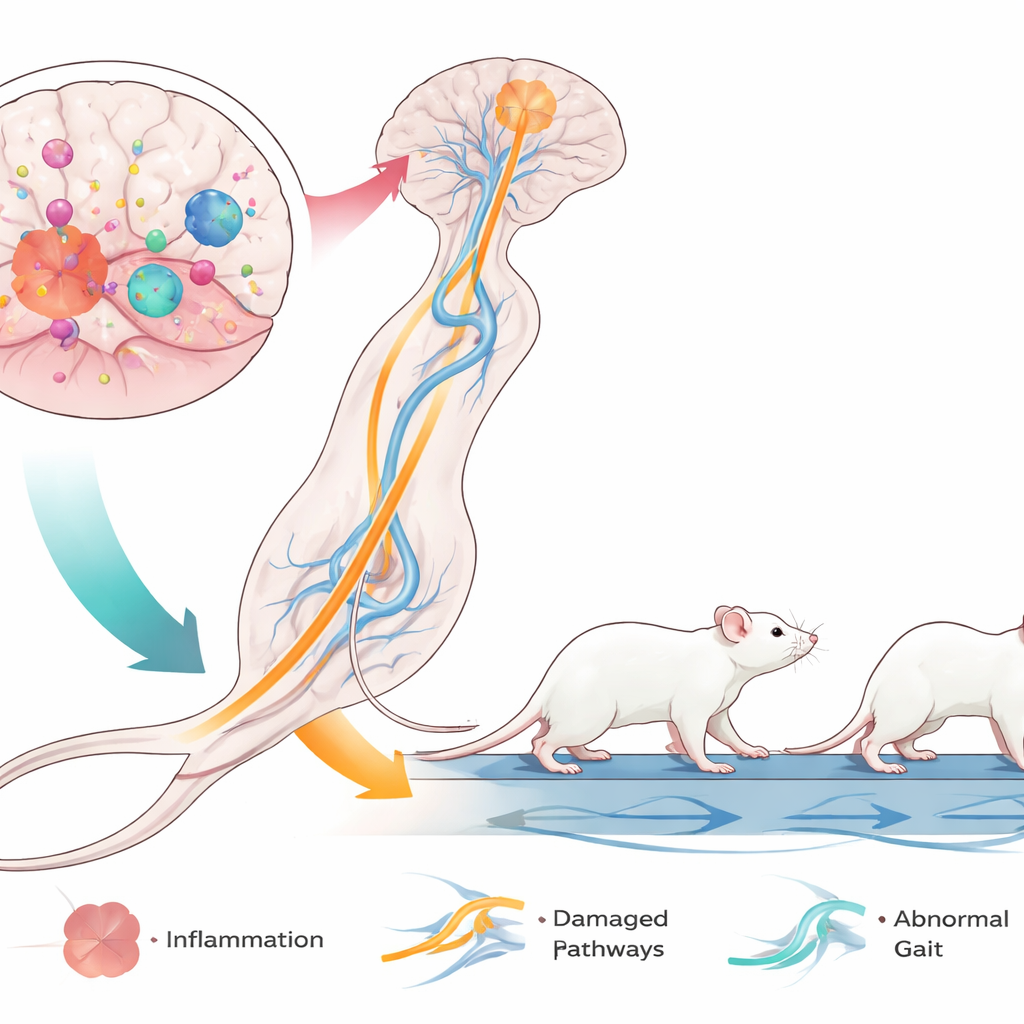
Qué puede estar ocurriendo dentro del cerebro
Aunque este estudio no midió directamente las células cerebrales, se basa en trabajos anteriores que sugieren que el LPS desencadena una respuesta inflamatoria agresiva en las células inmunitarias residentes del cerebro, llamadas microglía. Estas células activadas pueden dañar la vaina aislante alrededor de las fibras nerviosas—especialmente en las regiones de materia blanca que transmiten señales desde los centros motores del cerebro hasta la médula espinal y las piernas. Dado que los ratones carecen de células inmunitarias adaptativas pero aún conservan respuestas inmunes innatas, el modelo aísla cómo la inflamación temprana por sí sola puede alterar las vías motoras al tiempo que permanece compatible con trasplantes de células humanas. Los déficits centrados en las extremidades traseras apuntan a que regiones cerebrales y conexiones específicas para las patas traseras son particularmente vulnerables a este tipo de insulto en la primera etapa de la vida.
Qué significa esto para futuras terapias
En términos sencillos, los investigadores crearon ratones jóvenes cuyos problemas de movimiento se parecen y se comportan de forma muy parecida a una forma de parálisis cerebral en niños, afectando especialmente a las piernas, y lo hicieron en animales que pueden albergar con seguridad células humanas. Este nuevo modelo no captura todos los aspectos de la condición humana, pero ofrece una plataforma realista y éticamente refinada para explorar cómo la inflamación temprana lesiona el cerebro en desarrollo y para probar si tratamientos experimentales—especialmente terapias basadas en células humanas y otras células—pueden restaurar un movimiento más normal. Si emergen terapias exitosas en este contexto, es más probable que se traduzcan en mejoras significativas para los niños que viven con parálisis cerebral.
Cita: Yang, J., Li, Y., Shi, C. et al. Intracranial LPS injection induces cerebral palsy-like motor and behavioral deficits in immunodeficient mice. Sci Rep 16, 10105 (2026). https://doi.org/10.1038/s41598-026-40909-5
Palabras clave: parálisis cerebral, neuroinflamación, modelos animales, anomalías de la marcha, terapia celular