Clear Sky Science · de
Intrakranielle LPS-Injektion erzeugt zerebralpareseähnliche motorische und Verhaltensdefizite bei immundefizienten Mäusen
Warum diese Forschung wichtig ist
Zerebralparese ist eine der häufigsten Ursachen für lebenslange Bewegungsstörungen bei Kindern, dennoch fehlen Ärzten weiterhin Behandlungen, die das verletzte Gehirn wirklich reparieren können. Viele vielversprechende Ansätze, etwa Stammzelltherapien, müssen zunächst an Tieren getestet werden. Standard-Labororganismen wehren jedoch häufig menschliche Zellen ab, was es schwer macht vorherzusagen, ob eine Therapie bei Kindern funktionieren wird. Diese Studie stellt ein neues Mausmodell vor, das die wichtigsten Bewegungsstörungen der Zerebralparese eng nachbildet und gleichzeitig für menschliche Zellen kompatibel ist, und eröffnet so realistischere Testmöglichkeiten für zukünftige Therapien.
Aufbau eines speziellen Mausmodells
Das Team arbeitete mit neugeborenen immundefizienten Mäusen, denen wichtige Bestandteile des Immunsystems fehlen, die normalerweise fremde Zellen angreifen. Als die Jungen sechs Tage alt waren, injizierten die Forscher sorgfältig eine winzige Menge Lipopolysaccharid (LPS) — ein Molekül, das auf bestimmten Bakterien vorkommt — direkt in eine weißsubstantielle Region des Gehirns. LPS wird in der Forschung häufig verwendet, weil es zuverlässig eine Entzündung auslöst, ähnlich jener, die bei einer schweren Infektion vor oder kurz nach der Geburt auftreten kann, einem bekannten Risikofaktor für Zerebralparese. Eine zweite Gruppe von Jungen unterzog sich derselben Operation, erhielt jedoch nur Kochsalzlösung und diente als gesunde Kontrolle. Die Mäuse durften dann sechs Wochen heranwachsen, was ungefähr einem juvenilen Stadium entspricht, bevor Gesundheit und Verhalten detailliert untersucht wurden. 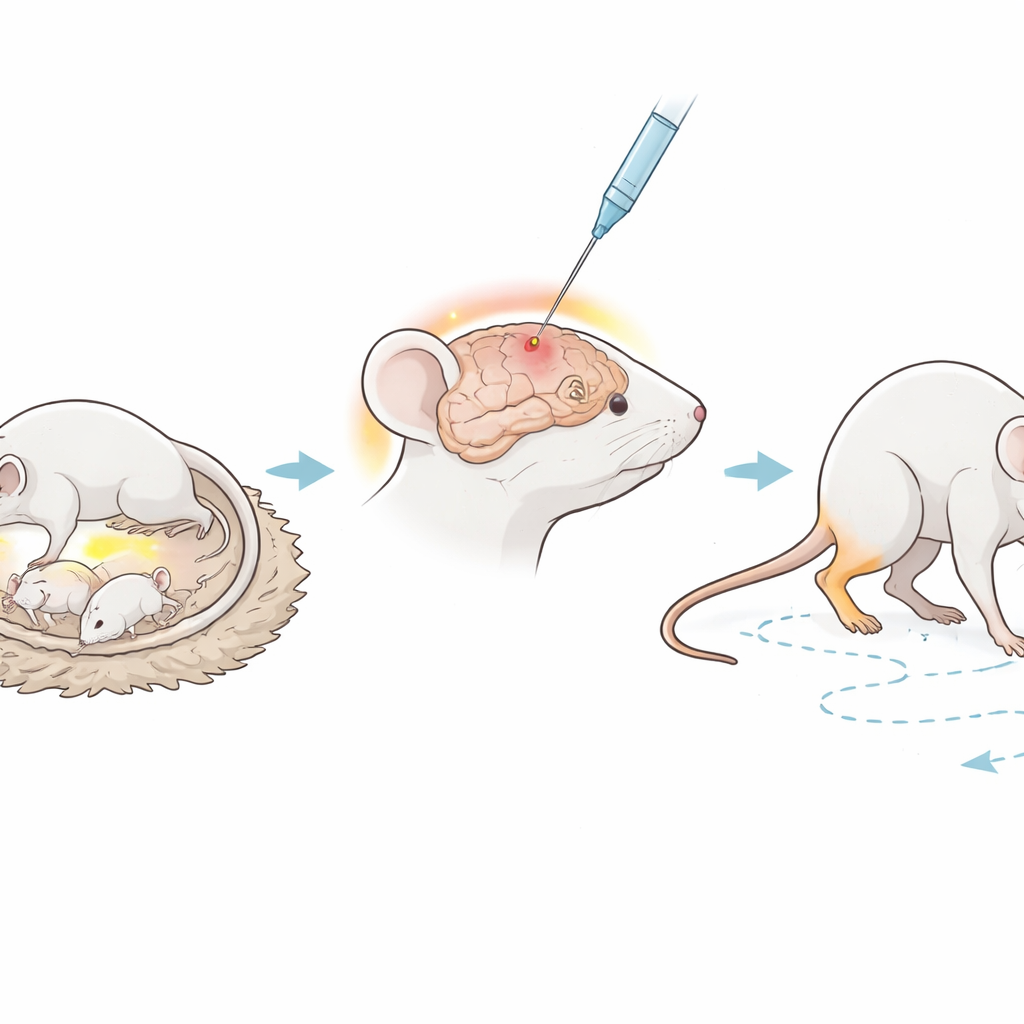
Anzeichen für vermindertes Wachstum und einseitige Bewegung
Im Vergleich zu Kontrolltieren überlebten weniger LPS-behandelte Mäuse bis zum Ende der Studie, und diejenigen, die überlebten, wogen weniger, was darauf hindeutet, dass der frühe Hirnschaden die allgemeine Entwicklung beeinträchtigte. Bei Tests grundlegender Bewegungsfunktionen zeigten die LPS-behandelten Mäuse ein deutliches Ungleichgewicht: Wenn sie vorsichtig am Schwanz gehalten wurden, schwangen ihre Körper häufiger zur einen Seite, und auf einer rotierenden Stange fielen sie früher herunter, was auf verminderte Balance und Ausdauer hinweist. In einer offenen Arena gingen diese Mäuse langsamer und legten insgesamt weniger Strecke zurück, ein Muster, das als Hypolokomotion bekannt ist. Interessanterweise verbrachten sie nicht mehr Zeit in der Arena-Mitte, doch ein größerer Anteil ihrer wenigen Bewegungen fand dort statt, was eher auf veränderte Erkundungsmuster als auf einfache Angstveränderungen hindeutet.
Gangveränderungen, die den Gehproblemen von Kindern ähneln
Die eindrücklichsten Befunde ergaben sich aus der computergestützten Ganganalyse, die misst, wie jede Pfote bewegt wird, während die Maus auf einem transparenten Laufband läuft. LPS-behandelte Mäuse liefen langsamer, mit längeren Schrittzyklen und weniger Schritten pro Sekunde. Besonders betroffen waren die Hinterbeine: Sie hatten längere Bodenkontaktzeiten und stärkere Abstoßphasen, während die Stützbasis schmaler wurde. Der Winkel der Hinterpfoten nahm zu und ähnelte damit dem nach innen drehenden, scherenartigen Fußstand, wie er oft bei Kindern mit spastischer Diplegie zu sehen ist. Gleichzeitig zeigten die Vorderpfoten andere Veränderungen, was auf eine komplexe Umgestaltung der Koordination zwischen Vorder- und Hintergliedmaßen hinweist. Zusammen deuten diese Muster auf eine vielschichtige Bewegungsstörung mit dominanten Defiziten der Hinterbeine hin, die den auf die unteren Gliedmaßen konzentrierten Problemen vieler Kinder mit Zerebralparese eng entspricht. 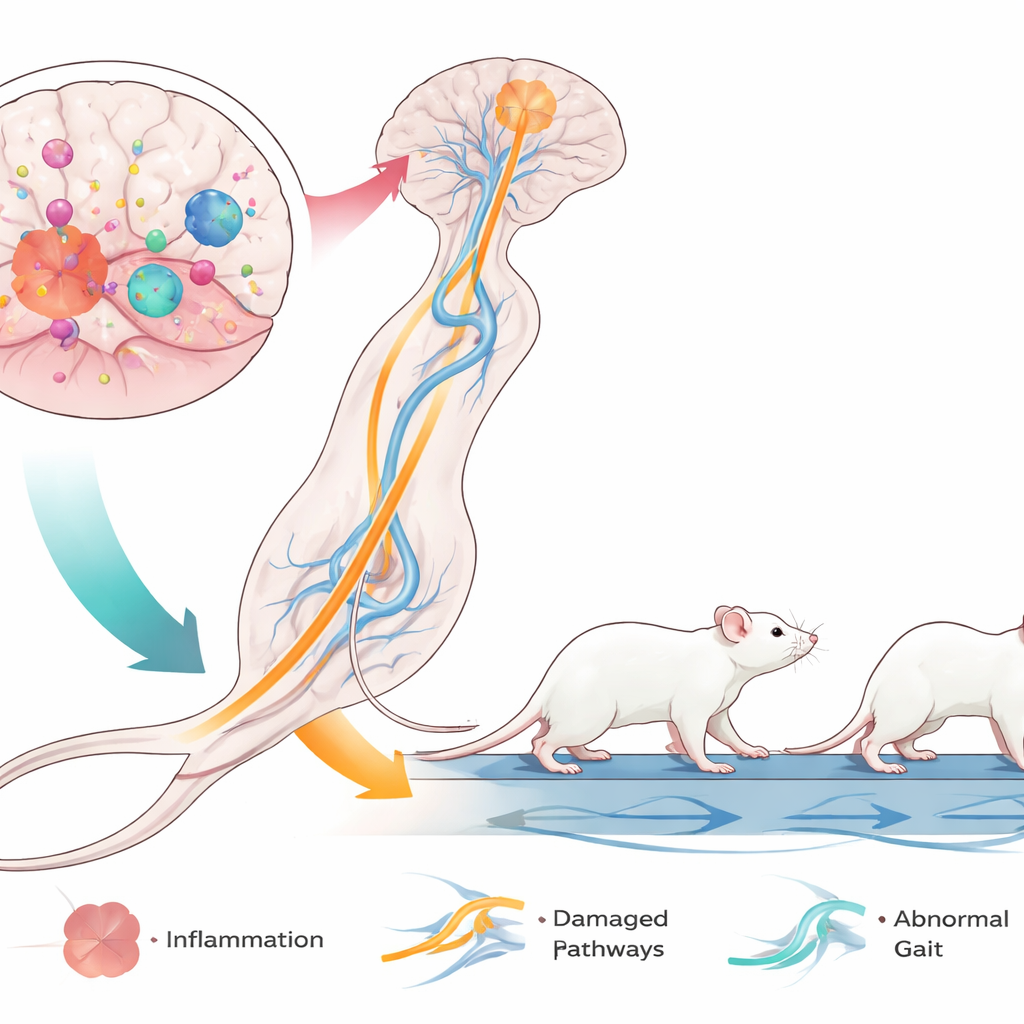
Was im Gehirn vor sich gehen könnte
Obwohl diese Studie die Hirnzellen nicht direkt untersuchte, stützt sie sich auf frühere Arbeiten, die darauf hindeuten, dass LPS eine aggressive Entzündungsreaktion in den im Gehirn ansässigen Immunzellen, den Mikroglia, auslöst. Diese aktivierten Zellen können die Isolierung um Nervenfasern schädigen — besonders in weißsubstantielle Bereichen, die Signale von den Bewegungszentren des Gehirns zum Rückenmark und zu den Beinen leiten. Da die Mäuse adaptive Immunzellen nicht haben, aber dennoch angeborene Immunantworten zeigen, isoliert das Modell, wie frühe Entzündung allein motorische Bahnen stören kann und gleichzeitig mit menschlichen Zelltransplantaten kompatibel bleibt. Die auf die Hinterbeine fokussierten Defizite deuten darauf hin, dass bestimmte Hirnregionen und Verschaltungen für die hinteren Gliedmaßen besonders verletzlich für diese Form einer frühkindlichen Schädigung sind.
Was das für künftige Therapien bedeutet
Vereinfacht gesagt schufen die Forschenden junge Mäuse, deren Bewegungsstörungen einem Formenkreis der Zerebralparese bei Kindern sehr ähnlich sind, insbesondere mit Beinbetonung, und das in Tieren, die menschliche Zellen aufnehmen können. Dieses neue Modell bildet nicht jeden Aspekt der menschlichen Erkrankung ab, bietet aber eine realistische und ethisch verfeinerte Plattform, um zu untersuchen, wie frühe Entzündungen das sich entwickelnde Gehirn schädigen, und um zu testen, ob experimentelle Behandlungen — insbesondere menschliche Stammzell- und andere zellbasierte Therapien — eine normalere Bewegung wiederherstellen können. Wenn in diesem Setting erfolgreiche Therapien entstehen, ist die Wahrscheinlichkeit größer, dass sie in sinnvolle Verbesserungen für Kinder mit Zerebralparese übersetzt werden können.
Zitation: Yang, J., Li, Y., Shi, C. et al. Intracranial LPS injection induces cerebral palsy-like motor and behavioral deficits in immunodeficient mice. Sci Rep 16, 10105 (2026). https://doi.org/10.1038/s41598-026-40909-5
Schlüsselwörter: Zerebralparese, Neuroinflammation, Tiermodelle, Gangstörungen, Zelltherapie