Clear Sky Science · sv
Testning av spermiedna-fragmentering för att förutse IVF- och PGT-A-resultat
Varför detta är viktigt för par som försöker bli gravida
När in vitro-fertilisering (IVF) misslyckas riktas uppmärksamheten ofta mot kvinnans ålder, hormoner eller livmoder. Men denna studie granskar noggrant den ofta förbisedd andra halvan av ekvationen: mannens spermier. Mer specifikt undersöks om små brott i spermiedna — för små för att se i ett vanligt mikroskop — kan förutsäga vilka embryon som blir friska och vilka IVF-försök som leder till ett barn, även när embryon noggrant screenas med avancerad genetisk testning.
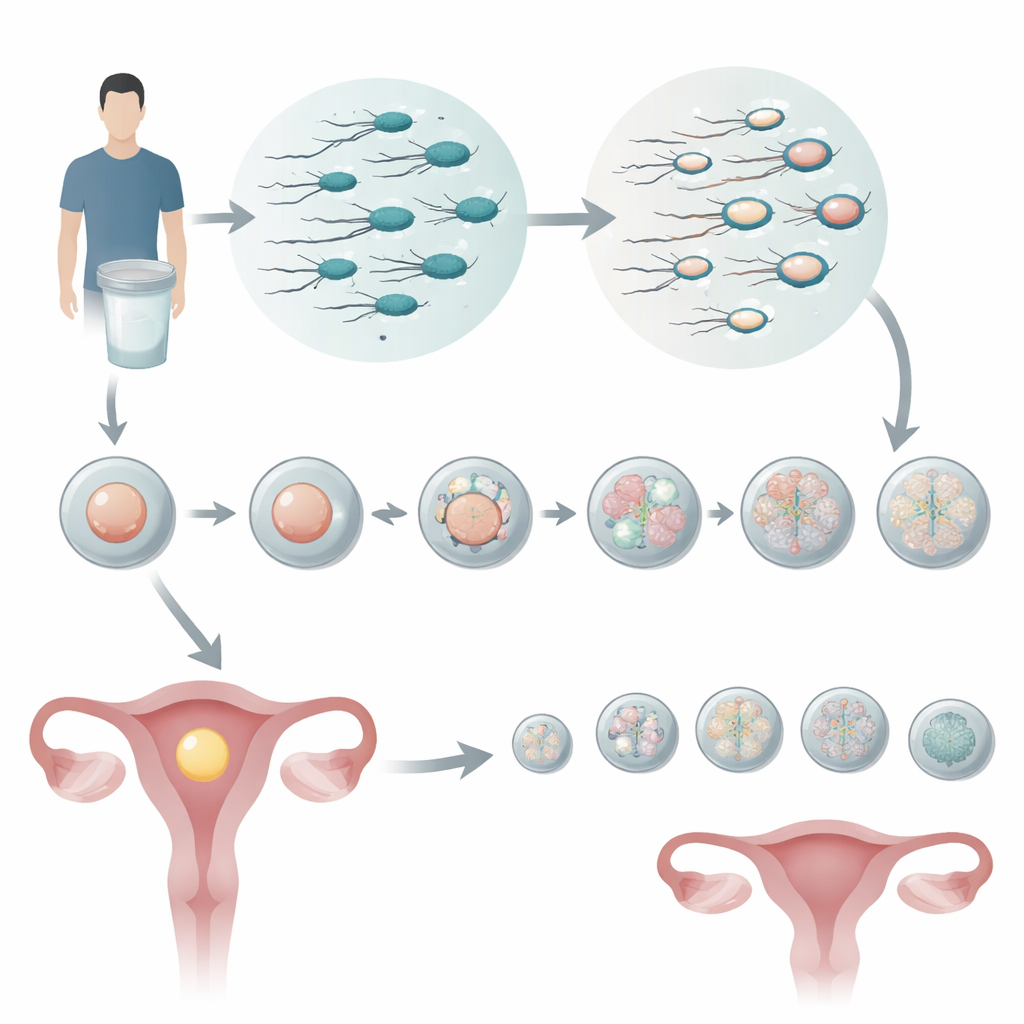
Att se bortom en enkel spermieräkning
De flesta fertilitetskliniker bedömer spermier främst efter antal, rörlighet och utseende. Dessa mått är användbara men grova, och två prover som ser likadana ut på papper kan bete sig mycket olika i laboratoriet. Forskarna fokuserade på en mer subtil egenskap: hur intakt spermiednat är. De använde ett test som mäter DNA fragmentation index (DFI) — i princip andelen spermier vars genetiska material är skadat. Männen delades in i låg, medel och hög DFI och deras partners genomgick IVF tillsammans med preimplantation genetic testing for aneuploidy (PGT-A), en teknik som kontrollerar embryon för felaktigt kromosomantal innan överföring.
Hur studien genomfördes
Teamet följde 124 par som behandlades vid ett enda fertilitetscenter. Alla män genomgick ett DFI-test och alla par genomgick IVF-cykler där embryon odlades till blastocyststadiet, biopsierades och analyserades med next-generation sequencing. Detta gjorde det möjligt för forskarna att koppla varje mans DFI-nivå till flera viktiga steg: befruktning av ägg (antingen med konventionell IVF eller spermieinjektion), antal och kvalitet på bildade blastocyster, andelen kromosomavvikelser som upptäcktes av PGT-A, och verkliga utfall såsom implantation, klinisk graviditet och levande födsel efter överföring av kromosomalt normala embryon.
Vad spermiedna-skador påverkade och inte påverkade
Män med hög DFI tenderade att vara äldre och hade sämre spermierörlighet. I dessa fall med hög DFI var befruktningsgraden lägre när en enskild spermie injicerades direkt i ägget (ICSI), och färre embryon utvecklades till blastocyster av god kvalitet lämpliga för nedfrysning. Detta tyder på att synliga spermieegenskaper som rörlighet och form inte fullt ut avslöjar djupare DNA-problem. När forskarna tittade på PGT-A-resultaten framkom dock en överraskning: andelen embryon med normalt, mosaic eller abnormt kromosomantal var liknande i grupperna med låg, medel och hög DFI. Med andra ord, bland de embryon som överlevde till biopsi översattes inte ett ursprung från mer skadade spermier tydligt till fler kromosomfel.
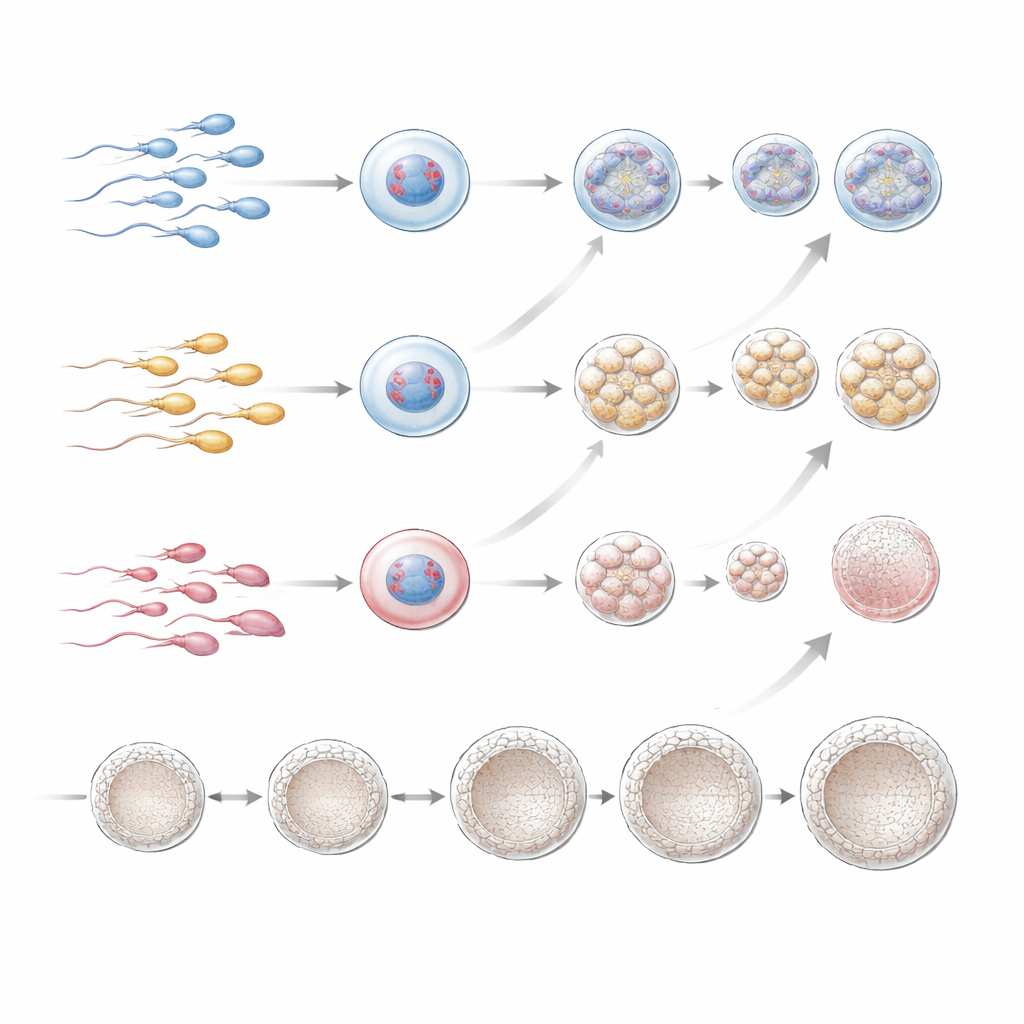
Do skadade spermier dömer IVF-försök?
För att besvara den fråga par bryr sig mest om följde teamet vad som hände efter överföring av embryon som PGT-A hade klassat som kromosomalt normala (eller med låggradig mosaicism). Implantations-, graviditets- och levande födsel-satser per embryoöverföring var i stora drag jämförbara mellan alla tre DFI-grupper, även i den lilla undergruppen med hög DFI. Medan hög DFI kopplades till färre bra embryon i frysen, verkade sannolikheten att ett chromosomalt normalt och välutvecklat blastocyst ändå skulle leda till ett barn inte starkt påverkas av hur fragmenterat faderns spermiedna varit i ursprungsprovet. Författarna varnar dock för att studien var retrospektiv, omfattade en starkt selekterad grupp av främst äldre kvinnor och inkluderade relativt få män med mycket hög DFI, så subtila effekter kan ha missats.
Vad detta betyder för patienter och kliniker
För par är huvudbudskapet tvådelat. För det första kan en hög nivå av spermiedna-skada göra det svårare att nå stadiet med flera bra embryon att välja mellan, och det kan måttligt minska framgång vid befruktning och tidig utveckling. För det andra, om IVF ändå ger kromosomalt normala embryon, kan dessa embryon fortfarande implantat och ge upphov till barn i liknande utsträckning som embryon från män med lägre DFI, möjligen eftersom ägget och det tidiga embryot kan reparera viss paternell DNA-skada. Författarna föreslår att testning av spermiedna-fragmentering används som ett kompletterande verktyg — inte för att utesluta behandling, utan för att identifiera manliga faktorer, vägleda spermievalsmetoder och förfina IVF-strategier som syftar till att öka antalet och kvaliteten på embryon tillgängliga för överföring.
Citering: Okubo, T., Kobayashi, T., Hayashi, T. et al. The role of sperm DNA fragmentation testing in predicting IVF and PGT-A outcomes. Sci Rep 16, 14607 (2026). https://doi.org/10.1038/s41598-026-38974-x
Nyckelord: manlig infertilitet, spermiedna-fragmentering, IVF-resultat, embryogenetisk testning, blastocystutveckling