Clear Sky Science · es
El papel de la prueba de fragmentación del ADN espermático para predecir los resultados de la FIV y PGT-A
Por qué importa a las parejas que intentan concebir
Cuando la fecundación in vitro (FIV) no funciona, la atención suele centrarse en la edad de la mujer, sus hormonas o el útero. Pero este estudio examina de cerca la otra mitad de la ecuación, a menudo descuidada: el esperma del hombre. En concreto, plantea si pequeñas roturas en el ADN espermático —demasiado pequeñas para verse con un microscopio convencional— pueden predecir qué embriones serán sanos y qué intentos de FIV conducirán a un bebé, incluso cuando los embriones se someten a cribado genético avanzado.
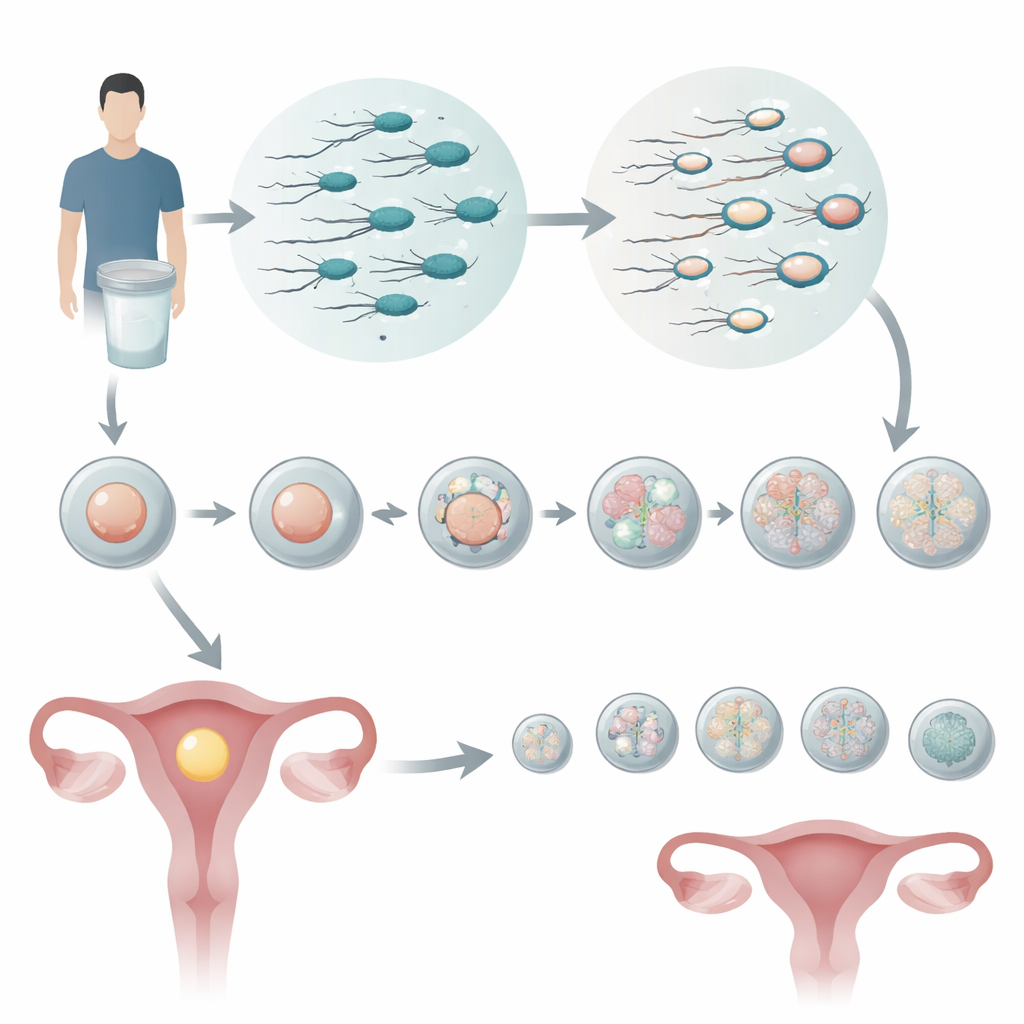
Mirando más allá de un recuento básico de espermatozoides
La mayoría de las clínicas de fertilidad evalúan el esperma principalmente por su recuento, su movilidad y su morfología. Estas medidas son útiles pero toscas, y dos muestras que parecen similares en el papel pueden comportarse de forma muy distinta en el laboratorio. Los investigadores se centraron en una característica más sutil: la integridad del ADN del esperma. Utilizaron una prueba que mide el índice de fragmentación del ADN (DFI), es decir, el porcentaje de espermatozoides cuyo material genético está roto. Los hombres se agruparon en DFI bajo, medio y alto, y sus parejas se sometieron a FIV junto con un test de diagnóstico genético preimplantacional para aneuploidías (PGT-A), una técnica que comprueba si los embriones tienen un número incorrecto de cromosomas antes de la transferencia.
Cómo se llevó a cabo el estudio
El equipo siguió a 124 parejas tratadas en un único centro de fertilidad. Todos los hombres se sometieron a la prueba de DFI y todas las parejas pasaron por ciclos de FIV en los que los embriones se cultivaron hasta la etapa de blastocisto, se biopsiaron y se analizaron mediante secuenciación de nueva generación. Esto permitió a los científicos relacionar el nivel de DFI de cada hombre con varios pasos clave: la fertilización de los óvulos (tanto por FIV convencional como por inyección intracitoplasmática de espermatozoides, ICSI), el número y la calidad de los blastocistos formados, la tasa de anomalías cromosómicas detectadas por PGT-A y resultados reales como la implantación, el embarazo clínico y el nacimiento vivo tras la transferencia de embriones cromosómicamente normales.
Qué afectó y qué no la lesión del ADN espermático
Los hombres con DFI alto tendían a ser mayores y tenían peor motilidad espermática. En estos casos de DFI alto, las tasas de fertilización fueron más bajas cuando se inyectó directamente un único espermatozoide en el óvulo (ICSI), y menos embriones evolucionaron hasta convertirse en blastocistos de buena calidad aptos para la congelación. Esto sugiere que rasgos espermáticos visibles como el movimiento y la forma no revelan por completo problemas de ADN más profundos. Sin embargo, al analizar los resultados de PGT-A surgió una sorpresa: la proporción de embriones con número de cromosomas normal, mosaico o anómalo fue similar en los grupos de DFI bajo, medio y alto. En otras palabras, entre los embriones que sobrevivieron hasta la biopsia, partir de esperma más dañado no se tradujo claramente en más errores cromosómicos.
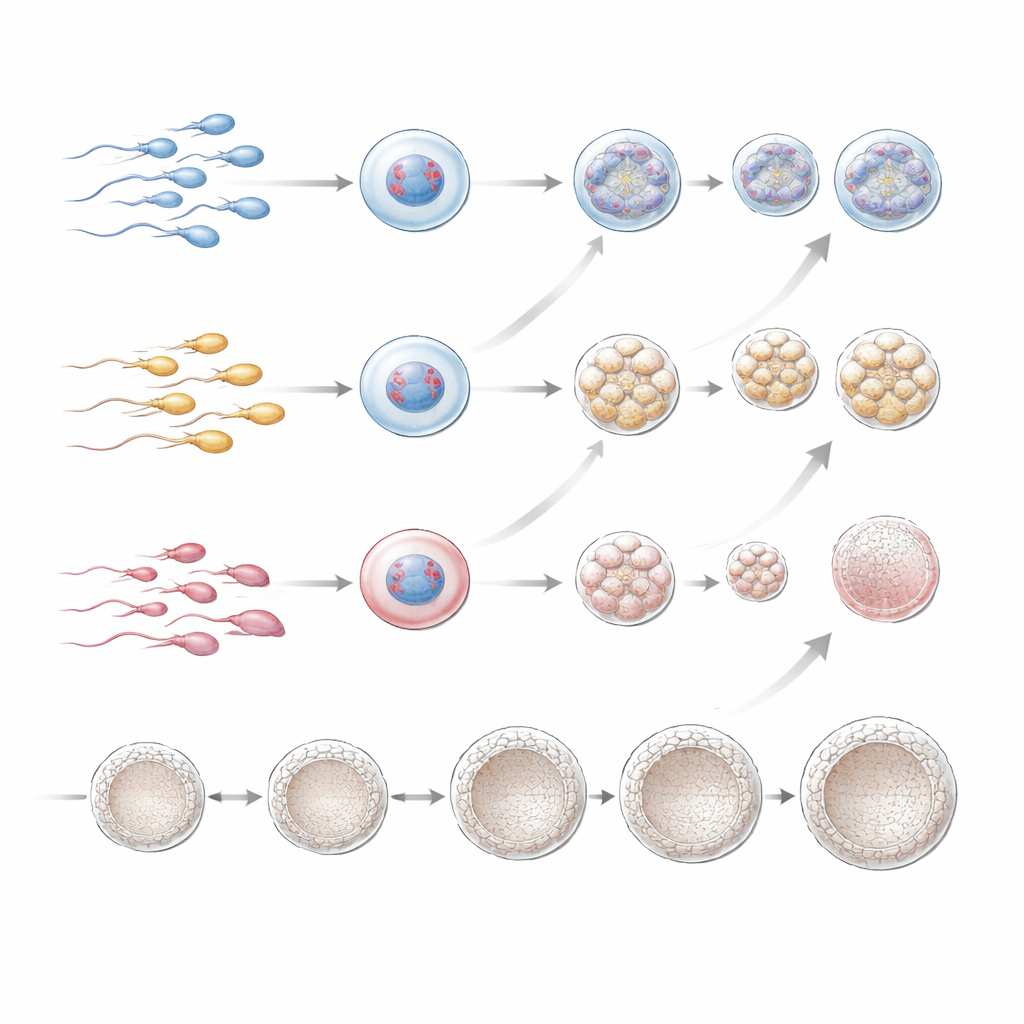
¿Condenan los espermatozoides dañados los intentos de FIV?
Para responder a la pregunta que más preocupa a las parejas, el equipo siguió lo que ocurrió tras la transferencia de embriones que PGT-A había calificado como cromosómicamente normales (o mosaicos de bajo nivel). Las tasas de implantación, embarazo y nacimiento vivo por transferencia embrionaria fueron, en general, comparables entre los tres grupos de DFI, incluso en el pequeño subgrupo de DFI alto. Aunque el DFI alto se asoció con menos embriones buenos en el banco, una vez que existía un blastocisto con apariencia sana y cromosómicamente normal, su probabilidad de dar lugar a un bebé no pareció estar fuertemente influida por el grado de fragmentación del ADN del padre en la muestra original. Los autores advierten, sin embargo, que su estudio fue retrospectivo, incluyó un grupo muy seleccionado de mujeres en su mayoría de edad avanzada y hubo relativamente pocos hombres con DFI muy alto, por lo que podrían haberse pasado por alto efectos sutiles.
Qué significa esto para pacientes y clínicas
Para las parejas, la conclusión es doble. Primero, un nivel elevado de daño del ADN espermático puede dificultar alcanzar la etapa de disponer de múltiples embriones buenos entre los que elegir, y puede reducir modestamente el éxito en la fertilización y el desarrollo temprano. Segundo, si la FIV produce embriones cromosómicamente normales, esos embriones aún pueden implantarse y producir bebés a tasas similares a las de hombres con DFI más bajo, posiblemente porque el óvulo y el embrión temprano pueden reparar parte del daño del ADN paterno. Los autores sugieren usar la prueba de fragmentación del ADN espermático como una herramienta adicional, no para descartar el tratamiento, sino para identificar problemas de factor masculino, guiar métodos de selección de esperma y perfeccionar estrategias de FIV destinadas a mejorar el número y la calidad de embriones disponibles para la transferencia.
Cita: Okubo, T., Kobayashi, T., Hayashi, T. et al. The role of sperm DNA fragmentation testing in predicting IVF and PGT-A outcomes. Sci Rep 16, 14607 (2026). https://doi.org/10.1038/s41598-026-38974-x
Palabras clave: infertilidad masculina, fragmentación del ADN espermático, resultados de la FIV, pruebas genéticas de embriones, desarrollo de blastocistos