Clear Sky Science · nl
De rol van sperma-DNA-fragmentatietests bij het voorspellen van IVF- en PGT-A-uitkomsten
Waarom dit belangrijk is voor stellen die proberen zwanger te worden
Wanneer in-vitrofertilisatie (IVF) niet werkt, ligt de aandacht vaak bij de leeftijd van de vrouw, hormonen of de baarmoeder. Deze studie richt zich echter op het vaak over het hoofd geziene andere deel van de vergelijking: het sperma van de man. Concreet onderzoekt ze of kleine breuken in het sperma-DNA — te klein om onder een gewone microscoop te zien — kunnen voorspellen welke embryo’s gezond zullen zijn en welke IVF-pogingen tot een baby leiden, zelfs wanneer embryo’s zorgvuldig worden gescreend met geavanceerde genetische testen.
Voorbij de basale spermatelling kijken
De meeste vruchtbaarheidsklinieken beoordelen sperma vooral op aantal, zwemvermogen en uiterlijke normaliteit. Die metingen zijn nuttig maar grof, en twee monsters die op papier vergelijkbaar lijken, kunnen zich in het laboratorium heel verschillend gedragen. De onderzoekers concentreerden zich op een subtieler kenmerk: hoe intact het sperma-DNA is. Ze gebruikten een test die de DNA-fragmentatie-index (DFI) meet — in feite het percentage zaadcellen waarvan het genetisch materiaal beschadigd is. Mannen werden in lage, middelmatige en hoge DFI-groepen ingedeeld en hun partners ondergingen allemaal IVF met pre-implantatie genetische testing op aneuploidie (PGT-A), een techniek die embryo’s controleert op een afwijkend aantal chromosomen vóór terugplaatsing.
Hoe de studie werd uitgevoerd
Het team volgde 124 stellen die behandeld werden in één vruchtbaarheidscentrum. Alle mannen ondergingen een DFI-test en alle paren doorliepen IVF-cycli waarbij embryo’s tot het blastocyststadium werden gekweekt, gebiopserd en geanalyseerd met next-generation sequencing. Dat stelde de onderzoekers in staat om het DFI-niveau van elke man te koppelen aan verschillende belangrijke stappen: bevruchting van eicellen (door conventionele IVF of intracytoplasmatische sperma-injectie), het aantal en de kwaliteit van gevormde blastocysten, het percentage chromosomale afwijkingen gedetecteerd door PGT-A, en klinische uitkomsten zoals implantatie, klinische zwangerschap en levendgeboorte na terugplaatsing van chromosomaal normale embryo’s.
Wat sperma-DNA-schade wel en niet beïnvloedde
Mannen met een hoge DFI waren doorgaans ouder en hadden slechtere spermamotiliteit. Bij deze hoge-DFI-gevallen waren de bevruchtingspercentages lager wanneer een enkele zaadcel direct in de eicel werd geïnjecteerd (ICSI), en ontwikkelden minder embryo’s zich tot goed-kwalitatieve blastocysten die geschikt waren om ingevroren te worden. Dit suggereert dat zichtbare sperma-eigenschappen zoals beweging en vorm niet volledig dieperliggende DNA-problemen onthullen. Toch bleek bij de PGT-A-resultaten een verrassing: het aandeel embryo’s met normale, mosaïek- of afwijkende chromosoomaantallen was vergelijkbaar in de lage, middelmatige en hoge DFI-groepen. Met andere woorden, onder embryo’s die het tot biopsie haalden, vertaalde het starten met meer beschadigd sperma zich niet duidelijk in meer chromosomale fouten.
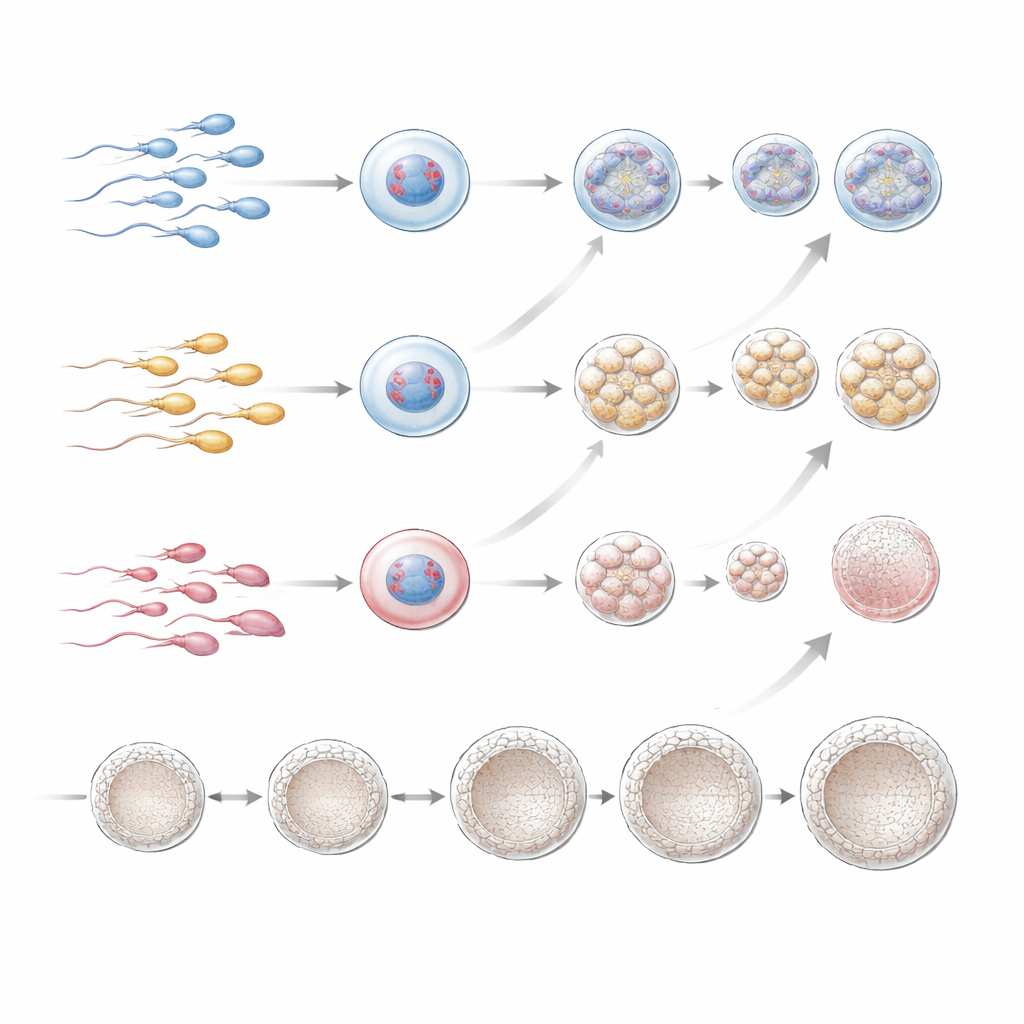
Zetten beschadigde zaadcellen IVF-pogingen op voor verlies?
Om de vraag te beantwoorden die stellen het meest bezighoudt, volgde het team wat er gebeurde na terugplaatsing van embryo’s die door PGT-A als chromosomaal normaal (of laag-niveau mosaïek) waren aangemerkt. Implantatie-, zwangerschap- en levendgeboortepercentages per embryo-terugplaatsing waren in grote lijnen vergelijkbaar tussen alle drie DFI-groepen, zelfs in de kleine subgroep met hoge DFI. Hoewel hoge DFI gekoppeld was aan minder goede embryo’s in de vriezer, leek eenmaal een gezond-ogende, chromosomaal normale blastocyst aanwezig was de kans dat deze tot een baby leidde niet sterk beïnvloed door de mate van fragmentatie in het oorspronkelijke sperma-monster van de vader. De auteurs waarschuwen echter dat hun studie retrospectief was, een sterk geselecteerde groep voornamelijk oudere vrouwen omvatte en relatief weinig mannen met zeer hoge DFI bevatte, zodat subtiele effecten over het hoofd zouden kunnen zijn gezien.
Wat dit betekent voor patiënten en klinieken
Voor stellen is de belangrijkste conclusie tweeledig. Ten eerste kan een hoog niveau van sperma-DNA-schade het moeilijker maken om het stadium te bereiken waarin meerdere goede embryo’s beschikbaar zijn om uit te kiezen, en het kan het succes bij bevruchting en vroege ontwikkeling enigszins verminderen. Ten tweede, als IVF toch chromosomaal normale embryo’s oplevert, kunnen die embryo’s nog steeds implantaatgoed en baby’s voortbrengen tegen percentages vergelijkbaar met die van mannen met lagere DFI, mogelijk omdat de eicel en het vroege embryo enige vaderlijke DNA-schade kunnen herstellen. De auteurs stellen voor om sperma-DNA-fragmentatietests te gebruiken als een aanvullend instrument — niet om behandeling uit te sluiten, maar om mannelijke factoren te identificeren, methoden voor spermaselectie te sturen en IVF-strategieën te verfijnen die gericht zijn op het verbeteren van het aantal en de kwaliteit van embryo’s die voor terugplaatsing beschikbaar zijn.
Bronvermelding: Okubo, T., Kobayashi, T., Hayashi, T. et al. The role of sperm DNA fragmentation testing in predicting IVF and PGT-A outcomes. Sci Rep 16, 14607 (2026). https://doi.org/10.1038/s41598-026-38974-x
Trefwoorden: mannelijke onvruchtbaarheid, spermatozoïd DNA-fragmentatie, IVF-uitkomsten, embryogenetische testen, blastocystontwikkeling