Clear Sky Science · de
Die Rolle des Tests auf Spermien-DNA-Fragmentierung zur Vorhersage von IVF- und PGT-A-Ergebnissen
Warum das für Paare, die schwanger werden wollen, wichtig ist
Wenn eine In-vitro-Fertilisation (IVF) nicht gelingt, richtet sich die Aufmerksamkeit oft auf das Alter der Frau, ihre Hormone oder die Gebärmutter. Diese Studie widmet sich jedoch der häufig übersehenen anderen Hälfte der Gleichung: den Spermien des Mannes. Konkret untersucht sie, ob winzige Brüche in der Spermien-DNA – zu klein, um sie mit einem normalen Mikroskop zu sehen – vorhersagen können, welche Embryonen gesund sind und welche IVF-Versuche zu einem Kind führen, selbst wenn die Embryonen mit fortschrittlichen genetischen Tests sorgfältig untersucht werden.
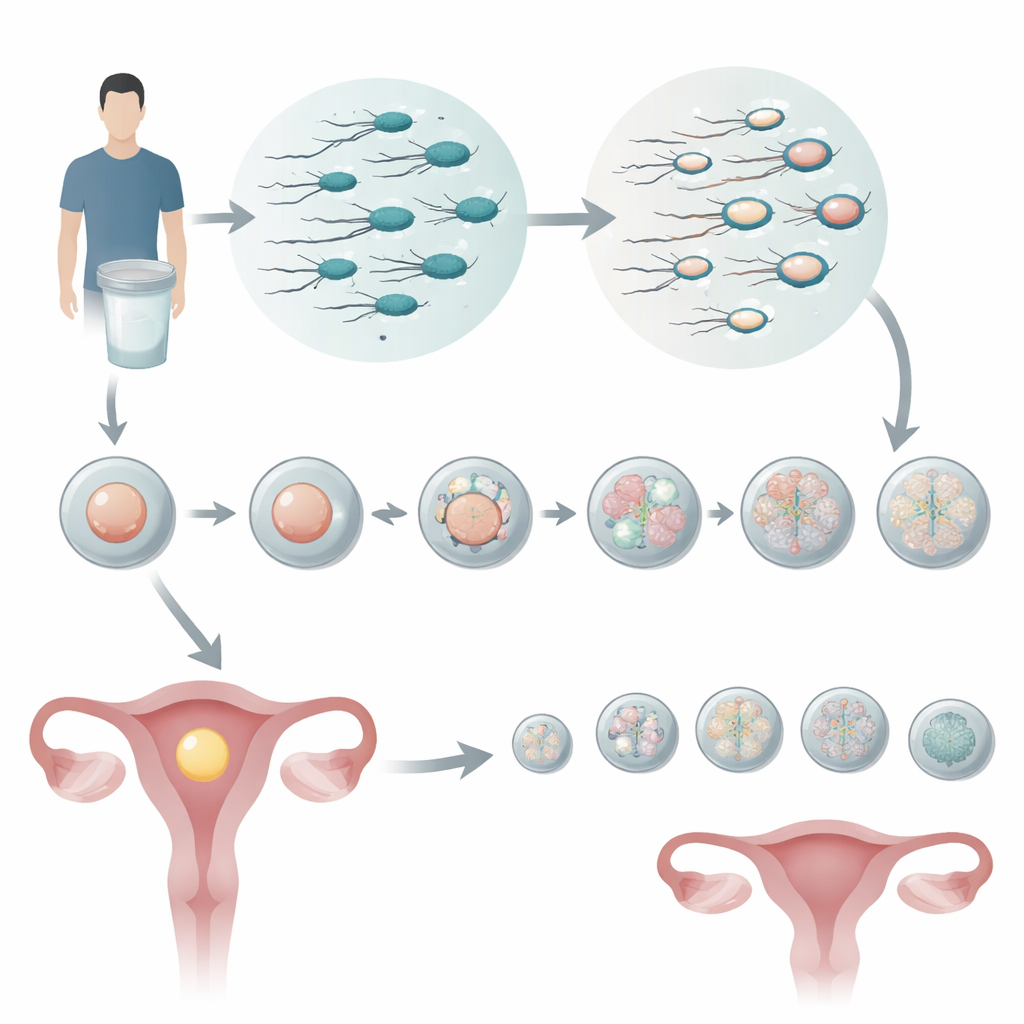
Über einen einfachen Spermiogramm-Blick hinaus
Die meisten Kinderwunschzentren beurteilen Spermien hauptsächlich nach Anzahl, Beweglichkeit und äußerlichem Erscheinungsbild. Diese Messgrößen sind nützlich, aber grob, und zwei Proben, die auf dem Papier ähnlich aussehen, können im Labor sehr unterschiedlich reagieren. Die Forschenden konzentrierten sich auf ein subtileres Merkmal: wie intakt die DNA der Spermien ist. Sie verwendeten einen Test, der den DNA-Fragmentierungsindex (DFI) misst — im Wesentlichen den Prozentsatz der Spermien mit gebrochener genetischer Substanz. Männer wurden in niedrige, mittlere und hohe DFI-Gruppen eingeteilt, und ihre Partnerinnen unterzogen sich alle einer IVF-Behandlung zusammen mit einer präimplantationsdiagnostischen Untersuchung auf Aneuploidie (PGT-A), einer Technik, die Embryonen vor dem Transfer auf falsche Chromosomenzahlen prüft.
Wie die Studie durchgeführt wurde
Das Team verfolgte 124 Paare, die an einem einzigen Kinderwunschzentrum behandelt wurden. Alle Männer hatten einen DFI-Test, und alle Paare durchliefen IVF-Zyklen, bei denen Embryonen bis zum Blastozystenstadium kultiviert, biopsiert und mittels Next-Generation-Sequencing analysiert wurden. Dadurch konnten die Forschenden den DFI-Wert jedes Mannes mit mehreren wichtigen Schritten verknüpfen: der Befruchtung der Eizellen (entweder durch konventionelle IVF oder intrazytoplasmatische Spermieninjektion), der Anzahl und Qualität der entstandenen Blastozysten, der Rate chromosomaler Abweichungen, die durch PGT-A entdeckt wurden, sowie realen Endpunkten wie Einnistung, klinischer Schwangerschaft und Lebendgeburt nach dem Transfer chromosomal normaler Embryonen.
Worauf sich Spermien-DNA-Schäden auswirkten und worauf nicht
Männer mit hohem DFI waren tendenziell älter und zeigten eine schlechtere Spermienmotilität. Bei diesen hoch-DFI-Fällen waren die Befruchtungsraten niedriger, wenn eine einzelne Samenzelle direkt in die Eizelle injiziert wurde (ICSI), und weniger Embryonen entwickelten sich zu Blastozysten von guter Qualität, die zum Einfrieren geeignet sind. Das deutet darauf hin, dass sichtbare Spermienmerkmale wie Bewegung und Form tiefere DNA-Probleme nicht vollständig offenbaren. Doch bei Betrachtung der PGT-A-Ergebnisse offenbarte sich eine Überraschung: der Anteil der Embryonen mit normaler, mosaikartiger oder abnormaler Chromosomenzahl war in den niedrigen, mittleren und hohen DFI-Gruppen ähnlich. Anders ausgedrückt: Unter den Embryonen, die bis zur Biopsie überlebten, ließ sich ausgehend von stärker beschädigten Spermien nicht eindeutig eine höhere Rate chromosomaler Fehler ableiten.
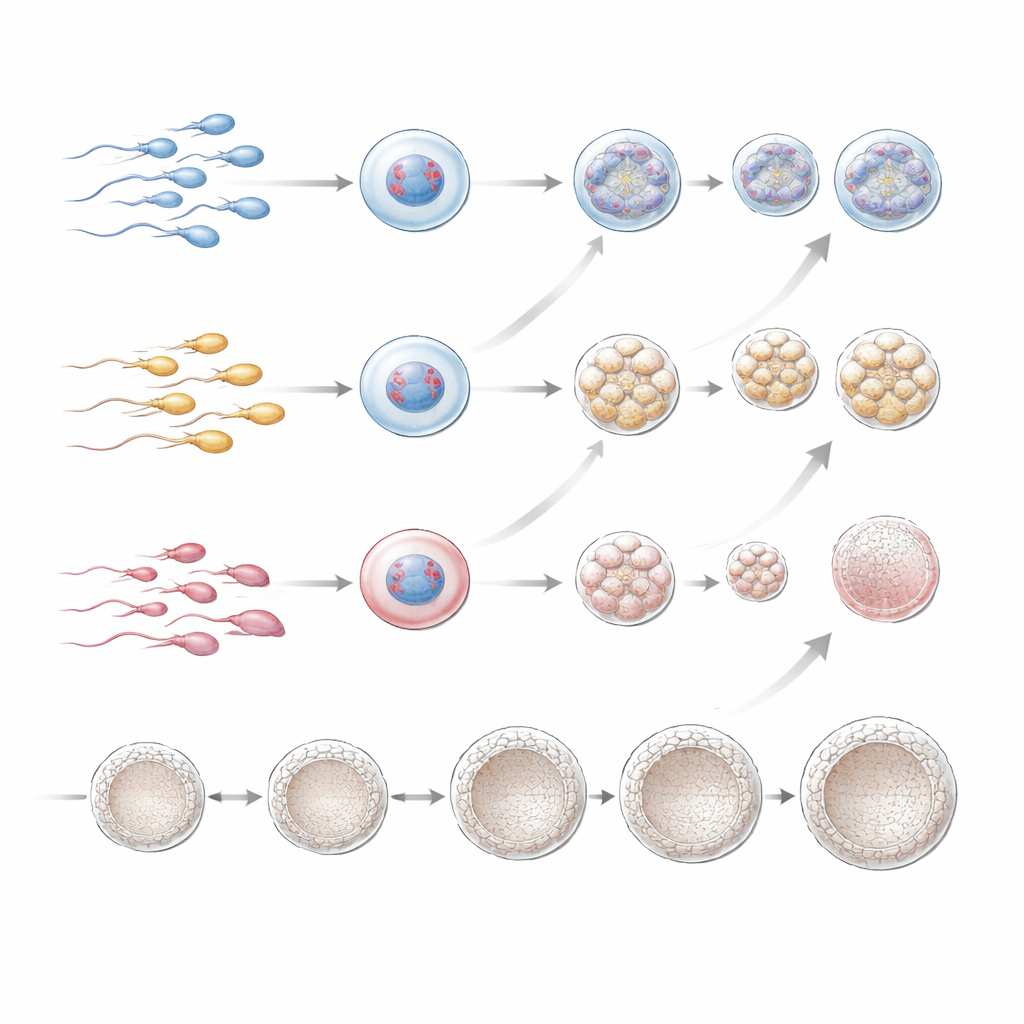
Verurteilen beschädigte Spermien IVF-Versuche zum Scheitern?
Um die Frage zu beantworten, die Paare am meisten interessiert, verfolgte das Team, was nach dem Transfer von Embryonen geschah, die von PGT-A als chromosomal normal (oder mit niedriggradiger Mosaikbildung) eingestuft worden waren. Die Raten von Einnistung, Schwangerschaft und Lebendgeburt pro Embryotransfer waren zwischen allen drei DFI-Gruppen weitgehend vergleichbar, sogar in der kleinen Hoch-DFI-Teilgruppe. Zwar war hoher DFI mit weniger guten Embryonen im Kryobestand verbunden, doch sobald eine gesund aussehende, chromosomal normale Blastozyste vorhanden war, schien ihre Chance, zu einem Kind zu führen, nicht stark davon beeinflusst zu sein, wie fragmentiert die Spermien-DNA des Vaters in der Ausgangsprobe gewesen war. Die Autorinnen und Autoren warnen jedoch, dass ihre Studie retrospektiv war, eine hochselektierte Gruppe überwiegend älterer Frauen einschloss und relativ wenige Männer mit sehr hohem DFI vertreten waren, sodass subtile Effekte übersehen worden sein könnten.
Was das für Patienten und Kliniken bedeutet
Für Paare lässt sich die Quintessenz in zweierlei Hinsicht zusammenfassen. Erstens kann ein hohes Maß an Spermien-DNA-Schäden es erschweren, die Phase zu erreichen, in der mehrere gute Embryonen zur Auswahl stehen, und es kann den Erfolg bei Befruchtung und früher Entwicklung moderat verringern. Zweitens: Liefert die IVF chromosomal normale Embryonen, können diese dennoch in vergleichbarem Maße einnisten und Babys hervorbringen wie Embryonen von Männern mit geringerem DFI — möglicherweise weil die Eizelle und der frühe Embryo einige väterliche DNA-Schäden reparieren können. Die Autorinnen und Autoren schlagen vor, den Test auf Spermien-DNA-Fragmentierung als zusätzliches Instrument zu nutzen, nicht um eine Behandlung auszuschließen, sondern um männliche Faktoren zu identifizieren, die Spermienauswahl zu steuern und IVF-Strategien zu verfeinern, die darauf abzielen, die Anzahl und Qualität der für den Transfer verfügbaren Embryonen zu verbessern.
Zitation: Okubo, T., Kobayashi, T., Hayashi, T. et al. The role of sperm DNA fragmentation testing in predicting IVF and PGT-A outcomes. Sci Rep 16, 14607 (2026). https://doi.org/10.1038/s41598-026-38974-x
Schlüsselwörter: männliche Unfruchtbarkeit, Spermien-DNA-Fragmentierung, IVF-Ergebnisse, genetische Embryotests, Blastozystenentwicklung