Clear Sky Science · fr
Le rôle du test de fragmentation de l’ADN spermatozoïdal pour prédire les résultats de FIV et de PGT-A
Pourquoi cela compte pour les couples qui essaient de concevoir
Quand la fécondation in vitro (FIV) échoue, l’attention se porte souvent sur l’âge de la femme, ses hormones ou son utérus. Mais cette étude examine de près l’autre moitié de l’équation, souvent négligée : le sperme de l’homme. Plus précisément, elle interroge si de petites cassures dans l’ADN des spermatozoïdes — trop petites pour être vues au microscope standard — peuvent prédire quels embryons seront sains et quelles tentatives de FIV aboutiront à un bébé, même lorsque les embryons sont soigneusement dépistés par des tests génétiques avancés.
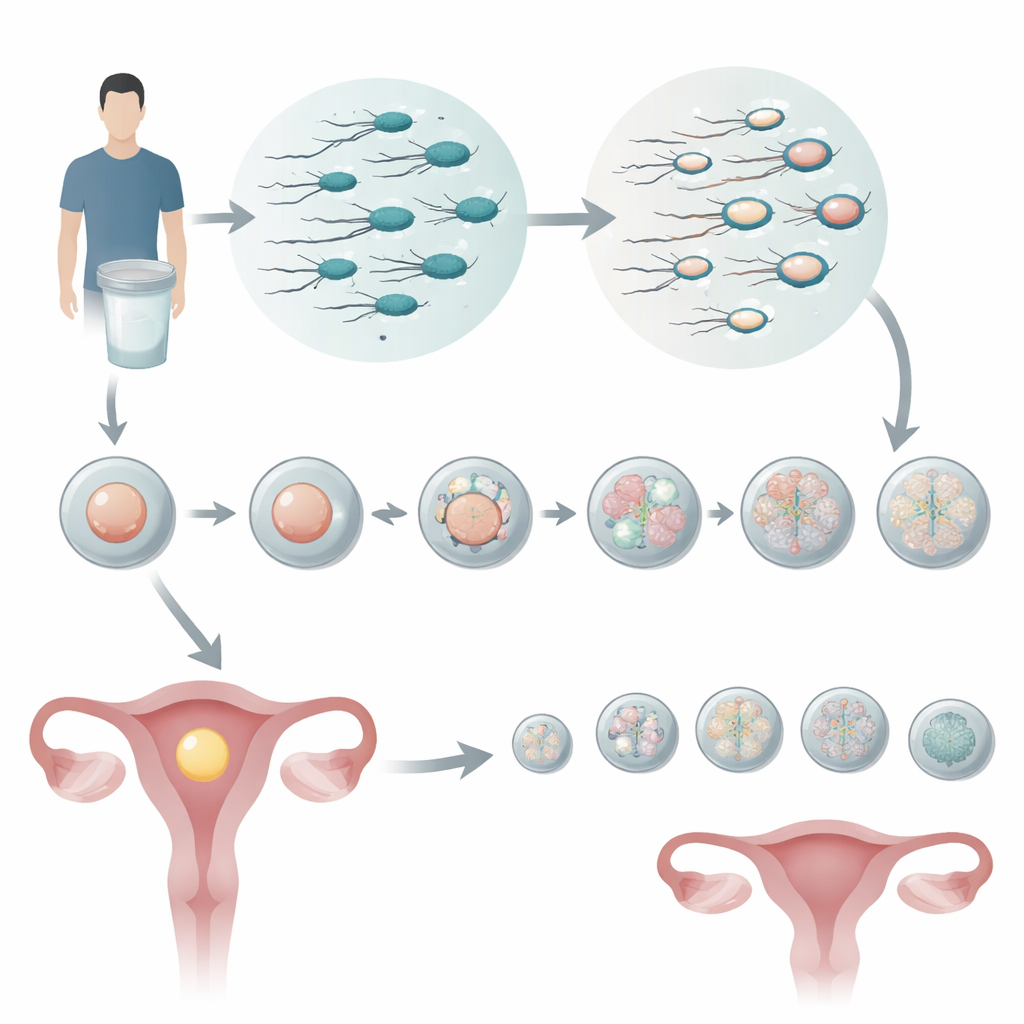
Aller au-delà d’un simple dénombrement des spermatozoïdes
La plupart des cliniques de fertilité évaluent le sperme principalement par le nombre, la mobilité et l’aspect morphologique. Ces mesures sont utiles mais rudimentaires, et deux prélèvements semblant similaires sur le papier peuvent se comporter très différemment en laboratoire. Les chercheurs se sont concentrés sur une caractéristique plus subtile : l’intégrité de l’ADN spermatozoïdal. Ils ont utilisé un test mesurant l’indice de fragmentation de l’ADN (DFI) — essentiellement le pourcentage de spermatozoïdes dont le matériel génétique est fragmenté. Les hommes ont été classés en groupes à DFI faible, moyen et élevé, et leurs partenaires ont tous subi une FIV avec un test génétique préimplantatoire pour l’aneuploïdie (PGT-A), une technique qui vérifie si les embryons ont un nombre anormal de chromosomes avant le transfert.
Comment l’étude a été menée
L’équipe a suivi 124 couples traités dans un centre de fertilité unique. Tous les hommes ont passé un test DFI, et tous les couples ont réalisé des cycles de FIV au cours desquels les embryons ont été cultivés jusqu’au stade de blastocyste, biopsiés et analysés par séquençage nouvelle génération. Cela a permis aux scientifiques de relier le niveau de DFI de chaque homme à plusieurs étapes clés : la fécondation des ovocytes (par FIV conventionnelle ou par injection intra-cytoplasmique de spermatozoïde), le nombre et la qualité des blastocystes formés, le taux d’anomalies chromosomiques détectées par PGT-A, et des résultats concrets tels que l’implantation, la grossesse clinique et la naissance vivante après transfert d’embryons chromosomiquement normaux.
Ce que les dommages de l’ADN spermatozoïdal ont affecté — et ce qu’ils n’ont pas affecté
Les hommes présentant un DFI élevé étaient en général plus âgés et avaient une motilité spermatozoïdale plus faible. Dans ces cas à DFI élevé, les taux de fécondation étaient plus bas lorsque le spermatozoïde était injecté directement dans l’ovocyte (ICSI), et moins d’embryons ont évolué en blastocystes de bonne qualité susceptibles d’être congelés. Cela suggère que des traits visibles du sperme, comme le mouvement et la morphologie, ne révèlent pas entièrement des problèmes d’ADN plus profonds. Pourtant, en regardant les résultats du PGT-A, une surprise est apparue : la proportion d’embryons avec un nombre de chromosomes normal, mosaïque ou anormal était similaire entre les groupes à DFI faible, moyen et élevé. Autrement dit, parmi les embryons arrivés au stade de biopsie, le fait d’être parti de spermatozoïdes plus endommagés ne s’est pas clairement traduit par davantage d’erreurs chromosomiques.
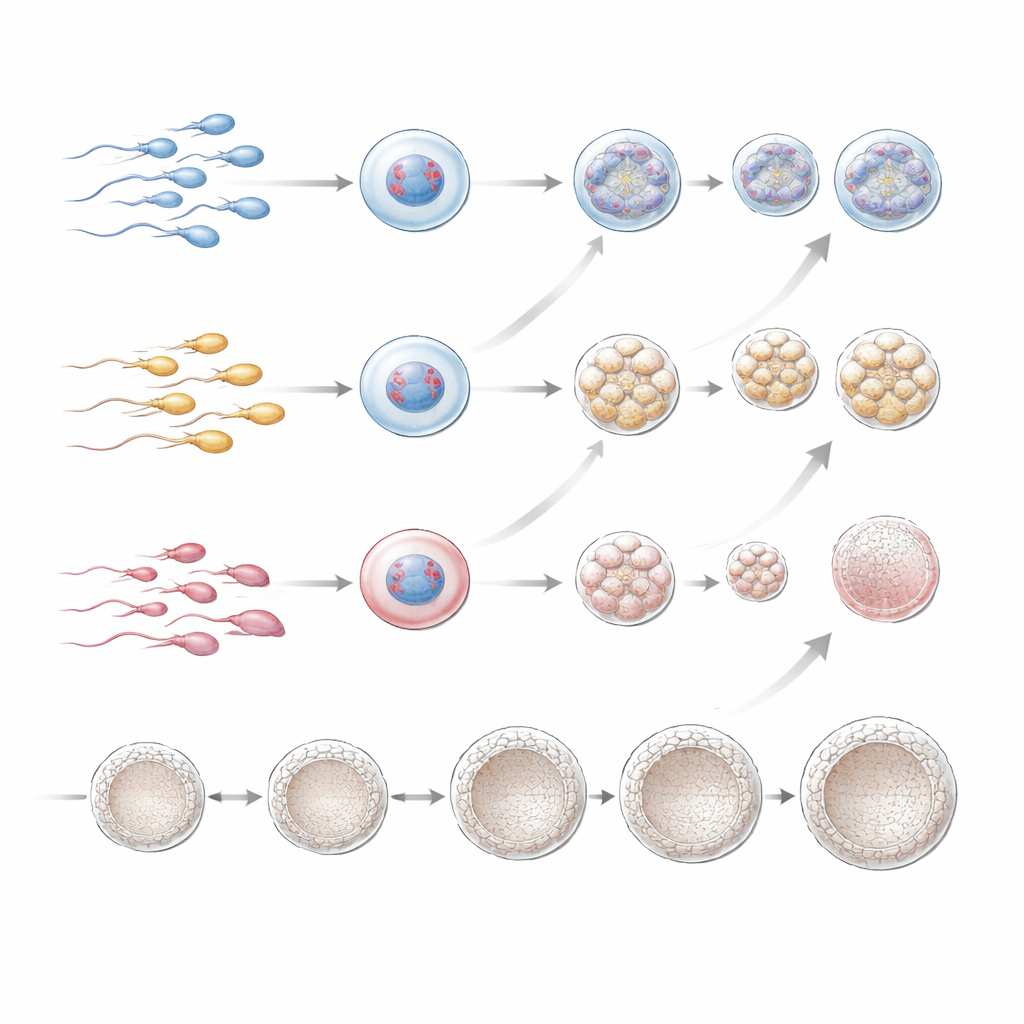
Les spermatozoïdes endommagés condamnent-ils les tentatives de FIV ?
Pour répondre à la question qui importe le plus aux couples, l’équipe a suivi ce qui s’est passé après le transfert d’embryons que le PGT-A avait classés comme chromosomiquement normaux (ou mosaïques de bas niveau). Les taux d’implantation, de grossesse et de naissance vivante par transfert d’embryon étaient globalement comparables entre les trois groupes de DFI, y compris dans le petit sous-groupe à DFI élevé. Bien qu’un DFI élevé soit associé à un nombre réduit d’embryons de qualité en congélation, une fois qu’un blastocyste d’apparence saine et chromosomiquement normal existe, sa probabilité de donner naissance à un bébé ne semblait pas fortement liée au degré de fragmentation de l’ADN paternel dans l’échantillon initial. Les auteurs soulignent toutefois que leur étude était rétrospective, portait sur un groupe fortement sélectionné composé majoritairement de femmes plus âgées, et incluait relativement peu d’hommes avec un DFI très élevé, de sorte que des effets subtils ont pu échapper à leur détection.
Ce que cela signifie pour les patients et les cliniques
Pour les couples, le message est double. D’une part, un taux élevé de dommages de l’ADN spermatozoïdal peut rendre plus difficile l’obtention d’un grand nombre d’embryons de qualité, et il peut réduire modestement le succès de la fécondation et du développement précoce. D’autre part, si la FIV produit des embryons chromosomiquement normaux, ces embryons peuvent encore s’implanter et donner naissance à des bébés à des taux similaires à ceux observés pour des hommes ayant un DFI plus faible, probablement parce que l’ovocyte et l’embryon précoce peuvent réparer une partie des dommages paternels à l’ADN. Les auteurs proposent d’utiliser le test de fragmentation de l’ADN spermatozoïdal comme un outil supplémentaire : non pas pour exclure un traitement, mais pour identifier des problèmes d’origine masculine, guider les méthodes de sélection des spermatozoïdes et affiner les stratégies de FIV visant à améliorer le nombre et la qualité des embryons disponibles pour transfert.
Citation: Okubo, T., Kobayashi, T., Hayashi, T. et al. The role of sperm DNA fragmentation testing in predicting IVF and PGT-A outcomes. Sci Rep 16, 14607 (2026). https://doi.org/10.1038/s41598-026-38974-x
Mots-clés: infertilité masculine, fragmentation de l’ADN spermatozoïdal, résultats de la FIV, test génétique des embryons, développement du blastocyste