Clear Sky Science · sv
Destillera populationsspecifik expertis till en enhetlig modell för generaliserbar hjärntumörsegmentering
Varför en modell för alla är viktig
Hjärntumörer ser inte likadana ut från en person till en annan. Barn, vuxna, patienter i olika länder och personer med olika tumörtyper kan alla uppvisa mycket olika mönster i MRT-bilder. Ändå föredrar läkare och sjukhus ett enda tillförlitligt datorverktyg som automatiskt kan avgränsa tumörer för varje patient, istället för att hantera många separata modeller. Denna studie introducerar ett nytt sätt att träna ett sådant enhetligt system så att det fungerar väl över fem mycket olika typer av hjärntumörer, vilket potentiellt kan ge mer konsekvent vård för patienter världen över.
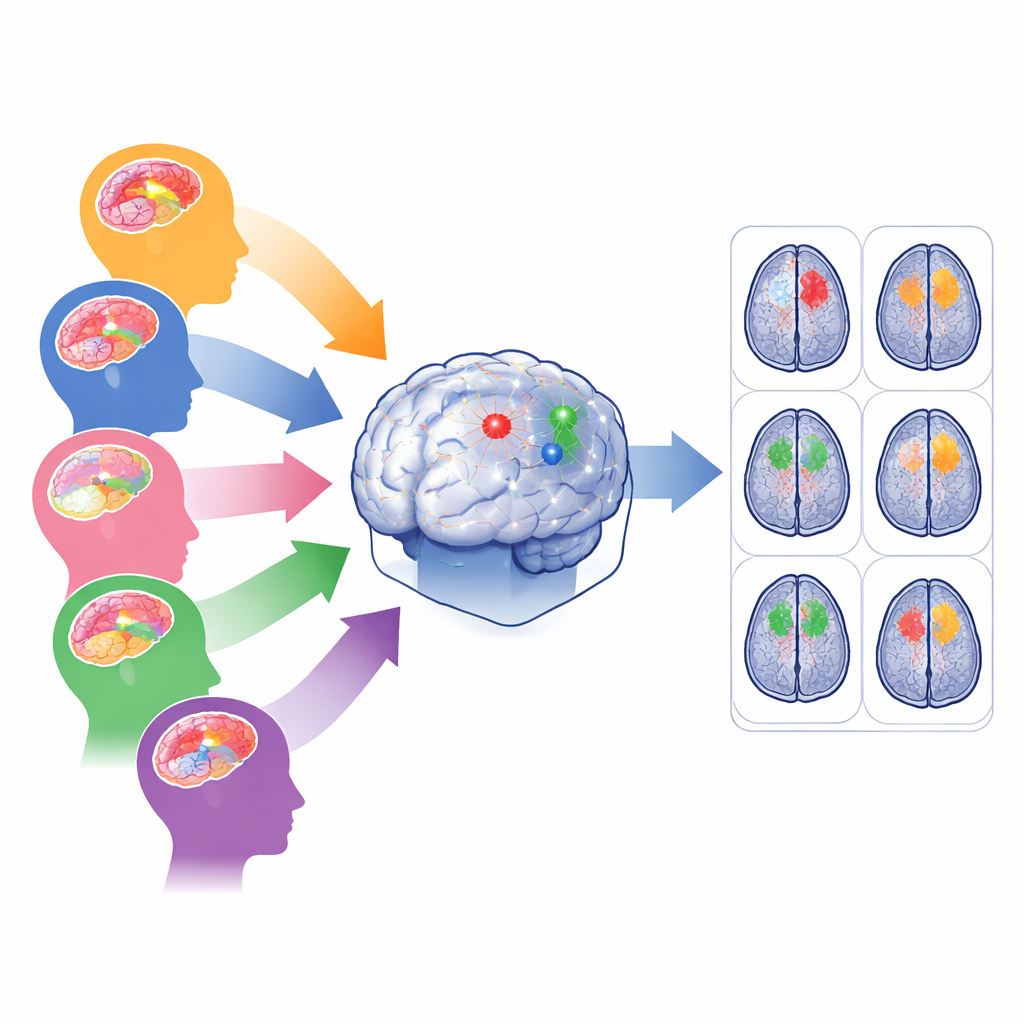
Utmaningen med många slags hjärntumörer
Moderna artificiella intelligensverktyg kan spåra hjärntumörer i MRT-bilder med imponerande noggrannhet—men vanligtvis bara när datan liknar den de tränats på. I verkliga sjukhus kommer bilder från olika maskiner och protokoll, och tumörer varierar i storlek, form och läge. Vuxna gliom ligger ofta djupt inne i hjärnan, gliom i Subsahariska Afrika fångas med lägre kvalitets-skannrar, pediatriska gliom omorganiserar interna tumörområden, meningiom sitter på hjärnans yta och metastaser kan framträda som många utspridda fläckar. Att träna en modell på alla dessa fall samtidigt tenderar att favorisera den vanligaste gruppen och försummelse sällsynta eller brusiga populationer, vilket riskerar dålig prestanda precis där hjälpen behövs mest.
Varför tidigare lösningar inte räckte
Forskare har prövat flera kringgående strategier. Ett alternativ är att finjustera en modell för varje nytt dataset eller sjukhus, men det kräver att man underhåller många versioner och kan få systemet att "glömma" tidigare kunskap. En annan strategi är att använda ensemblemetoder, där flera specialiserade modeller röstar om slutresultatet; även om detta ofta är exakt är det långsamt och beräkningskrävande. Curriculum learning, som matar data i en noggrant vald ordning från enklare till svårare fall, kan hjälpa men är knepigt att utforma och fångar fortfarande kanske inte alla tumörvarianter. Foundationsmodeller som "segment anything" lovar allmän segmentering, men de kräver ofta mänskliga prompts och är inte fullt automatiska—vilket begränsar deras användbarhet i rutinmässiga kliniska arbetsflöden.
Att blanda många experter till en student
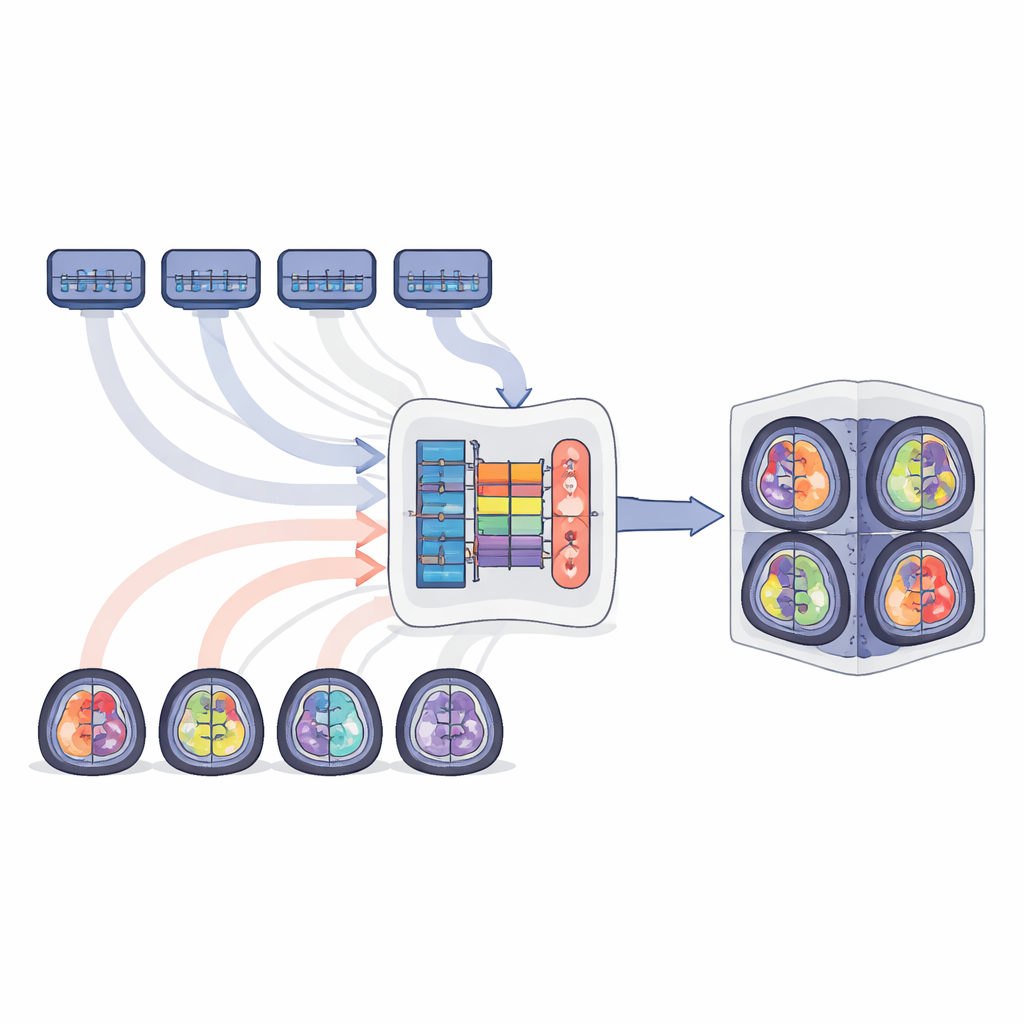
Författarna föreslår MTSS-KDNet, ett "multi-teacher, single-student"-angreppssätt inspirerat av hur en läkarkandidat kan lära sig från flera specialister. Först tränas fem expertmodeller separat, var och en inriktad på en tumörpopulation: vuxna gliom, gliom i Subsahariska Afrika, pediatriska gliom, meningiom och metastaser. Dessa lärarnätverk blir starkt anpassade till särdragen i sin egen grupp. Därefter tränas en enda studentmodell att imitera dem—men på ett smart, populationsmedvetet sätt. För varje träningsskanning bearbetar den matchande läraren och studenten bilden parallellt. Studenten uppmuntras att matcha lärarens interna mönster och slutliga prediktioner samtidigt som den korrigeras med hjälp av de verkliga tumörkonturerna. En rättviseinriktad provtagningsschema säkerställer att varje träningsbatch alltid inkluderar ett fall från varje population, så att sällsynta grupper syns lika ofta som vanliga.
Hur den enhetliga modellen presterar i praktiken
Efter träning används endast studentmodellen för nya patienter, vilket håller distributionen enkel och snabb. Forskarna utvärderade den på alla fem tumörpopulationer med standardmått för hur väl de förutsagda tumörvolymerna och gränserna överensstämmer med experternas etiketter. För hela tumören, tumörkärnan och aktivt växande regioner uppnådde den enhetliga modellen starka resultat som matchade eller överträffade inte bara sina individuella lärare utan också kraftfulla jämförelser som finjusterade modeller, curriculum learning och multimodells-ensembler. Vinsterna var särskilt markanta i svåra inställningar som pediatriska tumörer, lågkvalitativa skanningar från Subsahariska Afrika och spridda hjärnmetastaser, där studenten tydligt presterade bättre än populationsspecifika experter. Visuell granskning visade renare, mer kompletta konturer, och interna feature-kartor avslöjade att modellen lärde sig att separera populationer i sin interna representation utan att behöva etiketter vid testtid.
Vad detta innebär för framtida patientvård
För en icke-specialist är huvudidén att författarna har funnit ett sätt att hälla kunnandet från många smala, expertsystem in i en general modell, utan att förlora det som gör varje expert bra på sitt område. Deras MTSS-KDNet-ramverk behåller de praktiska fördelarna med ett enda, automatiskt verktyg samtidigt som det bevarar prestanda över olika patienter, skannrar och tumörtyper. Även om det fortfarande kräver betydande träningsresurser och är beroende av bra initiala lärarmodeller, pekar detta tillvägagångssätt mot "foundations"-segmenteringssystem som kan tjäna globala populationer mer rättvist. På längre sikt skulle sådana enhetliga modeller kunna bidra till att patienter med sällsynta tumörer, barn eller de i underresurserade regioner får samma nivå av bildprecision som de som vårdas vid större medicinska centra.
Citering: Elzayat, A., Hanafy, N., Magdy, M. et al. Distilling population specific expertise into a unified model for generalizable brain tumor segmentation. Sci Rep 16, 12969 (2026). https://doi.org/10.1038/s41598-026-35627-x
Nyckelord: hjärntumörsegmentering, medicinsk bildbehandling AI, kunskapsdestillering, modellgeneralisation, MRI