Clear Sky Science · de
Wissen aus populationsspezifischen Expertensystemen in ein einheitliches Modell für generalisierbare Hirntumorsegmentierung überführen
Warum ein Modell für alle wichtig ist
Hirntumoren sehen von Person zu Person unterschiedlich aus. Kinder, Erwachsene, Patienten in verschiedenen Ländern und Menschen mit unterschiedlichen Tumorarten zeigen auf MRT-Aufnahmen sehr unterschiedliche Muster. Ärzte und Krankenhäuser würden jedoch lieber ein einziges, verlässliches Computerwerkzeug haben, das Tumoren bei jedem Patienten automatisch abgrenzt, anstatt viele separate Modelle zu verwalten. Diese Studie stellt eine neue Methode vor, ein solches einheitliches System zu trainieren, damit es über fünf sehr verschiedene Arten von Hirntumoren hinweg gut funktioniert und so potenziell zu einer konsistenteren Versorgung von Patient:innen weltweit beitragen kann.
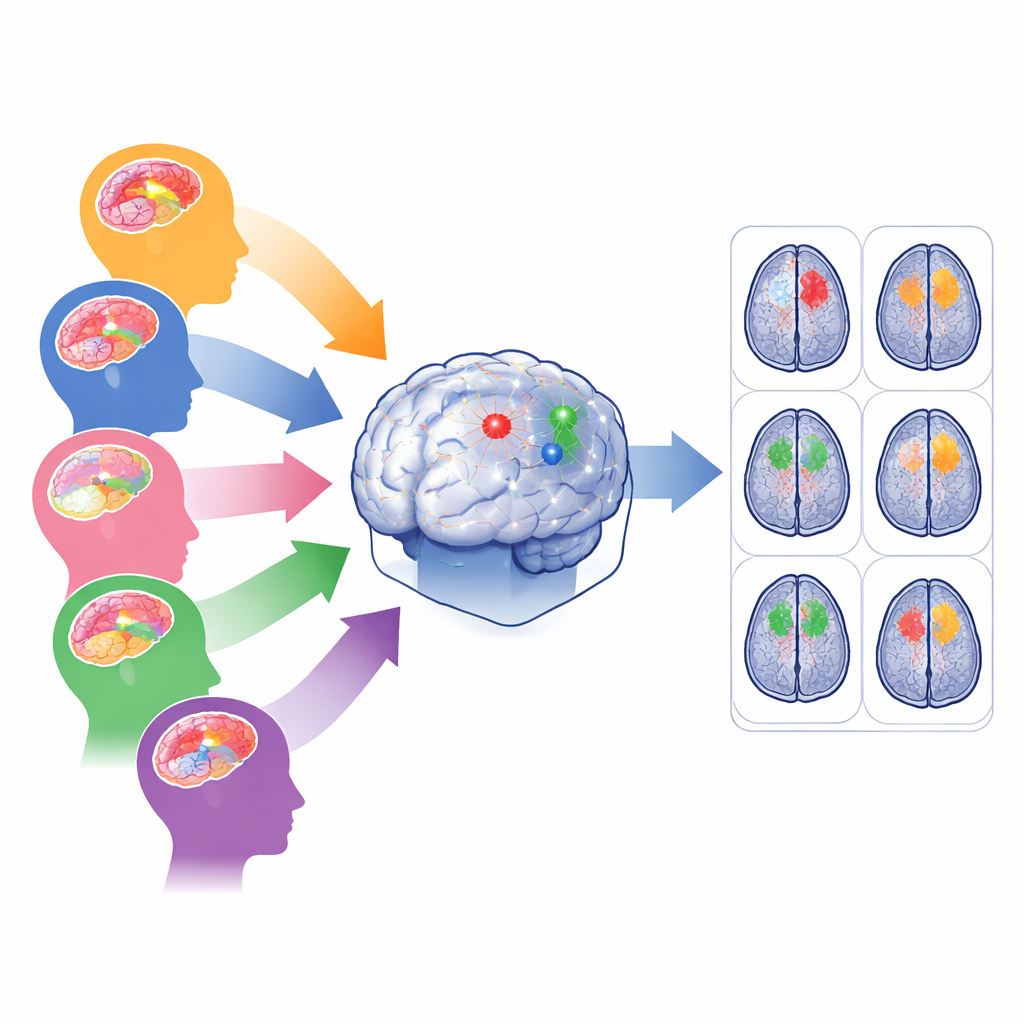
Die Herausforderung vieler Tumorarten
Moderne KI-Werkzeuge können Hirntumoren in MRT-Aufnahmen mit beeindruckender Genauigkeit nachzeichnen – doch meist nur, wenn die Daten denen ähneln, auf denen sie trainiert wurden. In realen Krankenhäusern stammen Aufnahmen von verschiedenen Geräten und Protokollen, und Tumoren variieren in Größe, Form und Lage. Erwachsenengliome liegen oft tief im Gehirn, Gliome in Subsahara-Afrika werden mit Geräten geringerer Bildqualität erfasst, pädiatrische Gliome verändern interne Tumorregionen, Meningeome sitzen auf der Gehirnoberfläche und Metastasen können als viele verstreute Herde auftreten. Ein Modell gleichzeitig auf all diese Fälle zu trainieren, neigt dazu, die häufigste Gruppe zu bevorzugen und seltene oder verrauschte Populationen zu vernachlässigen, was gerade dort zu schlechter Leistung führen kann, wo Hilfe am dringendsten benötigt wird.
Warum frühere Lösungen nicht ausreichten
Forscher:innen haben mehrere Umgehungsstrategien ausprobiert. Eine Möglichkeit ist, ein Modell für jedes neue Datenset oder Krankenhaus feinzujustieren, doch das erfordert die Pflege vieler Versionen und kann dazu führen, dass das System früheres Wissen „vergisst“. Eine andere Strategie sind Ensembles, bei denen mehrere spezialisierte Modelle über das Endergebnis abstimmen; zwar oft genau, aber langsam und rechenintensiv. Curriculum Learning, das Daten in einer sorgfältig gewählten Reihenfolge von einfachen zu schwierigen Fällen zuführt, kann helfen, ist aber schwer zu gestalten und erfasst möglicherweise nicht alle Tumorvarianten. Foundation-Modelle wie „segment anything“ versprechen universelle Segmentierung, benötigen jedoch meist menschliche Eingaben und sind nicht vollständig automatisch – was ihren Nutzen in routinemäßigen klinischen Abläufen einschränkt.
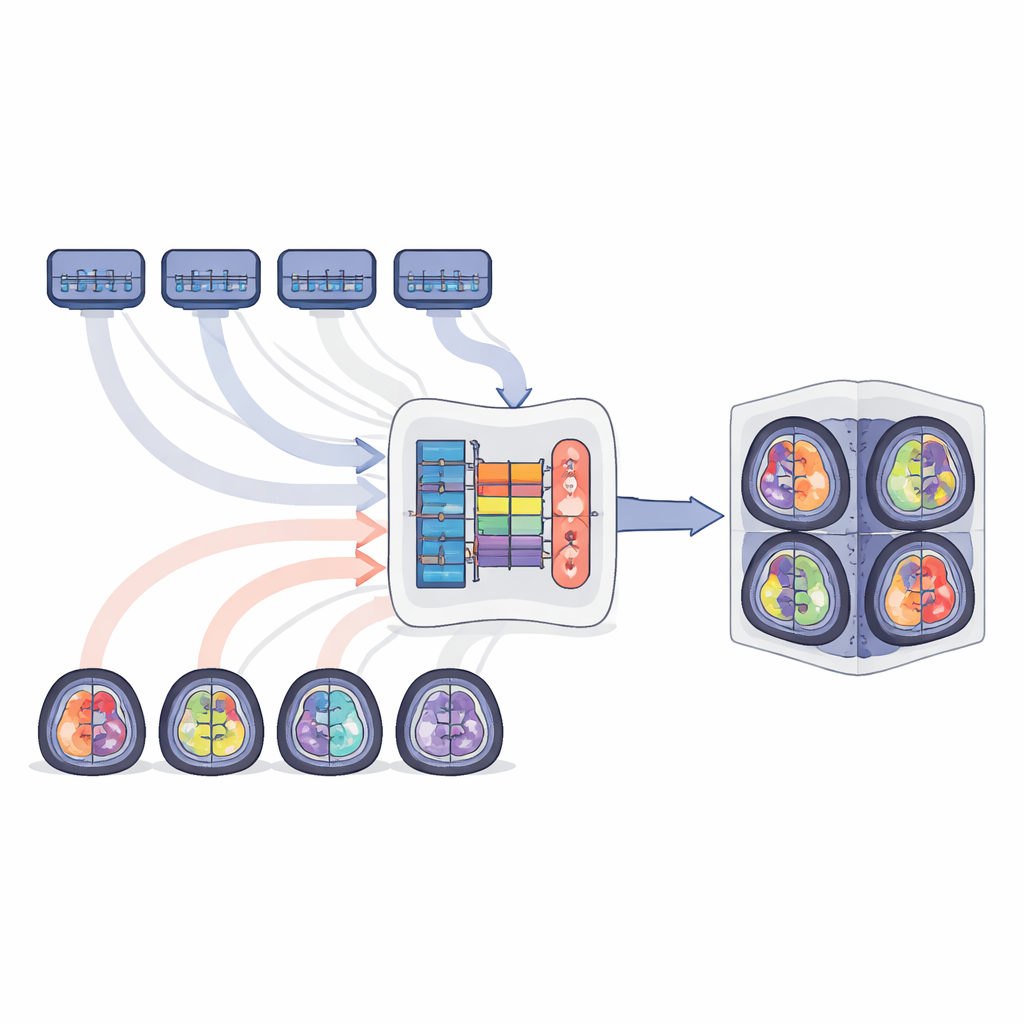
Mehrere Experten in einen Studenten vereinen
Die Autor:innen schlagen MTSS-KDNet vor, einen „Multi-Teacher, Single-Student“-Ansatz, inspiriert davon, wie ein Assistenzarzt von mehreren Spezialist:innen lernen könnte. Zuerst werden fünf Expertenmodelle separat trainiert, von denen sich jedes auf eine Tumorpopulation konzentriert: Erwachsenengliome, Gliome aus Subsahara-Afrika, pädiatrische Gliome, Meningeome und Metastasen. Diese Lehrernetzwerke werden sehr auf die Merkmale ihrer jeweiligen Gruppe abgestimmt. Anschließend wird ein einzelnes Studentenmodell trainiert, um sie nachzuahmen – jedoch auf eine intelligente, populationsbewusste Weise. Für jede Trainingsaufnahme verarbeiten der passende Lehrer und der Student das Bild parallel. Der Student wird dazu angeleitet, die internen Muster und die finalen Vorhersagen des Lehrers zu imitieren und gleichzeitig mithilfe der wahren Tumorsegmentierungen korrigiert. Ein auf Fairness ausgelegtes Sampling-Schema stellt sicher, dass jede Trainingscharge immer einen Fall aus jeder Population enthält, sodass seltene Gruppen genauso oft gesehen werden wie häufige.
Wie das einheitliche Modell in der Praxis abschneidet
Nach dem Training wird für neue Patient:innen nur noch das Studentenmodell eingesetzt, wodurch die Bereitstellung einfach und schnell bleibt. Die Forschenden evaluierten es an allen fünf Tumorpopulationen mit standardisierten Metriken, die messen, wie genau die vorhergesagten Tumorvolumina und -grenzen den Expertenannotationen entsprechen. Über Ganztumor, Tumorkern und aktiv wachsende Bereiche erzielte das einheitliche Modell starke Werte, die nicht nur mit seinen einzelnen Lehrern mithielten, sondern auch leistungsfähige Baselines wie feinjustierte Modelle, Curriculum Learning und Multi-Model-Ensembles übertrafen. Verbesserungen waren besonders auffällig in schwierigen Szenarien wie pädiatrischen Tumoren, niedrigqualitativen Subsahara-Aufnahmen und verstreuten Hirnmetastasen, wo der Student die populationsspezifischen Experten deutlich übertraf. Visuelle Inspektionen zeigten sauberere, vollständigere Umrisse, und interne Feature-Maps offenbarten, dass das Modell gelernt hatte, Populationen in seiner internen Repräsentation zu trennen, ohne dafür Labels zur Testzeit zu benötigen.
Was das für die zukünftige Patientenversorgung bedeutet
Für Nicht-Spezialist:innen besteht die Kernaussage darin, dass die Autor:innen einen Weg gefunden haben, das Know-how vieler enger Expertenmodelle in ein allgemeines Modell zu überführen, ohne die Stärken der einzelnen Experten zu verlieren. Ihr MTSS-KDNet-Framework verbindet die praktischen Vorteile eines einzigen, automatischen Werkzeugs mit der Bewahrung guter Leistung über unterschiedliche Patientengruppen, Scanner und Tumortypen hinweg. Zwar erfordert der Ansatz weiterhin erhebliche Trainingsressourcen und hängt von guten initialen Lehrermodellen ab, doch weist er in Richtung „Foundation“-Segmentierungssysteme, die globale Populationen gerechter bedienen könnten. Langfristig könnten solche einheitlichen Modelle dazu beitragen, dass Patienten mit seltenen Tumoren, Kinder oder Menschen in unterversorgten Regionen die gleiche Bildgebungspräzision erfahren wie Patient:innen in großen medizinischen Zentren.
Zitation: Elzayat, A., Hanafy, N., Magdy, M. et al. Distilling population specific expertise into a unified model for generalizable brain tumor segmentation. Sci Rep 16, 12969 (2026). https://doi.org/10.1038/s41598-026-35627-x
Schlüsselwörter: Hirntumorsegmentierung, medizinische Bildgebung KI, Knowledge Distillation, Modellgeneralisation, MRT