Clear Sky Science · it
Distillare competenze specifiche per popolazione in un modello unificato per la segmentazione generalizzabile dei tumori cerebrali
Perché un unico modello per tutti conta
I tumori cerebrali non assomigliano gli uni agli altri da una persona all’altra. Bambini, adulti, pazienti in diversi paesi e persone con diversi tipi di tumore possono mostrare pattern molto differenti nelle scansioni MRI. Eppure medici e ospedali preferirebbero uno strumento informatico unico e affidabile che possa delineare automaticamente i tumori per ogni paziente, invece di gestire numerosi modelli separati. Questo studio presenta un nuovo modo di addestrare un sistema unificato in modo che funzioni bene su cinque tipi molto diversi di tumori cerebrali, potenzialmente offrendo cure più coerenti ai pazienti in tutto il mondo.
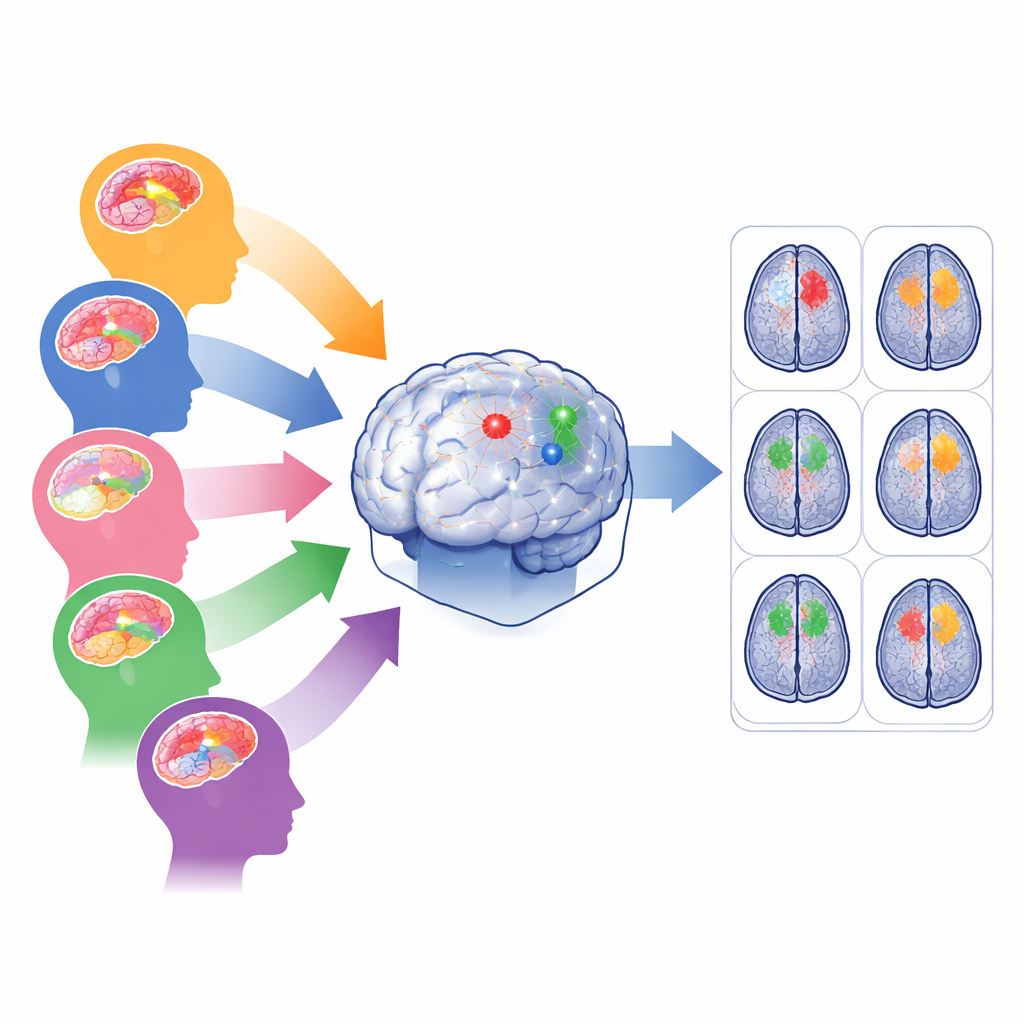
La sfida dei molti tipi di tumore cerebrale
Gli strumenti di intelligenza artificiale moderni possono tracciare i tumori cerebrali nelle scansioni MRI con accuratezza impressionante—ma di solito solo quando i dati somigliano a quelli su cui sono stati addestrati. Negli ospedali reali, le scansioni provengono da macchine e protocolli diversi, e i tumori variano per dimensione, forma e posizione. I gliomi negli adulti spesso si trovano in profondità nel cervello, i gliomi nell’Africa subsahariana sono acquisiti con scanner di qualità inferiore, i gliomi pediatrici riorganizzano le regioni interne del tumore, i meningiomi si trovano sulla superficie cerebrale e le metastasi possono apparire come molti punti sparsi. Addestrare un solo modello su tutti questi casi contemporaneamente tende a favorire il gruppo più comune e a trascurare popolazioni rare o rumorose, rischiando prestazioni scadenti proprio dove l’aiuto è più necessario.
Perché le soluzioni precedenti non sono state sufficienti
I ricercatori hanno provato diverse vie alternative. Un’opzione è adattare (fine-tune) un modello per ogni nuovo dataset o ospedale, ma ciò richiede di mantenere molte versioni e può portare il sistema a “dimenticare” conoscenze precedenti. Un’altra strategia è usare ensemble, dove diversi modelli specializzati votano sulla risposta finale; pur essendo spesso accurati, sono lenti e costosi dal punto di vista computazionale. Il curriculum learning, che fornisce i dati in un ordine calibrato dal più semplice al più difficile, può aiutare ma è complesso da progettare e può comunque non catturare tutte le varietà tumorali. I modelli di tipo foundation come “segment anything” promettono una segmentazione di uso generale, ma in genere richiedono prompt umani e non sono completamente automatici—limitando la loro utilità nei flussi di lavoro clinici di routine.
Combinare molti esperti in un unico studente
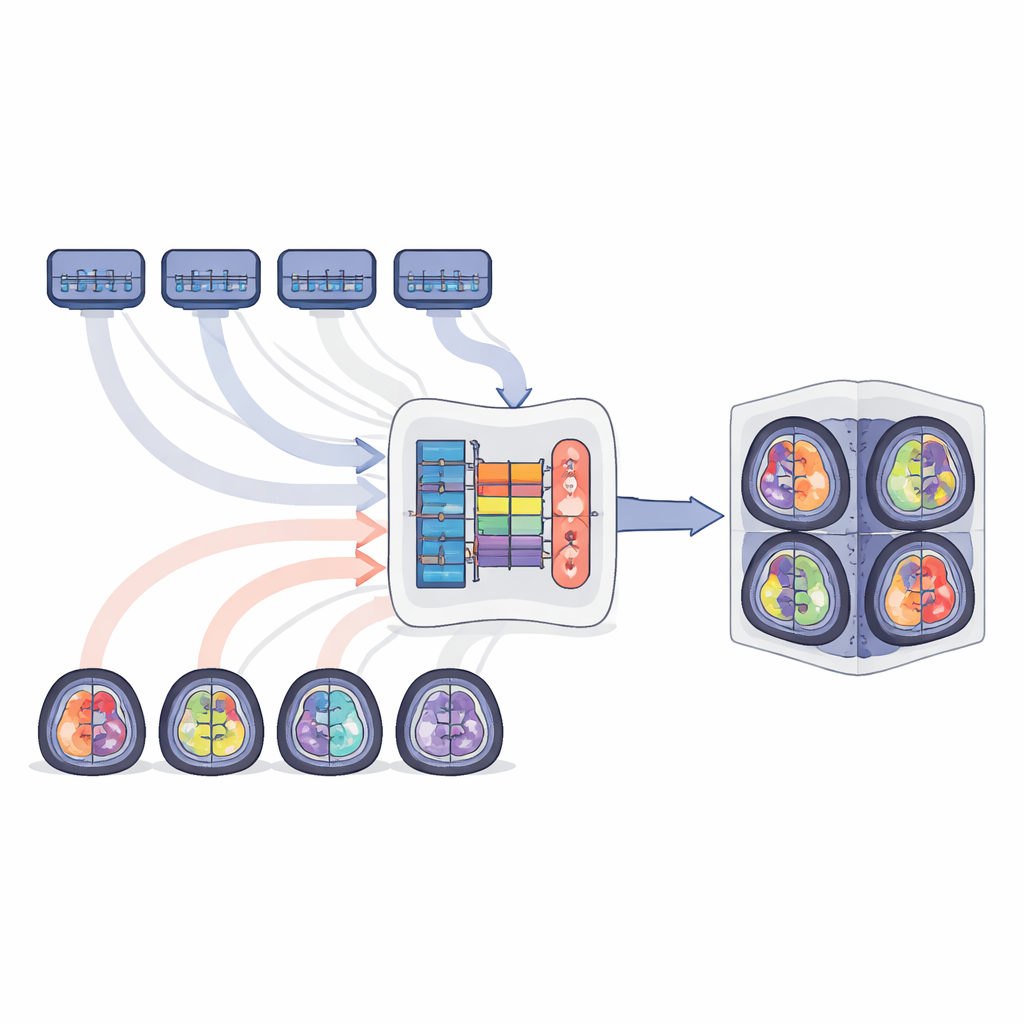
Gli autori propongono MTSS-KDNet, un approccio “multi-teacher, single-student” ispirato a come un medico in formazione potrebbe apprendere da diversi specialisti. Per prima cosa, vengono addestrati separatamente cinque modelli esperti, ciascuno focalizzato su una popolazione tumorale: gliomi adulti, gliomi dell’Africa subsahariana, gliomi pediatrici, meningiomi e metastasi. Queste reti “insegnanti” diventano altamente tarate sulle caratteristiche del loro gruppo. Poi un singolo modello studente viene addestrato a imitarle—ma in modo intelligente e consapevole della popolazione. Per ogni scansione di addestramento, l’insegnante corrispondente e lo studente elaborano l’immagine in parallelo. Lo studente viene spinto a corrispondere i pattern interni e le predizioni finali dell’insegnante, pur venendo corretto usando i contorni tumorali reali. Uno schema di campionamento focalizzato sulla equità assicura che ogni batch di addestramento includa sempre un caso per ciascuna popolazione, in modo che i gruppi rari vengano visti con la stessa frequenza di quelli comuni.
Come si comporta il modello unificato nella pratica
Dopo l’addestramento, per i nuovi pazienti viene utilizzato solo il modello studente, mantenendo il deployment semplice e veloce. I ricercatori lo hanno valutato su tutte e cinque le popolazioni tumorali usando misure standard di quanto i volumi tumorali e i confini predetti corrispondano alle etichette degli esperti. Su tumore completo, nucleo tumorale e regioni attivamente in crescita, il modello unificato ha ottenuto risultati solidi che hanno eguagliato o superato non solo i singoli insegnanti ma anche potenti baseline come modelli fine-tuned, curriculum learning e ensemble multi-modello. I miglioramenti sono stati particolarmente marcati in contesti difficili come i tumori pediatrici, le scansioni a bassa qualità dell’Africa subsahariana e le metastasi cerebrali sparse, dove lo studente ha chiaramente sovraperformato gli esperti specifici per popolazione. Ispezioni visive hanno mostrato contorni più puliti e completi, e le mappe delle caratteristiche interne hanno rivelato che il modello ha imparato a separare le popolazioni nella sua rappresentazione interna senza necessitare di etichette al momento del test.
Cosa significa questo per la cura futura dei pazienti
Per un non-specialista, l’idea chiave è che gli autori hanno trovato un modo per trasferire il know-how di molti sistemi esperti ristretti in un unico modello generale, senza perdere ciò che rende ciascun esperto bravo nel proprio compito. Il framework MTSS-KDNet conserva i vantaggi pratici di uno strumento singolo e automatico pur mantenendo le prestazioni su pazienti, scanner e tipi di tumore diversi. Sebbene richieda ancora risorse di addestramento significative e dipenda da buoni modelli insegnanti iniziali, questo approccio indica la strada verso sistemi di segmentazione “foundation” in grado di servire le popolazioni globali in modo più equo. A lungo termine, modelli unificati di questo tipo potrebbero contribuire a garantire che pazienti con tumori rari, bambini o persone in regioni con poche risorse ricevano lo stesso livello di precisione d’imaging di chi si trova in grandi centri medici.
Citazione: Elzayat, A., Hanafy, N., Magdy, M. et al. Distilling population specific expertise into a unified model for generalizable brain tumor segmentation. Sci Rep 16, 12969 (2026). https://doi.org/10.1038/s41598-026-35627-x
Parole chiave: segmentazione tumori cerebrali, IA per imaging medico, distillazione della conoscenza, generalizzazione del modello, risonanza magnetica