Clear Sky Science · nl
Het destilleren van populatiespecifieke expertise in een verenigd model voor generaliseerbare hersentumorsegmentatie
Waarom één model voor iedereen ertoe doet
Hersentumoren zien er niet bij iedereen hetzelfde uit. Kinderen, volwassenen, patiënten in verschillende landen en mensen met uiteenlopende tumortypen kunnen elk heel verschillende patronen op MRI-scans vertonen. Toch geven artsen en ziekenhuizen de voorkeur aan één betrouwbaar computerhulpmiddel dat automatisch tumoren voor elke patiënt kan omlijnen, in plaats van met veel afzonderlijke modellen te moeten werken. Deze studie introduceert een nieuwe manier om zo’n verenigd systeem te trainen zodat het goed presteert voor vijf zeer verschillende soorten hersentumoren, wat mogelijk kan leiden tot meer consistente zorg voor patiënten wereldwijd.
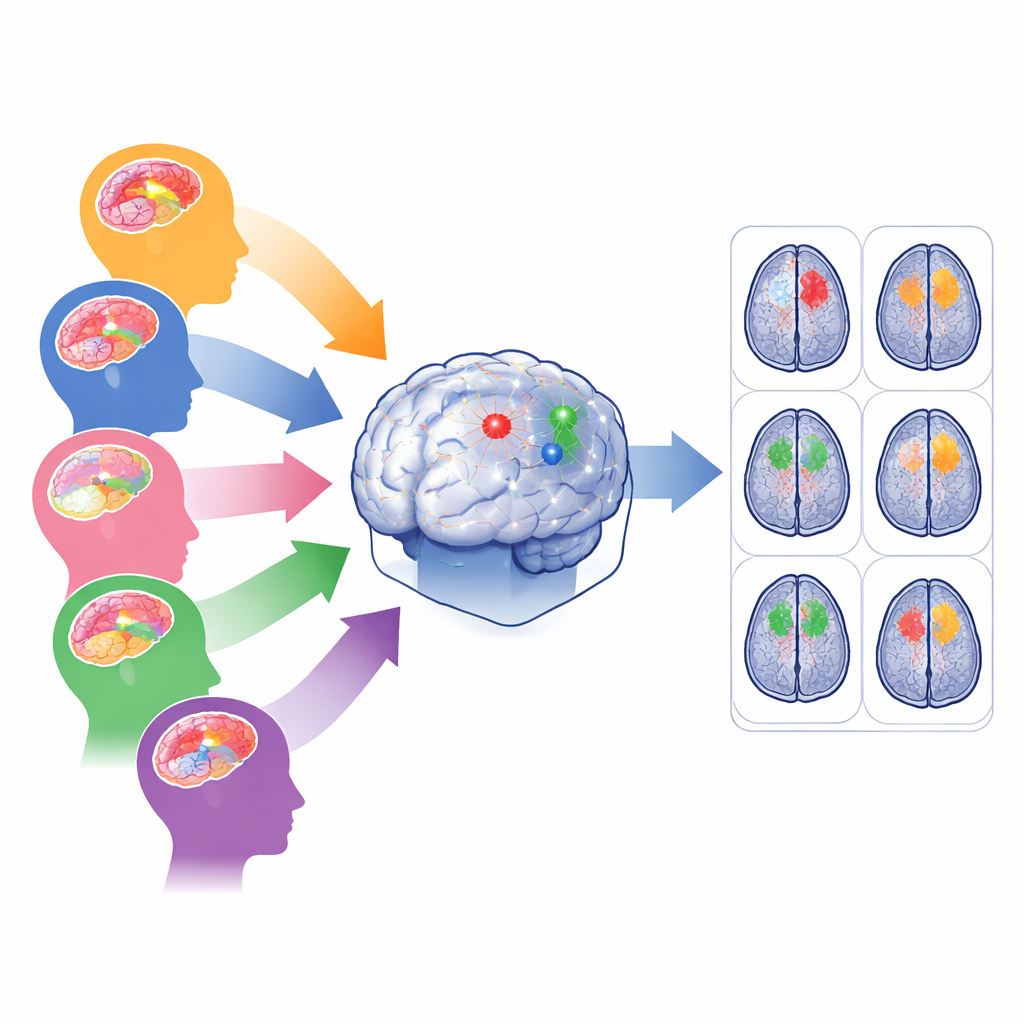
De uitdaging van veel verschillende soorten hersentumoren
Moderne kunstmatige-intelligentietools kunnen hersentumoren op MRI-scans met indrukwekkende nauwkeurigheid traceren—maar meestal alleen wanneer de gegevens lijken op wat ze tijdens training hebben gezien. In echte ziekenhuizen komen scans van verschillende apparaten en protocollen, en tumoren variëren in grootte, vorm en locatie. Volwassen gliomen liggen vaak diep in de hersenen, Sub-Sahara Afrikaanse gliomen worden met lagere kwaliteit scanners vastgelegd, pediatrische gliomen herschikken interne tumorgedeelten, meningeomen liggen aan het oppervlak van de hersenen en metastasen kunnen als vele verspreide plekjes verschijnen. Het trainen van één model op al deze gevallen tegelijk neigt ertoe de meest voorkomende groep te bevoordelen en zeldzame of lawaaierige populaties te verwaarlozen, waardoor de prestaties precies daar slecht kunnen zijn waar hulp het meest nodig is.
Waarom eerdere oplossingen tekortschoten
Onderzoekers hebben een aantal omwegen geprobeerd. Een optie is om een model voor elke nieuwe dataset of elk ziekenhuis fijn af te stemmen, maar dat vergt het bijhouden van veel versies en kan ertoe leiden dat het systeem eerder verworven kennis "vergeet". Een andere strategie is het gebruik van ensembles, waarbij meerdere gespecialiseerde modellen over het eindantwoord stemmen; hoewel vaak nauwkeurig, is dit traag en rekenkundig duur. Curriculum learning, waarbij data in een zorgvuldig gekozen volgorde van makkelijker naar moeilijker worden aangeboden, kan helpen maar is lastig te ontwerpen en vangt mogelijk nog steeds niet alle tumorvarianten. Foundation-modellen zoals "segment anything" beloven algemene segmentatie, maar hebben meestal menselijke prompts nodig en zijn niet volledig automatisch—waardoor hun bruikbaarheid in routinematige klinische workflows beperkt blijft.
Het samenvoegen van vele experts in één student
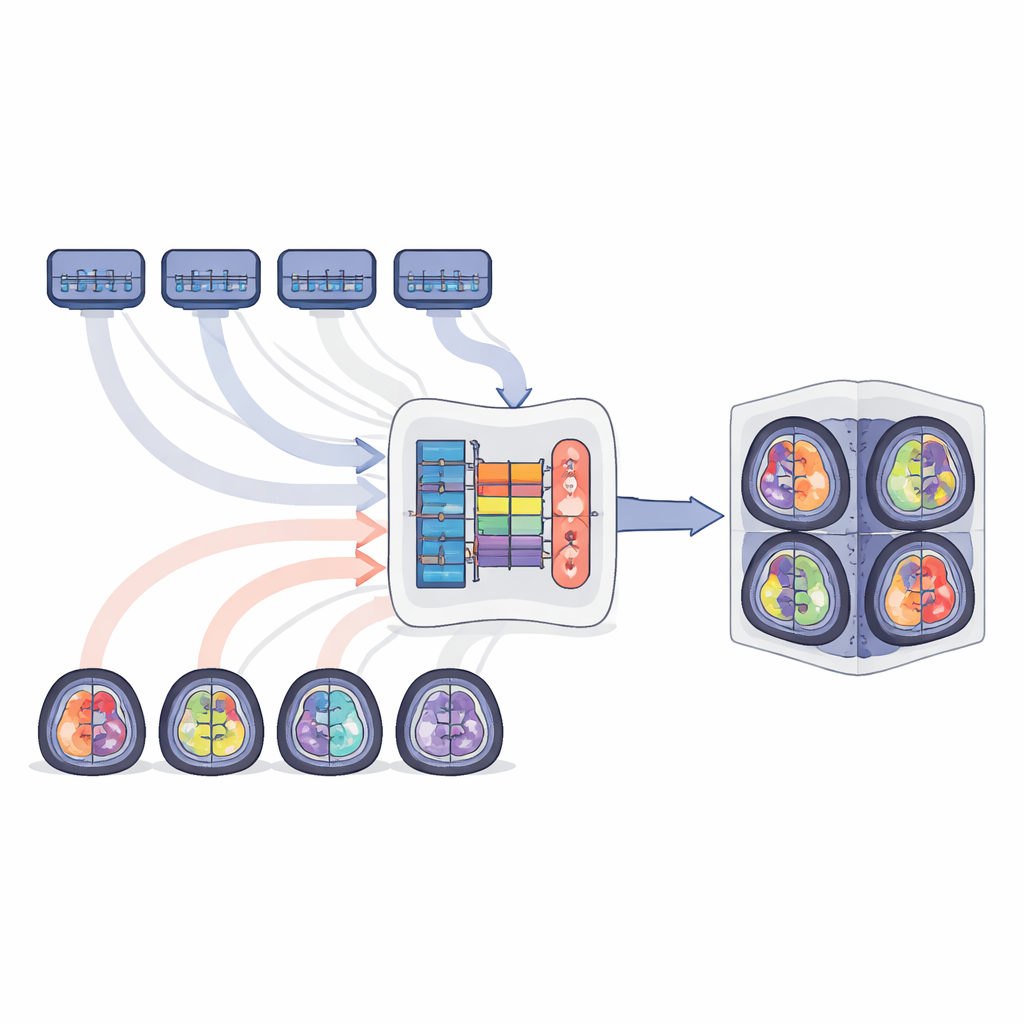
De auteurs stellen MTSS-KDNet voor, een "multi-teacher, single-student"-benadering geïnspireerd op hoe een arts in opleiding van meerdere specialisten kan leren. Eerst worden vijf expertmodellen afzonderlijk getraind, elk gericht op één tumorpopulatie: volwassen gliomen, Sub-Sahara Afrikaanse gliomen, pediatrische gliomen, meningeomen en metastasen. Deze teacher-netwerken worden sterk afgestemd op de kenmerken van hun eigen groep. Vervolgens wordt één studentmodel getraind om hen te imiteren—maar op een slimme, populatiebewuste manier. Voor elke trainingsscan verwerken de bijbehorende teacher en de student het beeld parallel. De student wordt aangestuurd om de interne patronen en eindvoorspellingen van de teacher te evenaren en wordt tegelijk gecorrigeerd met behulp van de werkelijke tumorcontouren. Een op eerlijkheid gericht steekproefsysteem zorgt ervoor dat elke trainingsbatch altijd één geval uit elke populatie bevat, zodat zeldzame groepen even vaak worden gezien als veelvoorkomende.
Hoe het verenigde model in de praktijk presteert
Na training wordt alleen het studentmodel gebruikt voor nieuwe patiënten, wat uitrol eenvoudig en snel houdt. De onderzoekers evalueerden het op alle vijf tumorpopulaties met standaardmaatregelen voor hoe nauwkeurig de voorspelde tumorvolumes en -grenzen overeenkomen met expertslabels. Over het gehele tumorvolume, tumorkern en actiever groeiende regio’s behaalde het verenigde model sterke scores die niet alleen overeenkwamen met maar ook de individuele teachers en krachtige baselines zoals fijn-afgestelde modellen, curriculum learning en multi-model ensembles overtroffen. Verbeteringen waren vooral opvallend in moeilijke situaties zoals pediatrische tumoren, laagwaardige Sub-Sahara Afrikaanse scans en verspreide hersenmetastasen, waar de student duidelijk beter presteerde dan populatiespecifieke experts. Visuele inspecties toonden schonere, meer volledige contouren en interne featuremaps lieten zien dat het model geleerd had populaties in zijn interne representatie te scheiden zonder labels nodig te hebben tijdens de testfase.
Wat dit betekent voor toekomstige patiëntenzorg
Voor niet-specialisten is het belangrijkste idee dat de auteurs een manier hebben gevonden om de kennis van vele smalle, gespecialiseerde systemen in één algemeen model te gieten, zonder te verliezen wat elk expertmodel goed maakt in zijn eigen taak. Hun MTSS-KDNet-kader behoudt de praktische voordelen van een enkel, automatisch hulpmiddel terwijl het de prestaties over diverse patiënten, scanners en tumortypen overeind houdt. Hoewel het nog steeds aanzienlijke trainingsmiddelen vereist en afhankelijk is van goede initiële teacher-modellen, wijst deze aanpak richting "foundation"-segmentatiesystemen die mondiale populaties eerlijker kunnen bedienen. Op de lange termijn zouden dergelijke verenigde modellen kunnen helpen waarborgen dat patiënten met zeldzame tumoren, kinderen of mensen in onderbemiddelde regio’s profiteren van hetzelfde niveau van beeldprecisie als die in grote medische centra.
Bronvermelding: Elzayat, A., Hanafy, N., Magdy, M. et al. Distilling population specific expertise into a unified model for generalizable brain tumor segmentation. Sci Rep 16, 12969 (2026). https://doi.org/10.1038/s41598-026-35627-x
Trefwoorden: segmentatie van hersentumoren, medische beeldvorming AI, kennisdistillatie, modelgeneralizatie, MRI