Clear Sky Science · fr
Distillation de l’expertise spécifique à chaque population dans un modèle unifié pour une segmentation généralisable des tumeurs cérébrales
Pourquoi un modèle unique pour tous est important
Les tumeurs cérébrales ne se présentent pas de la même façon d’un patient à l’autre. Les enfants, les adultes, les patients de différents pays et les personnes atteintes de types de tumeurs variés peuvent afficher des motifs très différents sur les images IRM. Pourtant, médecins et hôpitaux préfèreraient un outil informatique unique et fiable capable de délimiter automatiquement les tumeurs pour chaque patient, plutôt que de gérer de nombreux modèles distincts. Cette étude présente une nouvelle façon d’entraîner un tel système unifié afin qu’il fonctionne bien sur cinq types très différents de tumeurs cérébrales, apportant potentiellement une prise en charge plus homogène aux patients du monde entier.
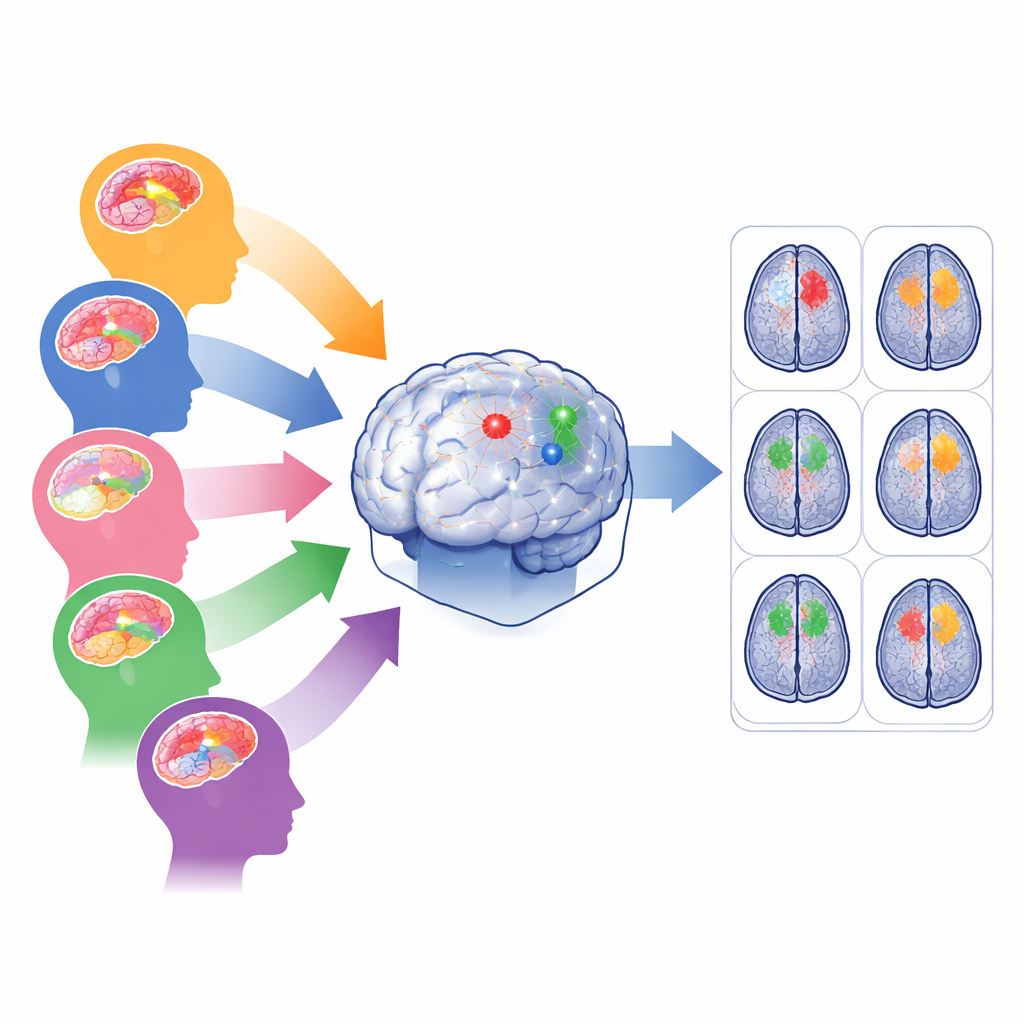
Le défi des multiples types de tumeurs cérébrales
Les outils d’intelligence artificielle modernes peuvent tracer les tumeurs cérébrales sur les IRM avec une précision impressionnante — mais généralement seulement lorsque les données ressemblent à celles utilisées pour l’entraînement. Dans les hôpitaux réels, les scans proviennent de machines et de protocoles différents, et les tumeurs varient en taille, forme et localisation. Les gliomes adultes se trouvent souvent profondément dans le cerveau, les gliomes d’Afrique subsaharienne sont acquis avec des scanners de moindre qualité, les gliomes pédiatriques réarrangent les régions internes de la tumeur, les méningiomes siègent à la surface cérébrale et les métastases peuvent apparaître sous forme de multiples foyers dispersés. Entraîner un seul modèle sur l’ensemble de ces cas tend à privilégier le groupe le plus fréquent et à négliger les populations rares ou bruyantes, au risque d’une performance médiocre précisément là où l’aide est la plus nécessaire.
Pourquoi les solutions précédentes ont montré leurs limites
Les chercheurs ont essayé plusieurs contournements. Une option consiste à affiner un modèle pour chaque nouveau jeu de données ou hôpital, mais cela implique de maintenir de nombreuses versions et peut conduire le système à «oublier» des connaissances antérieures. Une autre stratégie est d’utiliser des ensembles (ensembles de modèles), où plusieurs modèles spécialisés votent pour la réponse finale ; bien que souvent précis, cela reste lent et coûteux en calcul. L’apprentissage par curriculum, qui présente les données dans un ordre soigneusement choisi du plus simple au plus difficile, peut aider mais est délicat à concevoir et ne capture pas nécessairement toutes les variantes tumorales. Les modèles «fondation» comme «segment anything» promettent une segmentation polyvalente, mais nécessitent généralement des invites humaines et ne sont pas entièrement automatiques — limitant leur utilité dans les flux de travail cliniques de routine.
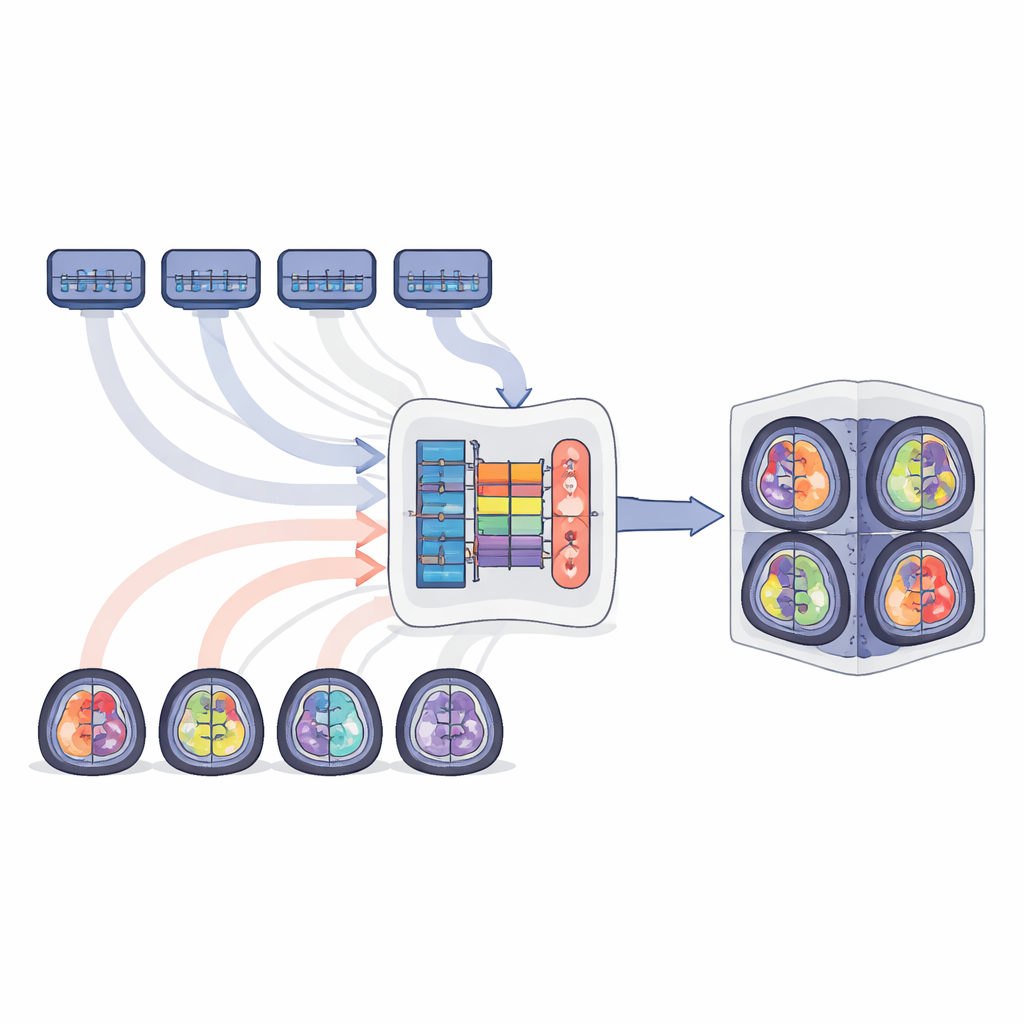
Mêler plusieurs experts en un seul étudiant
Les auteurs proposent MTSS-KDNet, une approche «multi-enseignants, étudiant unique» inspirée de la manière dont un médecin en formation pourrait apprendre auprès de plusieurs spécialistes. D’abord, cinq modèles experts sont entraînés séparément, chacun se concentrant sur une population tumorale : gliomes adultes, gliomes d’Afrique subsaharienne, gliomes pédiatriques, méningiomes et métastases. Ces réseaux enseignants deviennent très affinés sur les caractéristiques de leur propre groupe. Ensuite, un seul modèle étudiant est entraîné à les imiter — mais de façon intelligente et consciente des populations. Pour chaque scan d’entraînement, l’enseignant correspondant et l’étudiant traitent l’image en parallèle. L’étudiant est encouragé à reproduire les motifs internes et les prédictions finales de l’enseignant tout en étant corrigé à l’aide des contours tumoraux réels. Un schéma d’échantillonnage axé sur l’équité veille à ce que chaque lot d’entraînement inclue toujours un cas de chaque population, de sorte que les groupes rares soient vus aussi fréquemment que les groupes courants.
Comment le modèle unifié performe en pratique
Après l’entraînement, seul le modèle étudiant est utilisé pour les nouveaux patients, ce qui simplifie et accélère le déploiement. Les chercheurs l’ont évalué sur les cinq populations tumorales en utilisant des mesures standard de la concordance entre les volumes et les frontières tumorales prédites et les annotations d’experts. Sur la tumeur entière, le noyau tumoral et les régions actives, le modèle unifié a obtenu des scores solides qui égalent ou dépassent non seulement ses enseignants individuels mais aussi des références robustes comme les modèles affinés, l’apprentissage par curriculum et les ensembles de modèles. Les gains sont particulièrement marqués pour des contextes difficiles tels que les tumeurs pédiatriques, les scans de faible qualité d’Afrique subsaharienne et les métastases cérébrales diffuses, où l’étudiant a clairement surpassé les experts spécifiques à une population. Les inspections visuelles ont montré des contours plus propres et plus complets, et les cartes de caractéristiques internes ont révélé que le modèle avait appris à séparer les populations dans sa représentation interne sans nécessiter d’étiquettes au moment du test.
Ce que cela signifie pour les soins futurs aux patients
Pour un non-spécialiste, l’idée clé est que les auteurs ont trouvé un moyen de transvaser le savoir-faire de nombreux systèmes experts étroits dans un modèle général, sans perdre ce qui rend chaque expert performant dans son domaine. Leur cadre MTSS-KDNet conserve les avantages pratiques d’un outil unique et automatique tout en préservant la performance sur des patients, des scanners et des types de tumeurs divers. Bien que cette approche exige encore des ressources d’entraînement substantielles et dépende de bons modèles enseignants initiaux, elle ouvre la voie à des systèmes de segmentation «fondation» capables de servir les populations mondiales de manière plus équitable. À long terme, de tels modèles unifiés pourraient aider à garantir que les patients atteints de tumeurs rares, les enfants ou ceux des régions moins pourvues bénéficient du même niveau de précision d’imagerie que ceux des grands centres médicaux.
Citation: Elzayat, A., Hanafy, N., Magdy, M. et al. Distilling population specific expertise into a unified model for generalizable brain tumor segmentation. Sci Rep 16, 12969 (2026). https://doi.org/10.1038/s41598-026-35627-x
Mots-clés: segmentation des tumeurs cérébrales, IA en imagerie médicale, distillation des connaissances, généralisation des modèles, IRM