Clear Sky Science · sv
MechFind: ett datorramverk för de novo‑förutsägelse av enzymmekanismer
Varför förståelsen av enzymer är viktig
Varje levande cell drivs av små molekylära maskiner som kallas enzymer. Dessa proteiner påskyndar kemiska reaktioner som ger energi åt våra kroppar, får grödor att växa och möjliggör läkemedelstillverkning. Även om vi känner till den övergripande ”före och efter”‑kemin för tiotusentals enzymreaktioner, vet vi sällan de exakta steg‑för‑steg‑rörelser de använder för att gå från reaktanterna till produkterna. Denna artikel presenterar MechFind, ett datorramverk som automatiskt kan föreslå detaljerade enzymreaktionssteg med endast grundläggande kemisk information, och som hjälper forskare att designa bättre enzymer för medicin, industri och hållbar kemi.
Från saknade steg till en digital detektiv
De flesta biokemiska databaser listar vad som går in i en enzymdriven reaktion och vad som kommer ut, men inte sekvensen av bindningsbrott och bindningsbildningar däremellan. Färre än tusen reaktioner i litteraturen är annoterade med fullständiga mekanismer, vilket lämnar ett stort ”mekanismgap”. Tidigare beräkningsverktyg försökte fylla detta gap men krävde ofta detaljerade 3D‑strukturer av enzymer eller förhandskunskap om vilka aminosyror i proteinet som utför kemin, vilket kraftigt begränsade deras räckvidd. MechFind angriper problemet på ett annat sätt: det bortser från hela proteinet i 3D och fokuserar istället på hur små kemiska delar omarrangeras, vilket gör att det kan hantera vilken reaktion som helst där ingångs‑ och utgångsmolekylerna är kända.
Att bryta ner kemin i enkla byggstenar
I kärnan av MechFind finns ett ”moiety‑baserat” synsätt på kemi. Istället för att följa hela molekyler delar metoden upp dem i små märkta fragment baserat på varje atoms omedelbara grannar. Den representerar sedan en reaktion som vinster och förluster av dessa fragment. Med hjälp av en stor, kurerad samling kända enzymatiska steg sätter MechFind ihop kedjor av små fragmentförändringar som tillsammans reproducerar den övergripande reaktionen. Den föredrar de enklaste förklaringarna, söker efter mekanismer med så få steg som möjligt och upprätthåller strikt bevarande av atomer och laddning så att inget framstår eller försvinner olagligt under processen.
Kontrollera noggrannhet och upptäcka nya vägar
För att avgöra om dess förutsägelser är rimliga testade författarna först MechFind på hundratals reaktioner vars mekanismer redan dokumenterats i en betrodd databas. Med enbart start‑ och slutmolekyler som indata återvann MechFind den accepterade mekanismen som sitt främsta val i nästan två tredjedelar av fallen och placerade den bland topp tio i 85 % av fallen. Teamet utmanade sedan systemet med sex nyligen publicerade enzymmekanismer som det aldrig tidigare sett. MechFind identifierade fortfarande den korrekta steggemenskapen bland sina ledande kandidater, ofta genom att återanvända kemiska mönster härledda från obesläktade arter—till exempel genom att bygga en human enzymmekanism från steg som ursprungligen lärts in från jäst‑ eller växtenzymer.
Skalning upp till tiotusentals reaktioner
Efter att ha validerat sin noggrannhet släppte författarna lös MechFind på två stora samlingar av biokemiska reaktioner, täckande nästan 38 000 distinkta reaktioner. För mer än hälften av reaktionerna i varje databas producerade verktyget åtminstone en möjlig flerstegs‑mekanism, ofta med upp till tio alternativa vägar. Detta arbete genererade över 18 000 nya mekanistiska hypoteser, en mer än tiofaldig ökning av antalet reaktioner med föreslagna detaljerade steg. Samtidigt belyste storskaliga tester var metoden för närvarande misslyckas—antingen för att optimeringen blir för komplex inom den tilldelade beräkningstiden, eller för att de nödvändiga fragmenttyperna aldrig förekom i träningsdata.
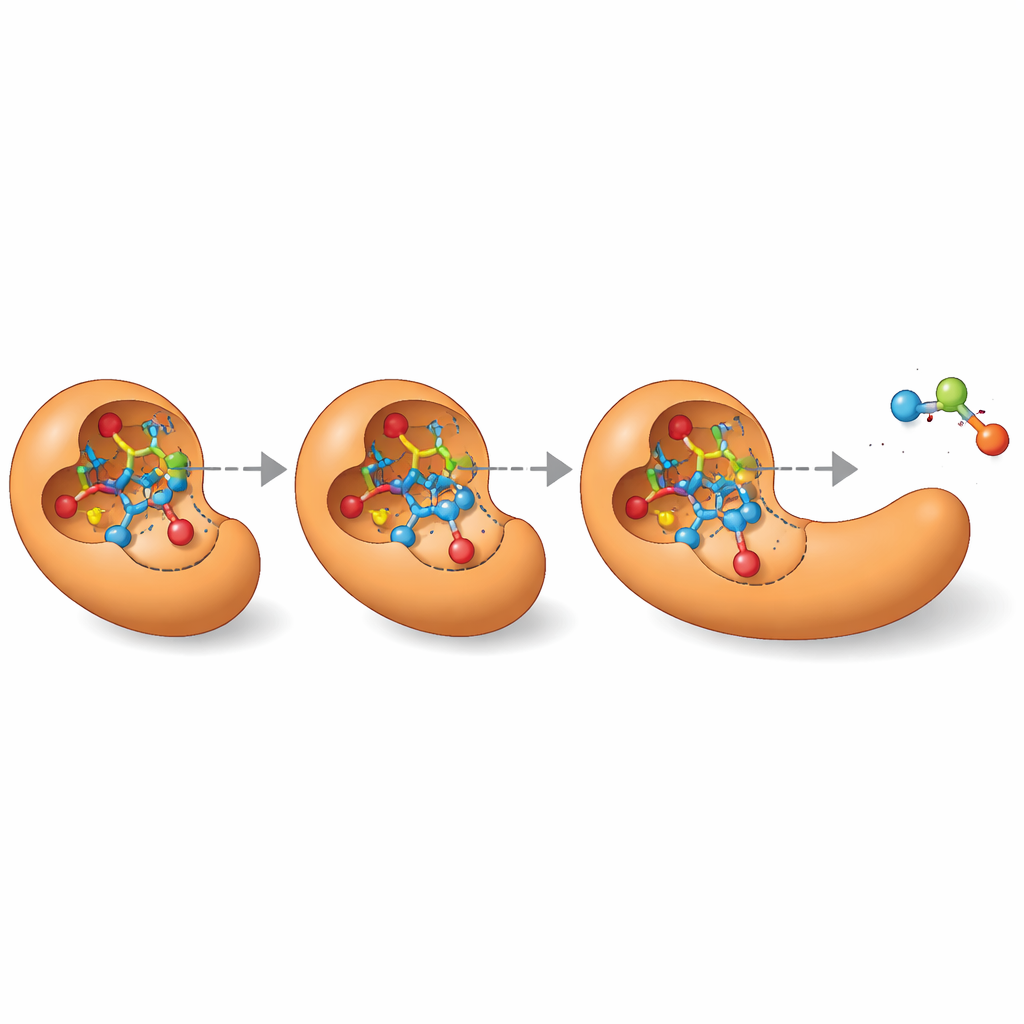
Öppnar dörrar för enzymdesign
Utöver att lista en enda ”bästa gissning” kan MechFind kartlägga hela nätverk av olika rimliga vägar som ett enzym kan använda för en given reaktion. Detta landskap av alternativ är särskilt värdefullt för att designa nya enzymer från grunden. Moderna proteindesignverktyg behöver en exakt tredimensionell bild av de flyktiga övergångstillstånd som reaktioner passerar genom. Genom att redogöra för stegvisa mekanismer pekar MechFind direkt på dessa nyckelintermediärer och övergångstillstånd, och förvandlar vaga designmål som ”bygg en esteras” till konkreta mål som ”stabilisera denna särskilda högenergistruktur.” Även om dess förutsägelser fortfarande kräver expertgranskning och uppföljande beräkningar eller experiment, utvidgar MechFind vårt katalog över möjliga enzymkemier avsevärt och banar en praktisk väg mot mer systematisk, datadriven enzymteknik.
Citering: Hartley, A.D., Upadhyay, V., Boorla, V.S. et al. MechFind: a computational framework for de novo prediction of enzyme mechanisms. Nat Commun 17, 3903 (2026). https://doi.org/10.1038/s41467-026-71957-0
Nyckelord: enzymmekanismer, beräkningsbiokemi, enzymdesign, metaboliska reaktioner, reaktionsförutsägelse