Clear Sky Science · ar
MechFind: إطار حسابي للتنبؤ من الصفر بآليات الإنزيمات
لماذا فهم الإنزيمات مهم
تعمل كل خلية حية بواسطة آلات جزيئية صغيرة تُسمى الإنزيمات. تسرّع هذه البروتينات التفاعلات الكيميائية التي تزود أجسامنا بالطاقة، وتُنمّي المحاصيل، وتصنّع الأدوية. وعلى الرغم من أننا نعرف كيمياء «قبل وبعد» آلاف التفاعلات الإنزيمية، نادراً ما نعرف الحركات الدقيقة خطوة بخطوة التي تقود من المواد الأولية إلى النواتج النهائية. يقدم هذا العمل MechFind، إطاراً حاسوبياً يمكنه اقتراح خطوات تفصيلية لتفاعلات الإنزيم تلقائياً باستخدام معلومات كيميائية أساسية فقط، مما يساعد العلماء على تصميم إنزيمات أفضل للطب والصناعة والكيمياء المستدامة.
من خطوات مفقودة إلى محقق رقمي
تدرج معظم قواعد البيانات الكيميائية الحيوية ما يدخل تفاعلاً تحركه الإنزيمات وما يخرج منه، لكنها لا تسجل تتابع كسر وكون الروابط في ما بينهما. أقل من ألف تفاعل في الأدبيات موشّح بآلية كاملة، تاركاً «فجوة في الآليات» واسعة. حاولت أدوات حسابية سابقة سد هذه الفجوة لكنها غالباً ما كانت تتطلب هياكل ثلاثية الأبعاد مفصّلة للإنزيمات أو معرفة مسبقة بالأحماض الأمينية المسؤولة عن الكيمياء، مما قلّص من نطاق تطبيقها بشدة. يتعامل MechFind مع المشكلة بطريقة مختلفة: يتجاهل البنية البروتينية ثلاثية الأبعاد ويركّز بدلاً من ذلك على كيفية إعادة ترتيب القطع الكيميائية الصغيرة، مما يتيح له العمل على أي تفاعل معروف فيه الجزيئات الداخلة والخارجة.
تحويل الكيمياء إلى لبنات بناء بسيطة
في جوهر MechFind رؤية «معتمدة على المجموعات» للكيمياء. بدلاً من تتبع الجزيئات الكاملة، يكسر الأسلوب الجزيئات إلى شظايا معنونة صغيرة استناداً إلى جيران كل ذرة المباشرين. ثم يمثل أي تفاعل ككسب وخسارة لهذه الشظايا. باستخدام مجموعة كبيرة ومنقّحة من الخطوات الإنزيمية المعروفة، يجمع MechFind سلاسل من تغيّرات الشظايا الصغيرة التي تعيد إنتاج التفاعل الكلي. يفضّل التفسيرات الأبسط، باحثاً عن آليات بعدد خطوات أقل ممكن ويفرض حفظاً صارماً للذرات والشحنة بحيث لا يظهر أو يختفي شيء بطريقة غير قانونية على طول الطريق.
التحقق من الدقّة واكتشاف مسارات جديدة
لمعرفة ما إذا كانت تنبؤاته منطقية، اختبر المؤلفون MechFind أولاً على مئات التفاعلات التي كانت آلياتها موثقة بالفعل في قاعدة بيانات موثوقة. باستخدام الجزيئات الابتدائية والنهائية فقط كمدخلات، استعاد MechFind الآلية المقبولة كخياره الأول في ما يقرب من ثلثي الحالات ووضعها ضمن الخيارات العشرة الأولى في 85% منها. ثم تحدى الفريق النظام بست آليات إنزيمية مُنشورة حديثاً لم يرها من قبل. لا يزال MechFind يحدد تتابع الخطوات الصحيح من بين المرشحين الأوائل له، غالباً بإعادة استخدام أنماط كيميائية مشتقة من أنواع غير مرتبطة، مثل بناء آلية إنزيم بشري اعتماداً على خطوات تعلّمها في الأصل من خميرة أو نباتات.
التوسّع إلى عشرات الآلاف من التفاعلات
بعد التحقق من دقته، أطلق المؤلفون MechFind على مجموعتين رئيسيتين من تفاعلات الكيمياء الحيوية، تغطيان ما يقرب من 38,000 تفاعل مميز. لأكثر من نصف التفاعلات في كل قاعدة بيانات، أنتجت الأداة آلية متعددة الخطوات معقولة على الأقل، مقترحة غالباً حتى عشرة مسارات بديلة. ولدت هذه الجهود أكثر من 18,000 فرضية آلية جديدة، بزيادة تفوق عشرة أضعاف في عدد التفاعلات ذات الخطوات التفصيلية المقترحة. وفي الوقت نفسه، أبرز الاختبار واسع النطاق الأماكن التي يفشل فيها الأسلوب حالياً — إما لأن التحسين يصبح معقداً جداً خلال زمن الحوسبة المخصص، أو لأن أنواع الشظايا اللازمة لم تظهر أبداً في بيانات التدريب.
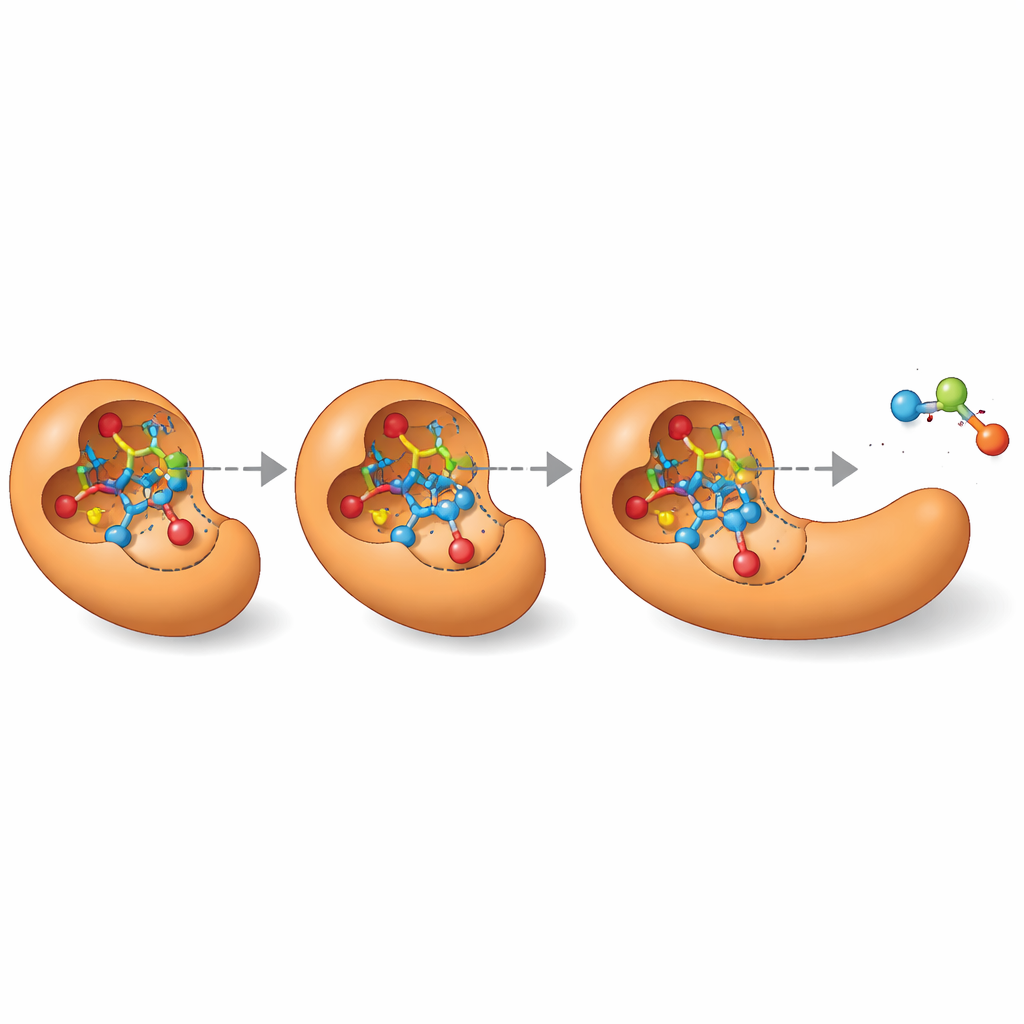
فتح آفاق لتصميم الإنزيمات
بعيداً عن سرد «أفضل تخمين» واحد، يمكن لـ MechFind رسم شبكات كاملة من المسارات المنطقية المختلفة التي قد يستخدمها إنزيم لتفاعل معين. تُعتبر هذه الخريطة من البدائل ذات قيمة خاصة لتصميم إنزيمات جديدة من الصفر. تحتاج أدوات تصميم البروتين الحديثة إلى صورة ثلاثية الأبعاد دقيقة لحالات العبور العابرة التي تمر بها التفاعلات. من خلال عرض آليات خطوة بخطوة، يوجّه MechFind مباشرة إلى تلك الوسائط والحوامل الانتقالية الرئيسية، محوّلاً أهداف التصميم الغامضة مثل «بناء إستراز» إلى أهداف ملموسة مثل «تثبيت هذا البناء عالي الطاقة المحدد». ورغم أن تنبؤاته لا تزال تتطلب مراجعة خبراء وحسابات أو تجارب متابعة، يوسّع MechFind بشكل كبير كتالوج الكيمياءات الإنزيمية الممكنة ويمهّد طريقاً عملياً نحو هندسة إنزيمية أكثر نظامية ومبنية على البيانات.
الاستشهاد: Hartley, A.D., Upadhyay, V., Boorla, V.S. et al. MechFind: a computational framework for de novo prediction of enzyme mechanisms. Nat Commun 17, 3903 (2026). https://doi.org/10.1038/s41467-026-71957-0
الكلمات المفتاحية: آليات الإنزيمات, الكيمياء الحيوية الحاسوبية, تصميم الإنزيمات, التفاعلات الأيضية, التنبؤ بالتفاعلات