Clear Sky Science · nl
MechFind: een computationeel kader voor de novo voorspelling van enzymmechanismen
Waarom het begrijpen van enzymen ertoe doet
Elke levende cel draait op kleine moleculaire machines die enzymen worden genoemd. Deze eiwitten versnellen chemische reacties die ons lichaam aandrijven, gewassen laten groeien en medicijnen produceren. Hoewel we de algemene “voor en na”-chemie voor tienduizenden enzymreacties kennen, weten we zelden de exacte stap‑voor‑stap bewegingen die ze gebruiken om van uitgangsstoffen naar eindproducten te komen. Dit artikel introduceert MechFind, een computerkader dat automatisch gedetailleerde stappen van enzymreacties kan voorstellen met alleen basischemische informatie, waarmee wetenschappers helpen betere enzymen te ontwerpen voor geneeskunde, industrie en duurzame chemie.
Van ontbrekende stappen naar een digitale detective
De meeste biochemische databases vermelden wat er in een enzymgedreven reactie gaat en wat eruit komt, maar niet de reeks van bindingsbreuk- en bindingsvormingsgebeurtenissen daartussen. Minder dan duizend reacties in de literatuur zijn voorzien van volledige mechanismen, wat een grote “mechanismekloof” achterlaat. Eerdere computationele tools probeerden deze kloof te dichten maar vereisten vaak gedetailleerde 3D-structuren van enzymen of voorafgaande kennis van welke aminozuren in het eiwit de chemie uitvoeren, wat hun toepasbaarheid sterk beperkte. MechFind pakt het probleem anders aan: het negeert het volledige 3D-eiwit en concentreert zich in plaats daarvan op hoe kleine chemische onderdelen worden herschikt, waardoor het op elke reactie kan werken waarvan de input- en outputmoleculen bekend zijn.
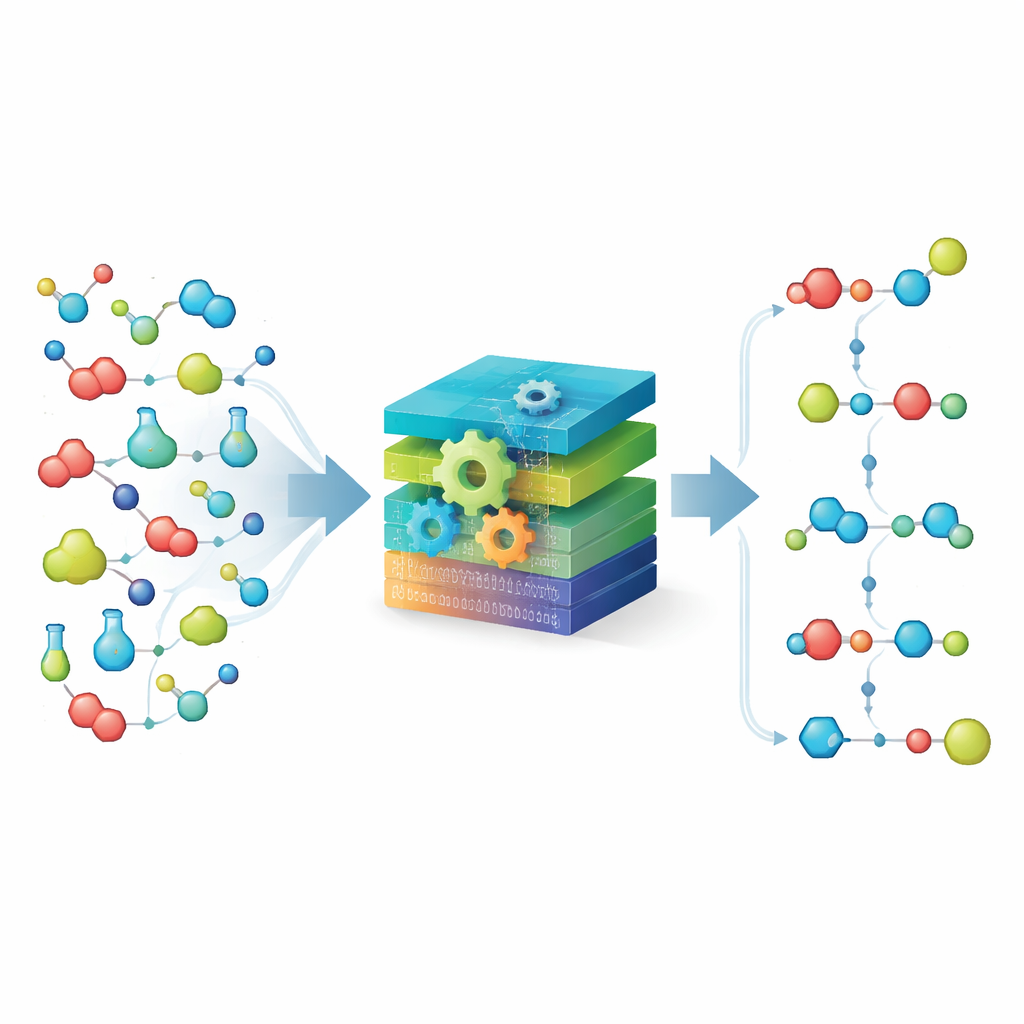
Chemie opdelen in eenvoudige bouwstenen
Centraal in MechFind staat een “moe-tiegebaseerde” kijk op chemie. In plaats van hele moleculen te volgen, splitst de methode ze op in kleine gelabelde fragmenten op basis van de directe buren van elk atoom. Vervolgens stelt het elke reactie voor als winst en verlies van deze fragmenten. Met behulp van een grote, gekuiste verzameling bekende enzymatische stappen zet MechFind ketens van kleine fragmentveranderingen in elkaar die samen de totale reactie reproduceren. Het geeft de voorkeur aan de eenvoudigste verklaringen, zoekt naar mechanismen met zo min mogelijk stappen en handhaaft strikte behoudswetten voor atomen en lading zodat er onderweg niets onwettig verschijnt of verdwijnt.
Nauwkeurigheid controleren en nieuwe paden ontdekken
Om te beoordelen of de voorspellingen logisch zijn, testten de auteurs MechFind eerst op honderden reacties waarvan de mechanismen al in een betrouwbare database waren gedocumenteerd. Met alleen de begin- en eindmoleculen als input vond MechFind het geaccepteerde mechanisme als eerste keus in bijna twee derde van de gevallen en plaatste het binnen de top tien in 85% van de gevallen. Het team daagde het systeem vervolgens uit met zes recent gepubliceerde enzymmechanismen die het nog nooit had gezien. MechFind identificeerde nog steeds de juiste stapvolgorde onder zijn voornaamste kandidaten, vaak door chemische patronen te hergebruiken die waren afgeleid van niet-verwante soorten, zoals het opbouwen van een menselijk enzymmechanisme uit stappen die oorspronkelijk uit gist- of plantenenzymen waren geleerd.
Opschalen naar tienduizenden reacties
Na validatie van de nauwkeurigheid zetten de auteurs MechFind los op twee grote collecties biochemische reacties, die gezamenlijk bijna 38.000 verschillende reacties bestrijken. Voor meer dan de helft van de reacties in elke database produceerde het hulpmiddel ten minste één plausibel meerstappenmechanisme, en vaak tot tien alternatieve paden. Deze inspanning genereerde meer dan 18.000 nieuwe mechanistische hypothesen, een meer dan tienvoudige toename van het aantal reacties met voorgestelde gedetailleerde stappen. Tegelijkertijd liet de grootschalige test zien waar de methode momenteel faalt — ofwel omdat de optimalisatie te complex wordt binnen de beschikbare rekentijd, of omdat de benodigde fragmenttypen nooit in de trainingsdata voorkwamen.
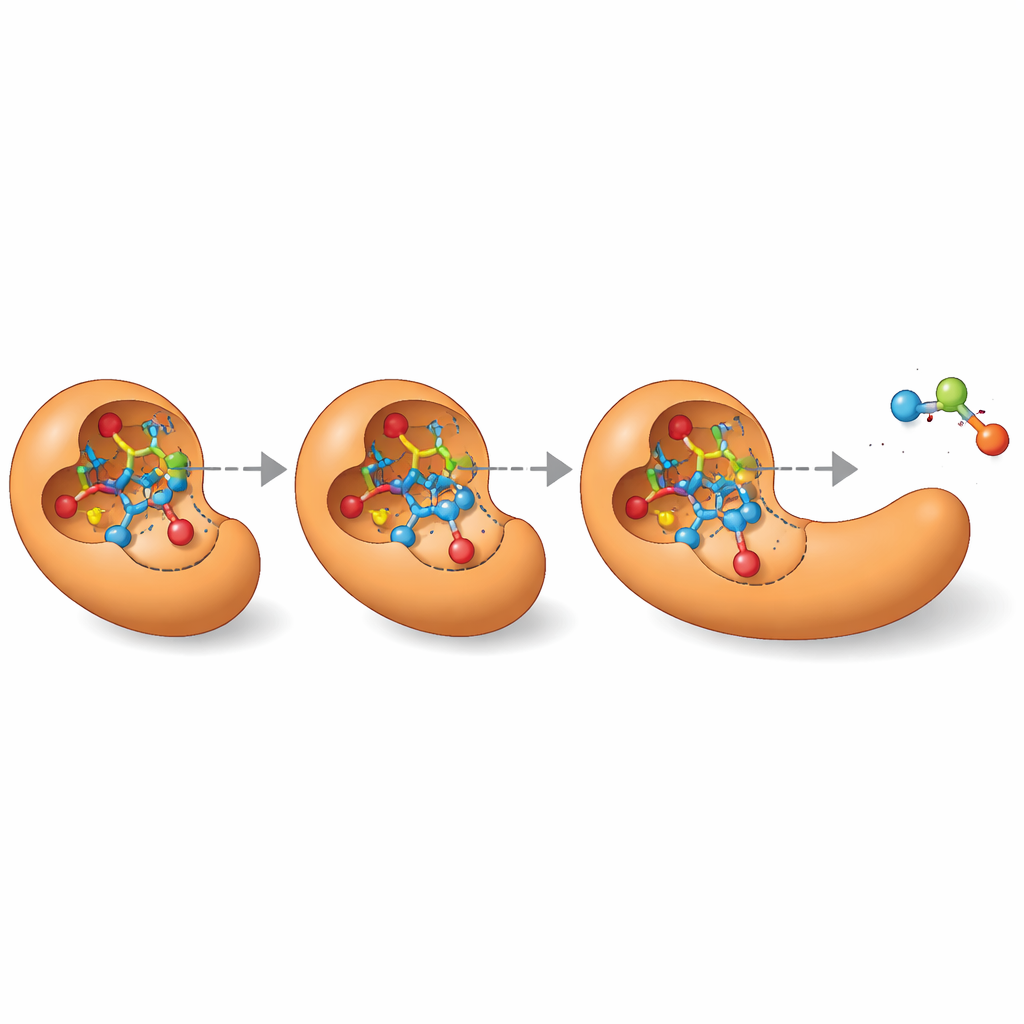
Deuren openen voor enzymontwerp
Buiten het opsommen van één “beste gok” kan MechFind volledige netwerken van verschillende plausibele routes in kaart brengen die een enzym voor een bepaalde reactie zou kunnen gebruiken. Dit landschap van alternatieven is vooral waardevol voor het ontwerpen van nieuwe enzymen vanaf nul. Moderne eiwitontwerptools hebben een nauwkeurig driedimensionaal beeld nodig van de vluchtige overgangstoestanden die reacties doorlopen. Door stapsgewijze mechanismen uit te tekenen, wijst MechFind direct naar die sleutelintermediaten en overgangstoestanden, waardoor vage ontwerptaken zoals “bouw een esterase” veranderen in concrete doelen zoals “stabiliseer deze specifieke hoge-energie structuur.” Hoewel de voorspellingen nog steeds deskundige beoordeling en vervolgberekeningen of -experimenten vereisen, vergroot MechFind wezenlijk ons repertoire aan mogelijke enzymchemieën en toont het een praktisch pad naar meer systematische, data‑gestuurde enzymengineering.
Bronvermelding: Hartley, A.D., Upadhyay, V., Boorla, V.S. et al. MechFind: a computational framework for de novo prediction of enzyme mechanisms. Nat Commun 17, 3903 (2026). https://doi.org/10.1038/s41467-026-71957-0
Trefwoorden: enzymmechanismen, computationele biochemie, enzymontwerp, metabole reacties, reactievoorspelling