Clear Sky Science · sv
Genomisk härledning av överföringsplatser under regional spridning av blaNDM Klebsiella pneumoniae i Michigan
Varför detta dolda sjukhushot är viktigt
Antibiotikaresistenta mikrober kan tyst följa med patienter när de flyttas mellan sjukhus, vårdhem och rehabiliteringscenter. När hälsomyndigheter upptäcker en farlig stam behöver de snabbt veta var den sprids och vilka anläggningar som omedvetet för den vidare. Denna studie visar hur läsning av bakteriers DNA, tillsammans med rutinmässiga journaler över patientrörelser, kan avslöja dessa dolda överföringshottspots över en hel region.
Att följa en farlig mikrob över Michigan
Forskarlaget fokuserade på en särskilt oroande bakterie, Klebsiella pneumoniae, som utvecklat resistens mot kraftfulla karbapenemantibiotika genom en gen känd som blaNDM-1. Mellan slutet av 2019 och 2022 samlade myndigheterna i Michigan in prover från 72 patienter som vårdats på 47 olika vårdinrättningar. Vad som först såg ut att vara ett problem i ett enskilt sjukhus växte till ett regionalt problem när fall dök upp på många fler platser. Genom att jämföra bakteriernas fullständiga DNA-sekvenser fann teamet att nästan alla dessa fall spårades till en enda nyligen introducerad stam som expanderat och spridit sig, snarare än många oberoende importfall.
Att använda DNA som ett kontaktspårningsverktyg
För att förstå hur stamen rörde sig räknade forskarna inte bara hur många DNA-förändringar som skilde ett prov från ett annat. Istället använde de en metod kallad "maximum shared variants" som enkelt frågar: för varje nytt fall, vilka tidigare prover är dess närmaste genetiska grannar. Eftersom denna metod inte bygger på en hård gräns i genetisk distans kan den fånga både mycket täta länkar och något mer avlägsna samband som ändå sannolikt har en nyligen gemensam källa. Forskarna lade sedan patienternas tidigare vårdvistelser ovanpå DNA:s släktträd för att se var genetiskt nära patienter överlappat i tid och rum.

Att peka ut sannolika spridningsplatser
För varje patient simulerade teamet en utredning i realtid och låtsades att de endast kände till fall rapporterade fram till det aktuella tillfället. De sökte efter överlapp i vårdexponering mellan ett nytt fall och dess närmaste genetiska matchningar. När mer än hälften av dessa kopplingar pekade mot samma anläggning markerades den platsen som den mest sannolika där patienten smittats. Med denna regel kunde de tilldela en enda sannolik källanläggning för 66 av 70 analyserbara patienter. Ungefär hälften av fallen förklarades bäst av spridning inom den anläggning där de diagnostiserades, medan resten verkade vara infektioner som uppnåtts på andra institutioner och förts in av patienter.
Avslöjande av viktiga nav och dolda reservoarer
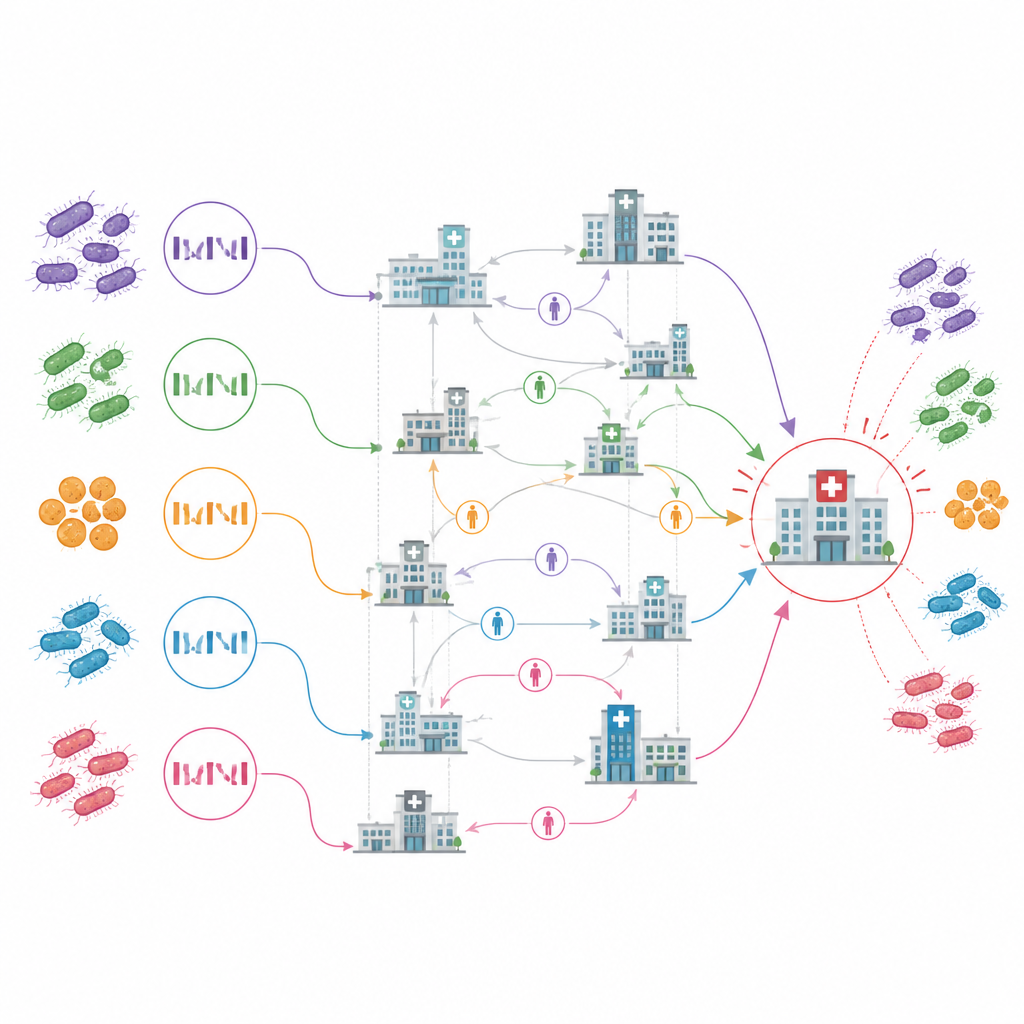
Kartan över överföringar mellan anläggningar satte en akutvårdssjukhus, betecknat ACH10 i studien, i centrum. Det var den tidigaste platsen med fall, visade pågående spridning inom sina väggar och framstod som ursprung för mer än en fjärdedel av fallen av spridning mellan anläggningar. De flesta andra länkar mellan vårdinrättningar föreföll vara engångsintroduktioner med begränsad vidare spridning. Anmärkningsvärt nog implicerade analysen flera anläggningar som sannolika källor till infektion innan de själva rapporterat något fall, och flaggade till och med vissa anläggningar som aldrig rapporterade fall men som låg på vanliga exponeringsvägar för nära besläktade infektioner.
Vad detta betyder för smittskyddet
Genom att kombinera bakterie-DNA med rutininformation om var patienter vistats visar denna studie att hälsomyndigheter kan återskapa hur en resistent stam rör sig genom ett helt nätverk av sjukhus och vårdcenter med de prover som redan samlas in. Metoden hjälper till att identifiera vilka anläggningar som driver regional spridning, vilka som främst tar emot importerade fall och var dolda reservoarer kan pyra innan någon märker det. Med denna typ av realtidsövervakning baserad på genomdata kan folkhälsoteam snabbare rikta rengöring, screening och isoleringsinsatser till rätt platser och därigenom bromsa framfarten hos farliga antibiotikaresistenta bakterier över en region.
Citering: Wan, T., McNamara, S., Brennan, B. et al. Genomic inference of sites of transmission during regional spread of blaNDM Klebsiella pneumoniae in Michigan. Nat Commun 17, 4154 (2026). https://doi.org/10.1038/s41467-026-70839-9
Nyckelord: antibiotikaresistens, sjukhusinfektioner, genomisk övervakning, Klebsiella pneumoniae, patientöverföringar