Clear Sky Science · es
Inferencia genómica de los sitios de transmisión durante la propagación regional de Klebsiella pneumoniae con blaNDM en Michigan
Por qué importa esta amenaza oculta en los hospitales
Los gérmenes resistentes a los antibióticos pueden moverse silenciosamente con los pacientes cuando se transfieren entre hospitales, residencias de ancianos y centros de rehabilitación. Cuando las autoridades sanitarias detectan una cepa peligrosa, necesitan con urgencia saber dónde se está propagando y qué instalaciones la están transmitiendo sin saberlo. Este estudio muestra cómo leer el ADN de las bacterias, junto con los registros rutinarios de movimiento de pacientes, puede revelar esos puntos calientes de transmisión ocultos en toda una región.
Siguiendo a un germen peligroso por Michigan
Los investigadores se centraron en una bacteria particularmente preocupante llamada Klebsiella pneumoniae que había aprendido a resistir los potentes antibióticos carbapenémicos mediante un gen conocido como blaNDM-1. Entre finales de 2019 y 2022, las autoridades sanitarias de Michigan recogieron muestras de 72 pacientes atendidos en 47 centros sanitarios diferentes. Lo que al principio parecía un problema en un solo hospital se convirtió en un asunto regional a medida que los casos aparecían en muchos más lugares. Al comparar las secuencias completas del ADN de las bacterias, el equipo encontró que casi todos estos casos remitían a una única introducción reciente de una sola cepa que se expandió y propagó, en lugar de múltiples importaciones no relacionadas.
Usar el ADN como herramienta de rastreo de contactos
Para entender cómo se movió la cepa, el equipo no se limitó a contar cuántos cambios en el ADN separaban una muestra de otra. En su lugar, emplearon un enfoque de “máximos variantes compartidas” que simplemente pregunta: para cada caso nuevo, cuáles de las muestras anteriores son sus vecinas genéticas más cercanas. Dado que este método no depende de un umbral rígido de distancia genética, puede capturar tanto enlaces muy estrechos como otros un poco más distantes que aun así probablemente comparten una fuente reciente. Los científicos superpusieron luego las estancias previas en centros sanitarios de los pacientes sobre el árbol genealógico del ADN, comprobando dónde los pacientes genéticamente cercanos coincidieron en tiempo y lugar.

Localizar los sitios probables de propagación
Para cada paciente, el equipo simuló una investigación en tiempo real, fingiendo que solo conocían los casos notificados hasta ese momento. Buscaron solapamientos en la exposición a instalaciones entre un caso nuevo y sus coincidencias genéticas más cercanas. Cuando más de la mitad de esos enlaces apuntaban a la misma instalación, ese lugar se etiquetaba como el sitio más probable donde el paciente adquirió la cepa resistente. Usando esta regla, pudieron asignar una única instalación fuente probable para 66 de los 70 pacientes analizables. Aproximadamente la mitad de los casos se explicaron mejor por la propagación dentro de la instalación donde fueron diagnosticados, mientras que el resto parecía reflejar infecciones adquiridas en otras instituciones y traídas por los pacientes.
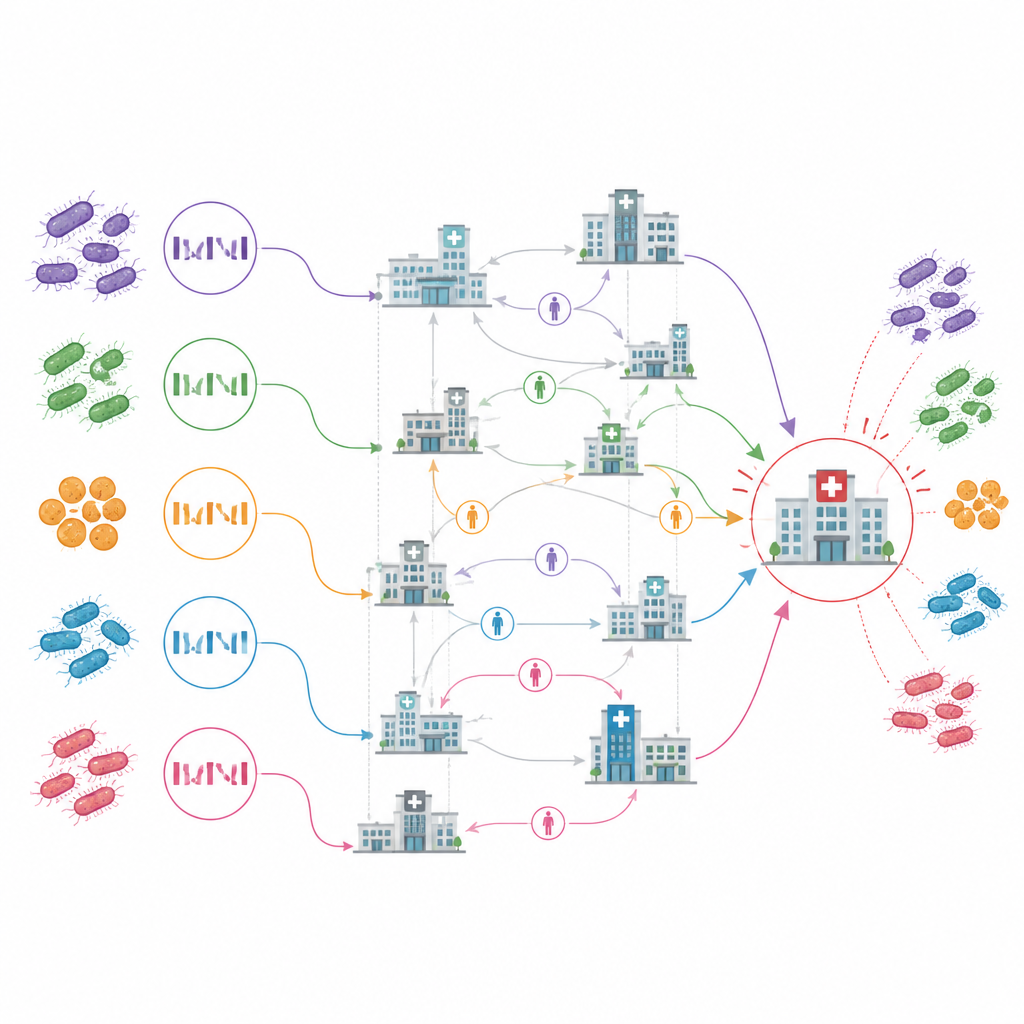
Revelando focos clave y reservorios ocultos
El mapa resultante de transmisión entre instalaciones destacó a un hospital de atención aguda, etiquetado como ACH10 en el estudio, como un centro neurálgico. Fue el sitio más temprano con casos, mostró propagación continua dentro de sus instalaciones y apareció como la fuente de más de una cuarta parte de los eventos de transmisión entre centros. La mayoría de los otros enlaces entre instalaciones parecieron ser introducciones puntuales con solo una propagación limitada posteriormente. De forma llamativa, el análisis también identificó varias instalaciones como fuentes probables de infección antes de que hubieran notificado algún caso, e incluso señaló algunas que nunca reportaron casos pero que se situaban en rutas comunes de exposición para infecciones estrechamente relacionadas.
Qué significa esto para el control de infecciones
Al combinar el ADN bacteriano con la información rutinaria sobre dónde han estado los pacientes, este estudio demuestra que las agencias sanitarias pueden reconstruir cómo se mueve una cepa resistente a través de toda una red de hospitales y centros de atención usando las muestras que ya recogen. El enfoque ayuda a identificar qué instalaciones están impulsando la propagación regional, cuáles reciben principalmente casos importados y dónde pueden existir reservorios ocultos antes de que nadie lo note. Con este tipo de vigilancia en tiempo real informada por genomas, los equipos de salud pública podrían dirigir más rápidamente las labores de limpieza, cribado y aislamiento a los lugares adecuados, frenando el avance de bacterias resistentes a los antibióticos en una región.
Cita: Wan, T., McNamara, S., Brennan, B. et al. Genomic inference of sites of transmission during regional spread of blaNDM Klebsiella pneumoniae in Michigan. Nat Commun 17, 4154 (2026). https://doi.org/10.1038/s41467-026-70839-9
Palabras clave: resistencia a antibióticos, infecciones hospitalarias, vigilancia genómica, Klebsiella pneumoniae, traslados de pacientes