Clear Sky Science · nl
Genomische reconstructie van transmissieplaatsen tijdens regionale verspreiding van blaNDM Klebsiella pneumoniae in Michigan
Waarom deze verborgen ziekenhuisdreiging ertoe doet
Antibioticaresistente microben kunnen geruisloos meereizen met patiënten wanneer zij van ziekenhuis naar verpleeghuis of revalidatiecentrum worden overgeplaatst. Wanneer volksgezondheidsdiensten een gevaarlijke stam ontdekken, moeten ze snel weten waar die zich verspreidt en welke instellingen die onbedoeld doorgeven. Deze studie toont hoe het lezen van het DNA van bacteriën, gecombineerd met routinematige gegevens over patiëntbewegingen, deze verborgen transmissiebrandhaarden over een hele regio kan onthullen.
Een gevaarlijke kiem volgen door Michigan
De onderzoekers richtten zich op een bijzonder zorgwekkende bacterie, Klebsiella pneumoniae, die resistentie had ontwikkeld tegen krachtige carbapenem‑antibiotica via een gen dat bekendstaat als blaNDM‑1. Tussen eind 2019 en 2022 verzamelden de autoriteiten in Michigan monsters van 72 patiënten die in 47 verschillende zorginstellingen werden behandeld. Wat aanvankelijk op een probleem in één ziekenhuis leek, groeide uit tot een regionaal vraagstuk toen gevallen in veel meer locaties opdoken. Door de volledige DNA‑reeksen van de bacteriën te vergelijken, vond het team dat bijna alle gevallen terug te voeren waren op één recente introductie van een enkele stam die zich had uitgebreid en verspreid, in plaats van op vele niet‑verwante importen.
DNA gebruiken als een contactonderzoekstool
Om te begrijpen hoe de stam zich verplaatste, telde het team niet alleen hoeveel DNA‑veranderingen twee monsters van elkaar scheidden. In plaats daarvan gebruikten ze een methode met "maximum shared variants" die eenvoudigweg vraagt: voor elk nieuw geval, welke eerdere monsters zijn diens dichtstbijzijnde genetische buren. Omdat deze methode niet afhankelijk is van een harde drempel in genetische afstand, kan ze zowel zeer nauwe verbanden als iets verdere maar nog steeds recent gedeelde bronnen vastleggen. De wetenschappers legden vervolgens de eerdere verblijven van patiënten over de genetische stamboom heen en onderzochten waar genetisch nauwe patiënten in tijd en plaats overlappen.

Waarschijnlijk verspreidingsplaatsen aanwijzen
Voor elke patiënt simuleerde het team een onderzoek in real time en deed alsof ze alleen kennis hadden van gevallen die tot dat moment waren gemeld. Ze zochten naar overlap in blootstelling aan instellingen tussen een nieuwe zaak en diens dichtstbijzijnde genetische matches. Wanneer meer dan de helft van die verbanden naar dezelfde instelling verwees, werd die locatie aangeduid als de meest waarschijnlijke plaats waar de patiënt de resistente stam had opgelopen. Met deze regel konden ze voor 66 van de 70 analyseerbare patiënten één waarschijnlijke broninstelling toewijzen. Ongeveer de helft van de gevallen was het beste te verklaren door verspreiding binnen de instelling waar ze werden gediagnosticeerd, terwijl de rest leek te wijzen op infecties die in andere instellingen waren opgelopen en door patiënten waren meegebracht.
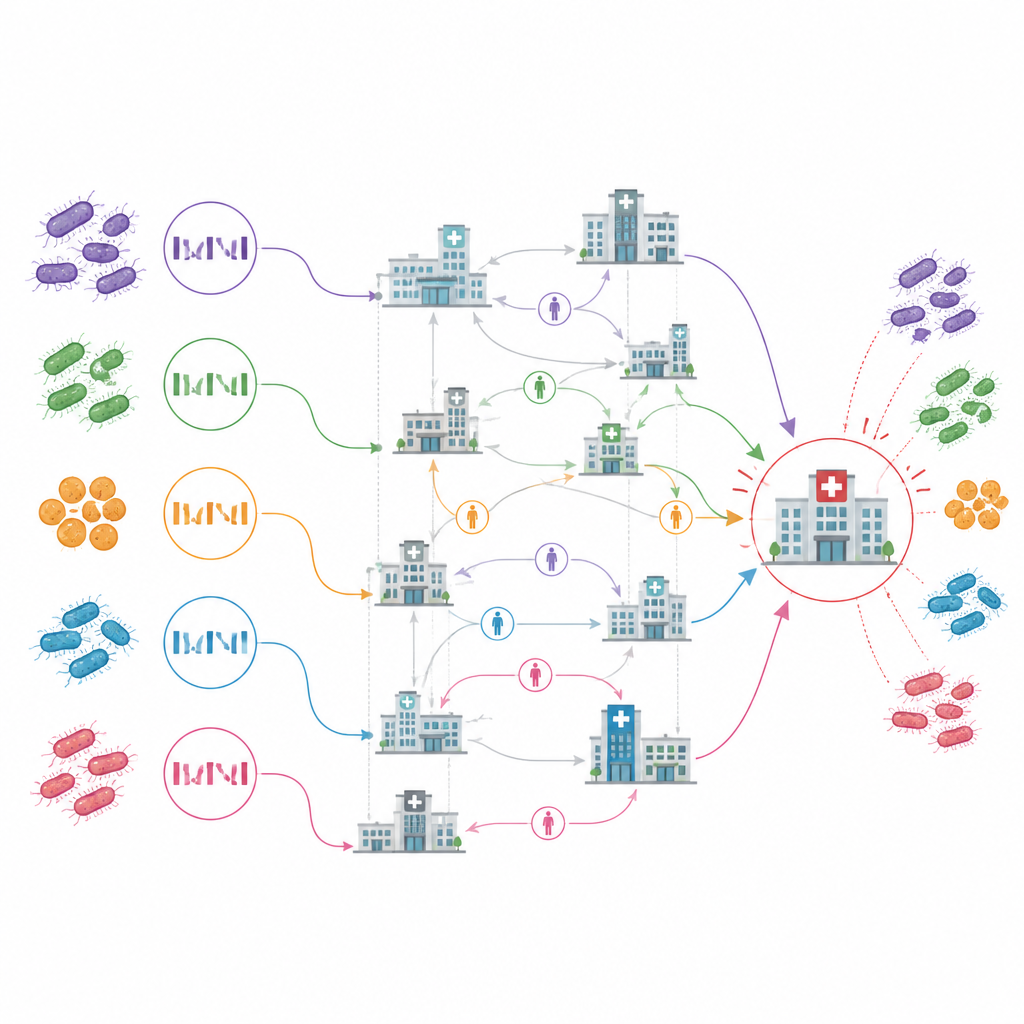
Belangrijke knooppunten en verborgen reservoirs onthuld
De resulterende kaart van transmissie tussen instellingen benadrukte één acute zorgziekenhuis, aangeduid als ACH10 in de studie, als een centraal knooppunt. Het was de vroegste locatie met gevallen, toonde voortdurende verspreiding binnen de muren en leek de bron te zijn voor meer dan een kwart van de transmissiegebeurtenissen tussen instellingen. De meeste andere verbindingen tussen instellingen leken eenmalige introducties met slechts beperkte verdere verspreiding. Opvallend genoeg wees de analyse ook een aantal instellingen aan als waarschijnlijke bronnen van infectie voordat ze ooit zelf een geval hadden gemeld, en markeerde zelfs enkele instellingen die nooit gevallen rapporteerden maar wel op veelvoorkomende blootstellingsroutes voor nauw verwante infecties lagen.
Wat dit betekent voor infectiecontrole
Door bacterieel DNA te combineren met routinematige informatie over waar patiënten zijn geweest, laat deze studie zien dat gezondheidsinstanties kunnen reconstrueren hoe een resistente stam zich door een heel netwerk van ziekenhuizen en zorgcentra beweegt met behulp van de monsters die ze al verzamelen. De aanpak helpt te identificeren welke instellingen de regionale verspreiding aanjagen, welke vooral geïmporteerde gevallen ontvangen en waar verborgen reservoirs mogelijk sudderen voordat iemand het opmerkt. Met dit soort real‑time, genomisch geïnformeerde surveillance kunnen publieke gezondheidsteams sneller schoonmaak-, screenings- en isolatiemaatregelen op de juiste plekken richten en zo de opmars van gevaarlijke antibioticaresistente bacteriën in een regio vertragen.
Bronvermelding: Wan, T., McNamara, S., Brennan, B. et al. Genomic inference of sites of transmission during regional spread of blaNDM Klebsiella pneumoniae in Michigan. Nat Commun 17, 4154 (2026). https://doi.org/10.1038/s41467-026-70839-9
Trefwoorden: antibioticaresistentie, ziekenhuisinfecties, genomische surveillance, Klebsiella pneumoniae, patiëntverplaatsingen