Clear Sky Science · ar
الاستدلال الجينومي لمواقع الانتقال أثناء الانتشار الإقليمي لبكتيريا Klebsiella pneumoniae حاملة blaNDM في ميشيغان
لماذا تهديد المستشفيات المخفي هذا مهم
يمكن للجراثيم المقاومة للمضادات الحيوية أن تنتقل بهدوء مع المرضى أثناء نقلهم بين المستشفيات ودور رعاية المسنين ومراكز التأهيل. عندما يكتشف مسؤولو الصحة سلالة خطرة، يحتاجون على وجه السرعة لمعرفة الأماكن التي تنتشر فيها وأي المرافق تنقلها دون أن تدري. تظهر هذه الدراسة كيف يمكن لقراءة الحمض النووي للبكتيريا، إلى جانب سجلات تحركات المرضى الروتينية، أن تكشف عن بقع الانتقال المخفية عبر منطقة بأكملها.
ملاحقة جرثوم خطير عبر ميشيغان
ركز الباحثون على بكتيريا مقلقة تُسمى Klebsiella pneumoniae التي طورت مقاومة لمضادات الكاربابينيم القوية عبر جين معروف باسم blaNDM-1. بين أواخر 2019 و2022، جمعت السلطات الصحية في ميشيغان عينات من 72 مريضاً عولجوا في 47 مرفق رعاية صحي مختلف. ما بدا في البداية كمشكلة في مستشفى واحد تطور إلى قضية إقليمية مع ظهور حالات في أماكن متعددة. بمقارنة التسلسلات الكاملة للحمض النووي للبكتيريا، وجد الفريق أن معظم هذه الحالات تعود إلى إدخال حديث واحد لسلالة مفردة توسعت وانتشرت، وليس إلى العديد من الواردات غير المرتبطة.
استخدام الحمض النووي كأداة لتتبع المخالَطين
لفهم كيفية تحرك السلالة، لم يقتصر الفريق على عد التغييرات الجينية بين عينة وأخرى. بدلاً من ذلك، استخدموا نهج "أقصى المتغيرات المشتركة" الذي يسأل ببساطة: بالنسبة لكل حالة جديدة، أي العينات الأقدم هي أقرب الجيران جينياً. ونظراً لأن هذه الطريقة لا تعتمد على حد قاسٍ للمسافة الجينية، فهي تلتقط الروابط الوثيقة جداً وتلك الأبعد قليلاً التي لا تزال على الأرجح تشترك في مصدر حديث. ثم وضع العلماء إقامة المرضى السابقة في مرافق الرعاية فوق شجرة العائلة الجينية، ليروا أين تداخل المرضى ذوو القرابة الجينية من حيث الزمن والمكان.

تحديد مواقع الترجيح للانتشار
بالنسبة لكل مريض، لمح الفريق تحقيقاً في الوقت الحقيقي على نحو محاكاة، متظاهراً بأنهم يعرفون فقط الحالات المبلغ عنها حتى تلك اللحظة. بحثوا عن تداخلات في التعرض للمرافق بين الحالة الجديدة وأقرب التطابقات الجينية لها. عندما أشارت أكثر من نصف تلك الروابط إلى نفس المرفق، وُسِم ذلك الموقع كأكثر الأماكن احتمالاً لاكتساب المريض السلالة المقاومة. باستخدام هذه القاعدة، تمكنوا من تعيين مرفق واحد على الأرجح كمصدر لـ 66 من أصل 70 مريضاً قابلاً للتحليل. نحو نصف الحالات كانت تُفسَّر أفضل على أنها انتشار داخل المرفق الذي شُخِصت فيه، بينما بدا أن الباقي يعكس عدوى اكتسبت في مؤسسات أخرى وحُملت بواسطة المرضى.
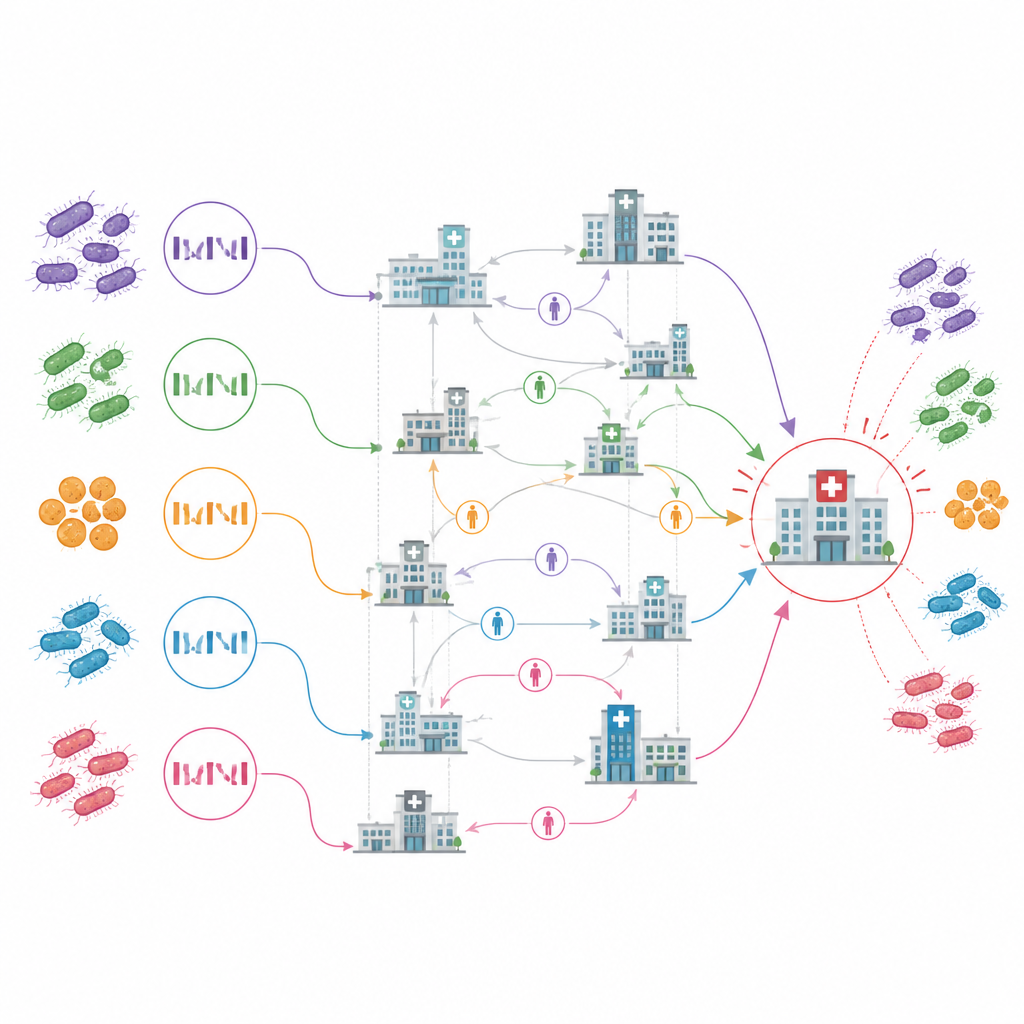
كشف المحاور الرئيسية والمخازن المخفية
أبرزت خريطة الانتقال الناتجة بين المرافق مستشفى رعاية حادة واحداً، وُسِم ACH10 في الدراسة، كمحور مركزي. كان الموقع الأقدم الذي ظهرت فيه حالات، وأظهر استمرار الانتشار داخل جدرانه، وظهر كمصدر لأكثر من ربع أحداث الانتقال بين المرافق. بدا أن معظم الروابط الأخرى بين المرافق تمثل إدخالات لمرة واحدة مع انتشار لاحق محدود. بشكل لافت، أشارت التحليلات أيضاً إلى أن بعض المرافق كانت مصادر محتملة للعدوى قبل أن تبلغ عن أي حالة بنفسها، وحتى وسمت بعض المرافق التي لم تُبلغ أبداً عن حالات لكنها كانت تقع على مسارات شائعة للتعرض لحالات متقاربة جينياً.
ماذا يعني ذلك لمكافحة العدوى
من خلال دمج حمضية البكتيريا مع معلومات روتينية حول أماكن إقامة المرضى، تُظهر هذه الدراسة أن وكالات الصحة يمكنها إعادة بناء كيفية تحرك سلالة مقاومة عبر شبكة كاملة من المستشفيات ومراكز الرعاية باستخدام العينات التي يجمعونها بالفعل. يساعد هذا النهج في تحديد أي المرافق تقود الانتشار الإقليمي، وأيها تستقبل في المقام الأول حالات واردة، وأين قد تكون المخازن المخفية تتكون قبل أن يلاحظها أحد. مع هذا النوع من المراقبة المبنية على الجينوم في الوقت الحقيقي، يمكن لفرق الصحة العامة توجيه جهود التنظيف والفحص والعزل بشكل أسرع إلى الأماكن المناسبة، مما يبطئ تقدم البكتيريا المقاومة للمضادات عبر المنطقة.
الاستشهاد: Wan, T., McNamara, S., Brennan, B. et al. Genomic inference of sites of transmission during regional spread of blaNDM Klebsiella pneumoniae in Michigan. Nat Commun 17, 4154 (2026). https://doi.org/10.1038/s41467-026-70839-9
الكلمات المفتاحية: مقاومة المضادات الحيوية, العدوى المرتبطة بالمستشفيات, المراقبة الجينومية, Klebsiella pneumoniae, نقل المرضى