Clear Sky Science · pl
Wnioskowanie genomowe miejsc transmisji podczas regionalnego rozprzestrzeniania się Klebsiella pneumoniae z genem blaNDM w Michigan
Dlaczego to ukryte zagrożenie w szpitalach ma znaczenie
Bakterie odporne na antybiotyki mogą potajemnie przemieszczać się z pacjentami podczas transferów między szpitalami, domami opieki i ośrodkami rehabilitacyjnymi. Gdy służby zdrowia wykrywają niebezpieczny szczep, pilnie muszą ustalić, gdzie się rozprzestrzenia i które placówki nieświadomie go przekazują. Badanie to pokazuje, jak analiza DNA bakterii, połączona z rutynowymi zapisami o przemieszczaniu pacjentów, może ujawnić te ukryte ogniska transmisji w całym regionie.
Śledzenie niebezpiecznej bakterii w Michigan
Naukowcy skupili się na szczególnie niepokojącej bakterii Klebsiella pneumoniae, która nabyła oporność na potężne karbapenemy dzięki genowi znanemu jako blaNDM-1. W okresie od końca 2019 do 2022 roku służby zdrowia w Michigan zebrały próbki od 72 pacjentów leczonych w 47 różnych placówkach. To, co początkowo wyglądało jak problem w jednym szpitalu, przekształciło się w sprawę o zasięgu regionalnym, gdy przypadki pojawiły się w wielu innych miejscach. Porównanie pełnych sekwencji DNA bakterii wykazało, że niemal wszystkie te przypadki można przypisać jednej niedawnej introdukcji pojedynczego szczepu, który się rozrósł i rozprzestrzenił, a nie wielu niezależnym importom.
Wykorzystanie DNA jak narzędzia do śledzenia kontaktów
Aby zrozumieć, jak szczep się przemieszczał, zespół nie ograniczał się do zliczania, ile zmian w DNA oddzielało próbki. Zamiast tego zastosowali podejście „maksymalnych wspólnych wariantów”, które po prostu pyta: dla każdego nowego przypadku, które wcześniejsze próbki są jego najbliższymi genetycznymi sąsiadami. Ponieważ metoda ta nie opiera się na twardym progu odległości genetycznej, może uchwycić zarówno bardzo ciasne powiązania, jak i nieco dalsze, które nadal prawdopodobnie mają wspólne niedawne źródło. Naukowcy następnie nałożyli wcześniejsze pobyty pacjentów w placówkach na drzewo genealogiczne DNA, sprawdzając, gdzie genetycznie bliscy pacjenci mieli czasowe i miejscowe nakładanie się pobytów.

Wskazywanie najbardziej prawdopodobnych miejsc rozprzestrzeniania
Dla każdego pacjenta zespół symulował dochodzenie w czasie rzeczywistym, udając, że zna tylko przypadki zgłoszone do tego momentu. Szukali nakładających się ekspozycji w placówkach między nowym przypadkiem a jego najbliższymi genetycznymi odpowiednikami. Gdy ponad połowa tych powiązań wskazywała tę samą placówkę, site oznaczano jako najbardziej prawdopodobne miejsce, w którym pacjent nabył oporny szczep. Stosując tę zasadę, mogli przypisać pojedynczą prawdopodobną placówkę źródłową dla 66 z 70 analizowanych pacjentów. Około połowy przypadków najlepiej tłumaczono transmisją wewnątrz placówki, w której zdiagnozowano pacjenta, podczas gdy pozostałe wydawały się odzwierciedlać infekcje nabyte w innych instytucjach i przywiezione przez pacjentów.
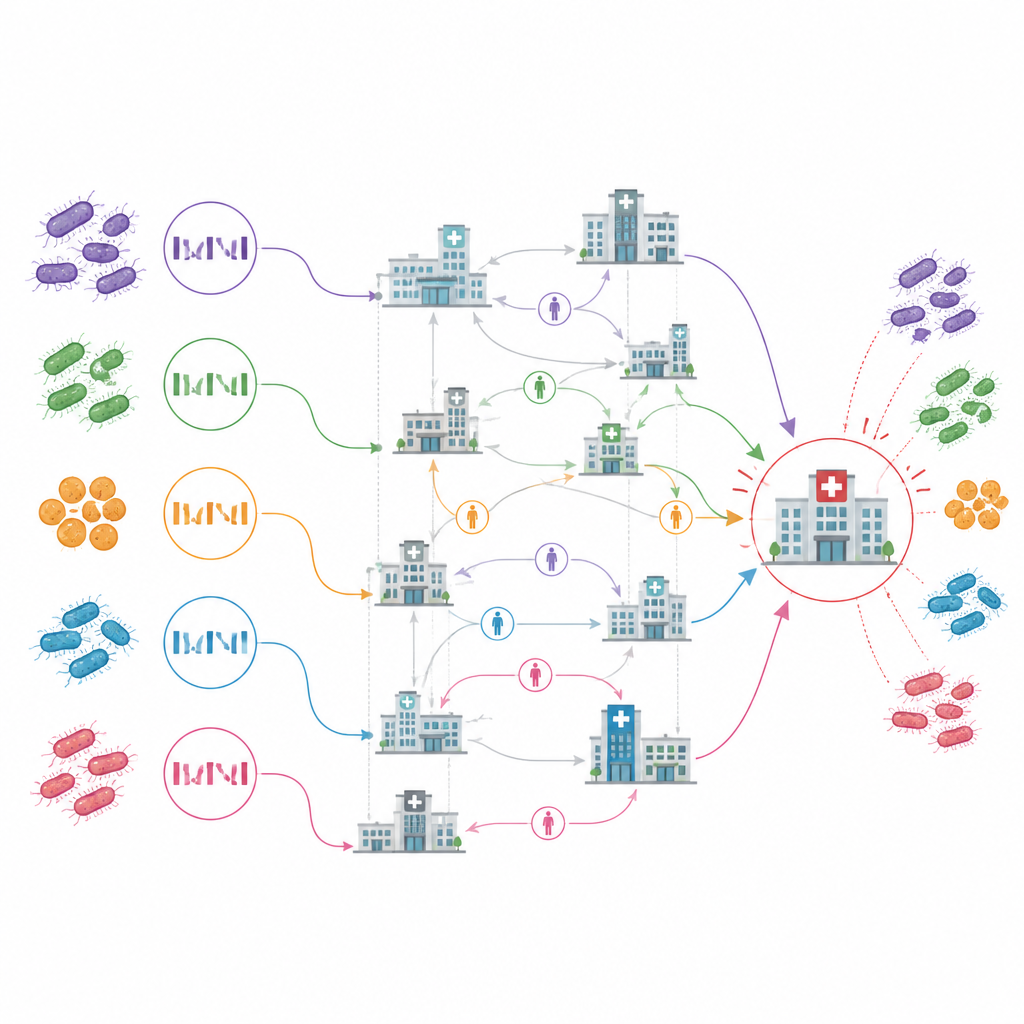
Odkrywanie kluczowych węzłów i ukrytych rezerwuarów
Mapa transmisji między placówkami wykazała, że jeden szpital opieki ostrej, oznaczony w badaniu jako ACH10, był centralnym węzłem. Był to najwcześniejszy lokal z przypadkami, wykazywał ciągłe rozprzestrzenianie w obrębie placówki i wydawał się źródłem ponad jednej czwartej zdarzeń transmisji między placówkami. Większość innych powiązań między placówkami wyglądała na jednorazowe introdukcje z ograniczonym dalszym rozprzestrzenianiem. Co uderzające, analiza również wskazała kilka placówek jako prawdopodobne źródła zakażeń zanim w ogóle zgłosiły swój pierwszy przypadek, a nawet zidentyfikowała niektóre placówki, które nigdy nie zgłosiły żadnych przypadków, lecz znajdowały się na wspólnych ścieżkach ekspozycji dla blisko spokrewnionych infekcji.
Co to oznacza dla kontroli zakażeń
Łącząc DNA bakterii z rutynowymi informacjami o tym, gdzie byli pacjenci, badanie pokazuje, że agencje zdrowia publicznego mogą zrekonstruować, jak oporny szczep porusza się przez całą sieć szpitali i ośrodków opieki, korzystając z próbek, które już zbierają. Podejście to pomaga zidentyfikować, które placówki napędzają rozprzestrzenianie w regionie, które głównie otrzymują importowane przypadki oraz gdzie mogą tlić się ukryte rezerwuary zanim ktokolwiek je zauważy. Przy takim genomowo-informowanym nadzorze w czasie rzeczywistym zespoły zdrowia publicznego mogłyby szybciej ukierunkować działania związane ze sprzątaniem, przesiewami i izolacją na właściwe miejsca, spowalniając rozprzestrzenianie się niebezpiecznych bakterii odpornych na antybiotyki w regionie.
Cytowanie: Wan, T., McNamara, S., Brennan, B. et al. Genomic inference of sites of transmission during regional spread of blaNDM Klebsiella pneumoniae in Michigan. Nat Commun 17, 4154 (2026). https://doi.org/10.1038/s41467-026-70839-9
Słowa kluczowe: oporność na antybiotyki, infekcje szpitalne, nadzór genomowy, Klebsiella pneumoniae, przemieszczanie pacjentów